抑制“有氧糖酵解”!上海交通大学发文:发现逆转“癌王”恶性进展的新靶点
| 导读 | 胰腺导管腺癌(PDAC)以基质硬化和糖代谢重编程为特征,尤其是瓦博格效应。然而,这些特征之间复杂的相互作用及其对肿瘤进展的影响仍未得到充分探讨。 |
8月17日,上海交通大学研究团队在期刊《Cell Reports》上发表了研究论文,题为“A CLIC1 network coordinates matrix stiffness and the Warburg effect to promote tumor growth in pancreatic cancer”,本研究中,研究人员整合了临床、细胞和生物信息学方法,探索了PDAC中基质刚度和瓦博格效应之间的联系,发现CLIC1是一个关键介质。在功能上,CLIC1可作为糖酵解代谢的催化剂,促进肿瘤增殖。机制上,CLIC1通过抑制活性氧簇(ROS)的羟化来增强HIF1α的稳定性。总之,PDAC细胞以基质刚度响应的方式提高了CLIC1水平,通过ROS/HIF1α信号增强瓦博格效应来驱动肿瘤生长。本研究见解强调了同时处理基质特性和代谢重组的靶向治疗的机会,CLIC1正成为一个有前景的干预点。

https://www.cell.com/cell-reports/fulltext/S2211-1247(24)00983-5#%20
背景知识
01
未经修饰的细胞外基质(ECM)通过其免疫功能和血管及结缔组织成分,在应对损伤时具有维持稳态的关键支持性功能。然而,癌症会劫持这种生理反应,并诱导周围组织基质发生改变,为肿瘤的快速生长创造有利的肿瘤微环境(TME)。ECM是肿瘤微环境中最丰富的非细胞固体成分,不仅维持肿瘤组织的三维形态结构,还通过生物化学或生物物理信号影响肿瘤细胞的生物学特性。在实体肿瘤中,ECM蛋白质的沉积、重塑和交联导致基质硬化的机械和物理特性。ECM丰富的癌症类型——胰腺导管腺癌(PDAC)突出了这一特点。致密的ECM不仅物理上阻碍了血管系统并限制了静脉治疗药物的输送,而且还诱导缺氧并抑制肿瘤免疫。这些与ECM刚度相关的障碍反过来会损害肿瘤内信号通路,如上皮转化生长因子β(TGF-β),并进一步激活经典的PDAC促进因子,如STAT3激活和SMAD4突变。因此,肿瘤的恶性进展和患者的不良预后与PDAC高度纤维化的性质相关。
基质在PDAC(胰腺癌)的多种表征中扮演着重要角色,包括增殖、侵袭、转移、凋亡、血管生成、淋巴管生成以及免疫逃逸。其中,ECM(细胞外基质)通常被阐释为肿瘤的保护盾以及关键刺激因子。然而,其对生物物理信号的影响尚未得到充分研究CAFs是ECM的主要成分,它改变了细胞表面的稳态力,并将由外源性基质产生的机械信号传递给细胞,反过来诱导细胞的生物学行为,如外泌体分泌和肿瘤干细胞富集,并激活内部信号通路,最终影响肿瘤细胞的上皮间质转化、代谢变化、侵袭和转移。基于上述考虑,可以提出假设,明确ECM在PDAC中的作用和机制,通过靶向PDAC肿瘤微环境的机械特性,特别是通过调节ECM的硬度,可能为这种致命疾病提供一种新的治疗途径。
细胞代谢最近已发展成为受机械信号调节的过程之一。为满足肿瘤的能量和物质需求,代谢重编程是肿瘤的核心特征之一。最近有报道称,ECM硬度参与了复杂的代谢重编程的调节,包括糖代谢,如葡萄糖摄取和有氧糖酵解,脂质代谢,如脂肪酸吸收和分解,以及氨基酸代谢,如谷氨酰胺和天冬氨酸交换。在这些过程中,肿瘤细胞倾向于在充足的氧气供应条件下通过糖酵解获取能量,这被称为瓦博格效应。重要的是,与富含间质的肿瘤,如乳腺癌不同,瓦博格效应仍然是在患者来源的组织或小鼠模型中检测到的PDAC的主要代谢效应。此外,瓦博格效应在富含间质的肿瘤微环境中更有利于PDAC细胞的生存和增殖。而且,靶向瓦博格效应可以有效抑制肿瘤进展。因此,阐明瓦博格效应过程的核心调节因子对于开发PDAC的治疗靶点至关重要。然而,需注意的是,PDAC中瓦博格效应过程的TME(尤其是ECM硬度)的作用尚未完全阐明。这些事实迫切需要研究揭示ECM硬度与瓦博格效应之间的关联,以寻找新的治疗靶点或疗效预测标志物。
CLIC1通过增强瓦博格效应促进PDAC细胞的生长
02
为了确定CLIC1如何促进PDAC进展,研究人员使用GEO和TCGA公共数据库进行了基因集富集分析(GSEA)。多个数据库中的HALLMARK_GLYCOLYSIS通路在高CLIC1表达样本中富集。这一结果也得到了TCGA队列的基因相关性分析的支持,该分析显示CLIC1表达与两种常用的糖酵解标志物之间存在显著的正相关。这些发现促使研究人员推测CLIC1可能在PDAC的有氧糖酵解中发挥作用。CLIC1调节PDAC细胞的瓦博格效应这一想法得到了以下结果的支持。(1) qPCR结果显示,CLIC1的遗传修饰对葡萄糖转运蛋白和许多糖酵解成分的mRNA表达产生了显著影响。(2) CLIC1敲低降低了细胞外酸化率(糖酵解的指标),而CLIC1过表达则产生了相反的效果。(3) CLIC1OE细胞的葡萄糖摄取和乳酸生成增强,而CLIC1KD细胞则出现了相反的结果。(4) 在14例接受18F-氟脱氧葡萄糖PET-CT检查的PDAC样本的IHC染色中,高CLIC1表达与SUV-max值较高相一致,反映了代谢活性,而低表达则相反。此外,在克隆形成模型中添加两种糖酵解抑制剂(2-DG和乳糖)显著抑制了CLIC1促进克隆形成的能力,这意味着CLIC1通过有氧糖酵解促进细胞增殖。
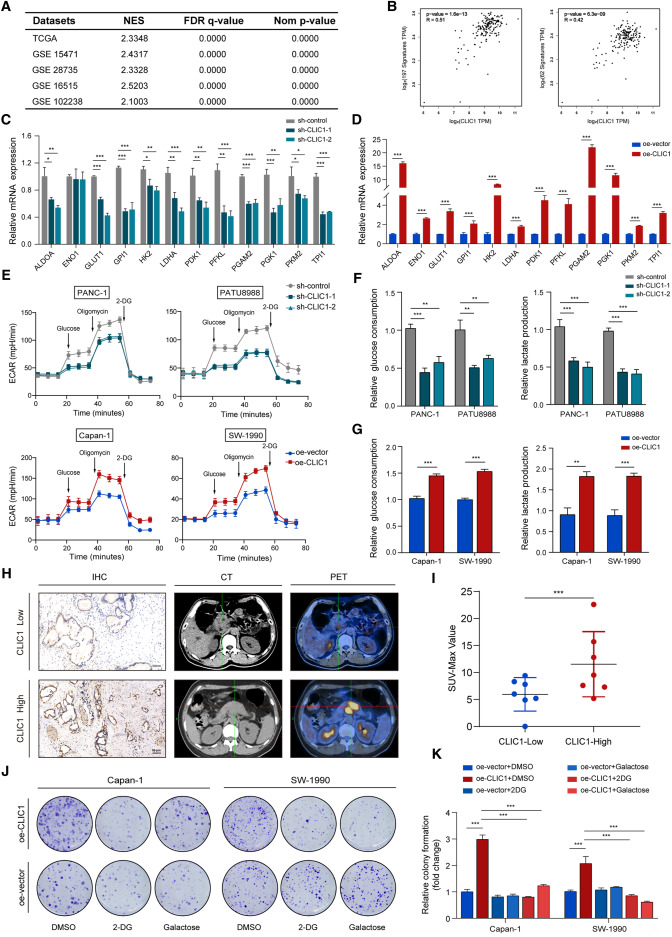
CLIC1通过增强瓦博格效应促进PDAC细胞的生长
研究小结
03
总之,本研究揭示了CLIC1在PDAC中发挥重要作用,其中由基质硬度增加引起的CLIC1表达增加促进了瓦博格效应。此外,研究人员的发现提供了对CLIC1参与HIF1α稳定过程的更深入的理解,通过在ROS水平依赖性的方式中抑制HIF1α的羟基化来实现。上述研究结果表明,靶向CLIC1/ROS/HIF1α轴以抑制有氧糖酵解并逆转PDAC的恶性进展是完全可行的。(转化医学网360zhyx.com)
【参考资料】
https://www.cell.com/cell-reports/fulltext/S2211-1247(24)00983-5#%20
【关于投稿】
转化医学网(360zhyx.com)是转化医学核心门户,旨在推动基础研究、临床诊疗和产业的发展,核心内容涵盖组学、检验、免疫、肿瘤、心血管、糖尿病等。如您有最新的研究内容发表,欢迎联系我们进行免费报道(公众号菜单栏-在线客服联系),我们的理念:内容创造价值,转化铸就未来!
转化医学网(360zhyx.com)发布的文章旨在介绍前沿医学研究进展,不能作为治疗方案使用;如需获得健康指导,请至正规医院就诊。
 腾讯登录
腾讯登录









还没有人评论,赶快抢个沙发