新见解!南京医科大学/南通大学合作发文:靶向STING通路的肿瘤治疗新策略
| 导读 | 染色体外环状DNA (extracchromosomal circular DNA, eccDNAs)是一类双链DNA (double-stranded DNA, dsdna),可促进DNA传感机制的激活,与多种疾病的进展和预后有关。虽然eccDNAs的作用仍存在争议,但其在弥漫大B细胞淋巴瘤(DLBCL)中的意义尚未见报道。 |
8月25日,南京医科大学与南通大学研究人员合作在期刊《Clinical And Translational Medicine》上发表了研究论文,题为“Multi-omics integration reveals the oncogenic role of eccDNAs in diffuse large B-cell lymphoma through STING signalling”,本研究中,研究人员发现EccDNAs在DLBCL中广泛表达,且与患者预后相关。eccDNAs丰度的升高促进了DLBCL的进展。化疗药物诱导的DNA损伤触发eccDNAs的生成,导致STING信号以非cGAS依赖的方式激活。此外,抑制STING与顺铂具有协同抗肿瘤作用。这一发现为化疗联合靶向STING提供了合理的治疗策略。

https://onlinelibrary.wiley.com/doi/full/10.1002/ctm2.1815
背景知识
01
弥漫大B细胞淋巴瘤(DLBCL)是全球最主要的非霍奇金淋巴瘤,每年新发病例达15万例。虽然大多数患者可以通过R-CHOP(利妥昔单抗、环磷酰胺、多柔比星、长春新碱和泼尼松)免疫化疗获得缓解,但仍有相当比例(30-40%)的患者治疗失败并最终死亡。虽然在DLBCL的基础研究方面取得了一定的进展,但加深对DLBCL发病机制的理解,制定改善患者预后的策略仍是当务之急。
染色体外环状DNA (eccDNAs)是一类以环状形式存在的双链DNA (dsdna)。eccDNAs来源于基因组DNA,独立于染色体运作。据报道,由eccDNAs编码的基因如MYC和EGFR通过自我复制的过程比染色体基因更有效地扩增。eccDNAs的不均匀分离可能有助于理解这一现象,并为eccDNAs如何促进肿瘤发生提供新的见解。eccDNAs的形成可受到DNA损伤修复途径、染色体畸变、细胞凋亡等未知因素的影响。染色体畸变导致这些生物学过程中的基因组重排,形成的序列可以连接和环化形成eccDNAs,增加癌基因的拷贝数和表达。eccDNAs在肿瘤诊断、靶向治疗和预后评估中的潜在应用已被探索。然而,eccDNAs在DLBCL中的作用尚不清楚。
cGAS-STING信号通路由第二信使环GMP-AMP合成酶(cGAS)和干扰素基因环GMP-AMP受体刺激因子(STING)组成,捕获异常DNA,从而激活针对病毒感染的固有免疫应答。cGAS-STING信号通路在调控自噬、蛋白质翻译、代谢稳态、DNA损伤修复、细胞衰老和细胞死亡等方面发挥了多方面的作用。不平衡的cGAS-STING信号通路已被发现与恶性疾病有关,并在肿瘤中表现出双重作用。例如,细胞核cGAS抑制DNA修复并促进肿瘤生长。STING通路及其下游非经典NF-κB信号的激活驱动了肿瘤的演变。同时,研究人员发现癌细胞内在的STING激活有助于抑制肺腺癌转移。靶向cGAS-STING轴的选择性小分子抑制剂和激动剂的研发在多种疾病中取得了令人惊讶的疗效。研究人员迫切需要深入了解cGAS-STING通路的作用,以拓宽对DLBCL的认识。
化疗药物诱导的DNA损伤引起eccDNAs的生成并激活STING信号通路
02
既往研究报道,DNA损伤可诱导eccDNAs的产生。检测DNA损伤标志物组蛋白H2AX Ser 139位点磷酸化(γH2AX)在DLBCL细胞株中的表达水平。H组细胞γH2AX表达高于L组。γH2AX的表达与ecdna丰度呈正相关。此外,化疗药物如顺铂、多柔比星、伊立替康和靶向药物奥拉帕利的治疗确实诱导了DNA损伤。另外,这些药物还触发了eccDNAs的产生。双链DNA水平也随着DNA损伤而升高。同时,p-STING及其下游蛋白和参与非经典NF-κB信号通路的蛋白表达显著增强。为了进一步验证体内DNA损伤和eccDNAs之间的关联,研究人员使用顺铂处理U2932细胞建立的免疫缺陷小鼠模型。免疫组织化学(IHC)检测证实顺铂处理的小鼠肿瘤中γH2AX水平升高。同样,研究人员也观察到eccDNAs的上调。免疫荧光法检测顺铂处理组细胞中dsDNA和p-STING的表达,证实顺铂处理组细胞中dsDNA和p-STING的表达增加。为了研究这些发现是否适用于免疫系统功能正常的小鼠,研究人员使用小鼠B细胞淋巴瘤细胞系(A20)建立了免疫功能正常的小鼠模型,并观察到一致的结果。
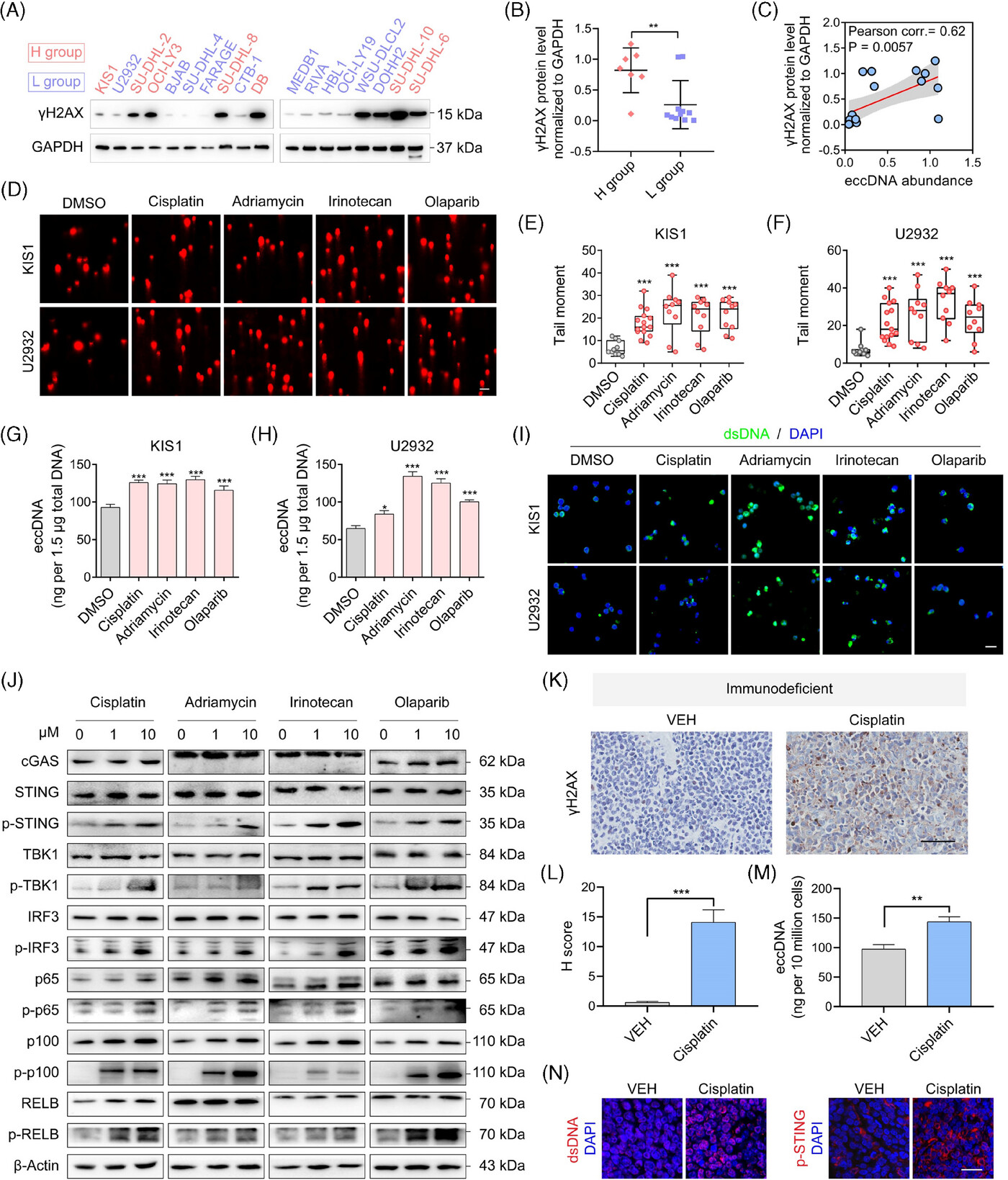
DNA损伤化疗药物促进eccDNAs的生成和STING信号通路的激活
抑制STING与顺铂具有协同抗肿瘤作用
03
研究表明STING和TBK1的抑制呈剂量依赖性地抑制细胞生长,而cGAS抑制剂和STING激动剂对细胞生长无明显抑制作用。另一种STING抑制剂H-151在更多的细胞系中使用,在多个细胞系中观察到显著的抑制作用。随后,流式细胞术分析显示h -151诱导细胞凋亡,蛋白质免疫印迹实验显示h -151处理后活化的凋亡蛋白水平增加。此外,STING抑制剂H-151和C-176分别显著延缓了免疫缺陷和免疫正常小鼠模型的肿瘤生长。接下来,研究人员将H-151与dna损伤剂联合处理。值得注意的是,在大多数情况下,联合治疗显著增强了对细胞活力的抑制。C-176 (STING的特异性抑制剂)也能抑制A20细胞的增殖。与顺铂联用时观察到合成效应。TBK1抑制剂治疗也增强了顺铂的疗效。在体内实验中,与溶剂或单药治疗相比,顺铂联合STING抑制剂H-151的抗肿瘤作用显著增强。免疫组织化学法检测到PCNA水平显著降低,证实了这一结果。免疫正常小鼠给予C-176和顺铂后肿瘤生长最慢,PCNA表达水平最低。
研究小结
04
总之,本研究发现强调了eccDNAs通过不依赖cgas的方式激活STING信号通路在肿瘤发生中的有趣作用。这些结果显著促进了研究人员对DLBCL中eccDNAs的理解,并为患者的治疗策略提供了新的见解。(转化医学网360zhyx.com)
【参考资料】
https://onlinelibrary.wiley.com/doi/full/10.1002/ctm2.1815
【关于投稿】
转化医学网(360zhyx.com)是转化医学核心门户,旨在推动基础研究、临床诊疗和产业的发展,核心内容涵盖组学、检验、免疫、肿瘤、心血管、糖尿病等。如您有最新的研究内容发表,欢迎联系我们进行免费报道(公众号菜单栏-在线客服联系),我们的理念:内容创造价值,转化铸就未来!
转化医学网(360zhyx.com)发布的文章旨在介绍前沿医学研究进展,不能作为治疗方案使用;如需获得健康指导,请至正规医院就诊。
 腾讯登录
腾讯登录









还没有人评论,赶快抢个沙发