【Cell子刊】北京大学邓宏魁团队成功研发双属性iTNK细胞,为癌症免疫治疗带来新希望!
| 导读 | 这项研究为癌症免疫治疗提供了一种理想的效应细胞类型,并建立了它们从hPSC衍生的策略。 |
2024年8月30日, 北京大学生命科学学院邓宏魁团队在期刊《Cell Reports Methods》上发表了题为“Generation of dual-attribute iTNK cells from hPSCs for cancer immunotherapy”的研究论文。在这项研究中,团队从hPSC生成双属性诱导的T-NK(iTNK)细胞,表达细胞毒性T和NK细胞的标志物。单细胞RNA和T细胞受体(TCR)测序分析显示,iTNK细胞表达与NK和T细胞相关的特征基因,并表现出多样化的TCR库。iTNK细胞释放细胞毒性介质,对多种肿瘤细胞系发挥细胞毒性,并在体内抑制肿瘤生长。通过利用适应性和先天免疫反应,hPSC衍生的iTNK细胞,为癌症免疫治疗,提供了有前途的策略。

https://www.cell.com/cell-reports-methods/fulltext/S2667-2375(24)00216-9
研究背景
01
双属性免疫细胞结合了细胞毒性T细胞和自然杀伤(NK)细胞的优势,为免疫疗法提供了一种有吸引力的途径。不变的自然杀伤T(iNKT)细胞,具有独特的识别特性,通过多种机制的溶细胞特性显示出前景,但可用性有限。人体血液中含有极少量的iNKT细胞,在许多癌症患者中,它们的数量和功能减少,这限制了它们在癌症治疗中的潜在临床应用。为了克服这一限制,体外扩增的iNKT细胞,来自iNKT细胞来源的诱导多能干细胞(iPSC)的再分化iNKT细胞和造血干细胞工程iNKT细胞已经产生,并显示出癌症治疗的潜力。
以前的研究通过在体外对原代T淋巴细胞进行基因编辑或培养,来产生双属性免疫细胞。Bcl11b的基因缺失将T细胞重编程为诱导的T到NK(ITNK)细胞,这些细胞表现出NK细胞特性,并降低一些T细胞特征基因的表达。人ITNK细胞也可以通过使脐带血或外周血T细胞中的BCL11B失活来产生。这些细胞表现出先天性和适应性特征,显示出不依赖T细胞受体(TCR)的抗肿瘤细胞毒性。涉及自体ITNK细胞的临床研究,显示出有希望的结果,患者经历了肿瘤稳定和部分缓解。此外,细胞因子诱导的杀伤(CIK)细胞,包括CD3CD56细胞,在癌症治疗结果方面表现出一些改善。迄今为止的证据表明,双属性细胞在肿瘤免疫治疗中,具有相当大的潜在用途。
然而,获得足够的双属性细胞以进行广泛的临床使用,仍然是一个挑战。人类多能干细胞(hPSC),例如,胚胎干细胞(ESC)、23iPSCs和化学诱导的多能干细胞(CiPSC),为产生丰富的功能细胞,提供理想的细胞来源。然而,科学界尚未实现从hPSC生产用于临床应用的双属性细胞。
为了解决这一限制,这项研究介绍了一种从hPSC生产双属性诱导的T-NK(iTNK)细胞的方法。产生并富集造血祖细胞(HPC),以诱导T细胞谱系的产生;随后,成功生成了iTNK细胞。这些细胞同时表达CD8 T细胞和NK细胞特征基因,表现出多样化的TCR库,并在刺激和杀伤过程中,释放高水平的各种细胞毒性介质。iTNK细胞通过来自CD3-TCR复合物和NK受体的信号传导,对各种肿瘤细胞系,表现出有效的细胞毒性。此外,低剂量的iTNK细胞有效地抑制了体内肿瘤生长。研究结果表明,使用一种有前途的杀伤细胞类型,开发增强型癌症免疫疗法的潜力。
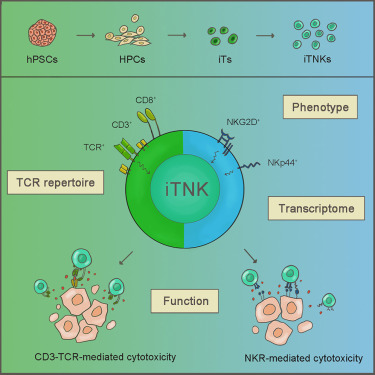
图形摘要
研究进展
02
在3D和2D系统中将hPSC分化为HPC
淋巴样细胞来源于造血干细胞/祖细胞,因此,需要诱导HPC作为初步步骤。通过优化团队之前的协议,团队成功地建立了一个化学定义的方案,用于3D和2D系统中序贯中胚层诱导和造血诱导。这是使用人CiPSC(hCiPSC)系CiPS-3、hESC系H1和hiPSC系iPS-7实现的。在3D系统中,hPSCs发生自聚集,形成胚胎体。经过10天的诱导期后,团队获得了CD34 HPC,由大约2/3的CD31CD43CD45细胞和1/3的CD31CD43组成CD45系列细胞。在2D系统中,hPSC接种在玻连蛋白包被的平板上,并以2D形态分化。经过12天的诱导期后,产生的CD34HPC主要是CD31CD43CD45细胞。CD34 HPC在3D和2D系统中的平均纯度,约为24%和30%。就产量而言,100万个hPSC在3D系统中产生了大约45万个CD34HPC,而它们在2D系统中产生了316万个CD34 HPC。在两个系统中,所有3种细胞系,都可以分化为HPC。
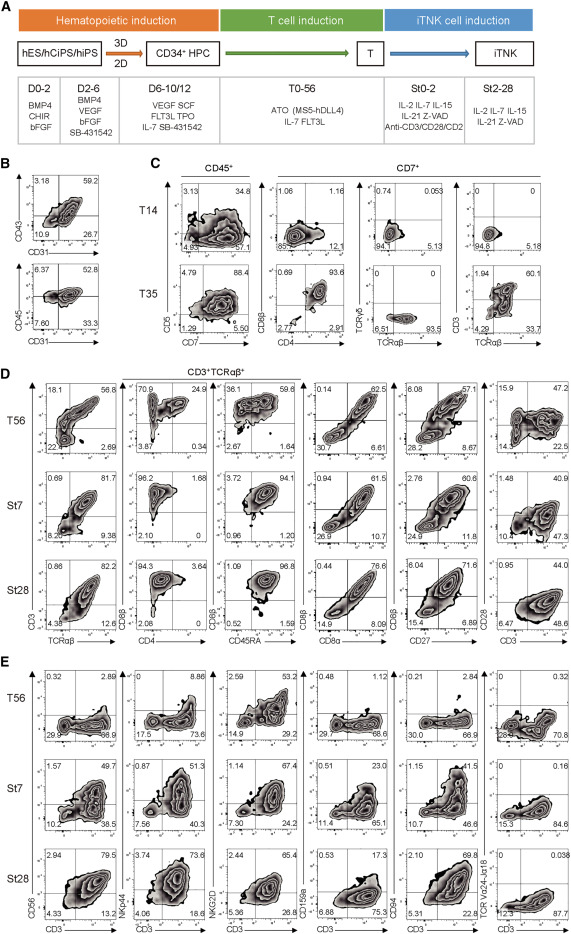
从hPSC生成iTNK细胞
iTNK细胞对肿瘤细胞具有强效的细胞毒性
团队构建了异位表达OKT3的OKT3 NALM-6细胞,用于CD3-TCR复合物刺激,iTNK细胞有效裂解OKT3 NALM-6细胞,但表现出对NALM-6细胞的有限裂解,表明iTNK细胞可以通过OKT3刺激,实现细胞毒性。iTNK细胞还对实体瘤细胞系表现出有效的细胞毒性,包括HCT116、HepG2、A375和MDA-MB-231。与NK细胞类似,iTNK细胞可以在4小时内实现肿瘤细胞杀伤,并在12小时内表现出更高的效率。NKp30的抑制,降低了iTNK细胞对A375细胞的杀伤效率。因此,iTNK细胞通过CD3-TCR复合物介导和NK受体介导的肿瘤细胞杀伤细胞毒性,表现出双重靶向。
在与HCT116肿瘤细胞共培养时,与NK细胞相比,iTNK细胞释放更高水平的IFN-γ、颗粒酶A、颗粒酶B、穿孔素、IL-17A、颗粒溶血素、IL-2和IL-10。在与NALM-6-OKT3肿瘤细胞共培养时,iTNK细胞表现出比T细胞更高水平的颗粒酶A、颗粒酶B、穿孔素、IL-17A、颗粒溶血素、IL-10和sFasL。此外,T细胞中IFN-γ的释放水平较高。这些结果表明,iTNK细胞在肿瘤杀伤过程中,表现出更大的多样性和更高水平的细胞毒性介质。
iTNK细胞在3周内显著抑制HCT116结直肠癌异种移植模型中的肿瘤生长,而不会对小鼠体重或外观造成不利影响。在iTNK细胞注射后3天,检测到小鼠血液中穿孔素、颗粒溶血和IFN-γ的释放。观察到iTNK细胞浸润到肿瘤、肝脏、肺和脾脏中。这些结果表明iTNK细胞的体内功能。
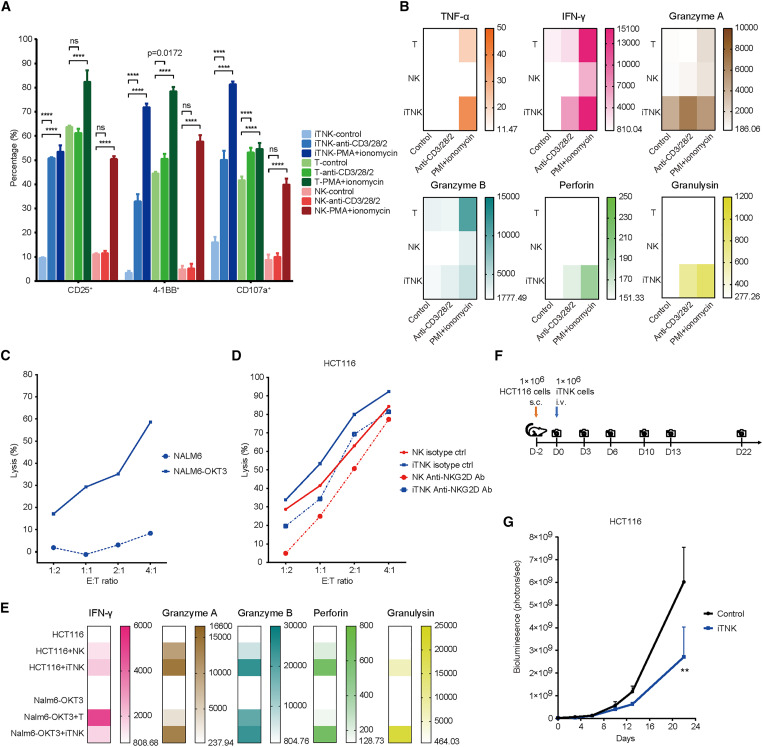
iTNK细胞的活化和细胞毒性
研究结论
03
这项研究成功地展示了iTNK细胞强大的肿瘤杀伤能力,并为它们从hPSC衍生,建立了稳健的方法。iTNK细胞用于肿瘤免疫治疗的潜力是巨大的。鉴于iTNK细胞表现出的细胞毒性T细胞和NK细胞的双重属性和组合功能,本研究为开发以iTNK细胞为中心的创新免疫治疗策略,铺平了道路。
参考资料:
1.Brennan, P.J. ∙ Brigl, M. ∙ Brenner, M.B.
Invariant natural killer T cells: an innate activation scheme linked to diverse effector functions
Nat. Rev. Immunol. 2013; 13:101-117
2.Shissler, S.C. ∙ Webb, T.J.
The ins and outs of type I iNKT cell development
Mol. Immunol. 2019; 105:116-130
 腾讯登录
腾讯登录









还没有人评论,赶快抢个沙发