【Nature子刊】 浙江省人民医院葛明华团队揭示蛋白质合成和甲状腺未分化癌进展的机制
| 导读 | 团队的研究表明,着丝粒蛋白NUF2在蛋白质合成中,起着至关重要的作用,并推动了ATC的进展。甲状腺癌患者的预后,与NUF2高表达呈正相关。 |
2024年9月6日,杭州医学院附属浙江省人民医院葛明华团队在期刊《Cell Death & Disease》上发表了题为“Maintenance of magnesium homeostasis by NUF2 promotes protein synthesis and anaplastic thyroid cancer progression”的研究论文。研究结果表明,NUF2通过维持细胞内Mg2+的稳态,作为蛋白质合成的新兴调节因子发挥作用,最终推动ATC进展。

https://www.nature.com/articles/s41419-024-07041-6
研究介绍
01
甲状腺癌(TC)是最常见的内分泌相关癌症,占所有内分泌恶性肿瘤的90%以上。甲状腺未分化癌(ATC)是TC的致命亚型,中位生存期仅为6个月,占TC相关死亡总数的40-50%。与其他常见的TC亚型不同,ATC生长迅速,导致呼吸困难、发音困难和吞咽困难等颈部压迫症状。
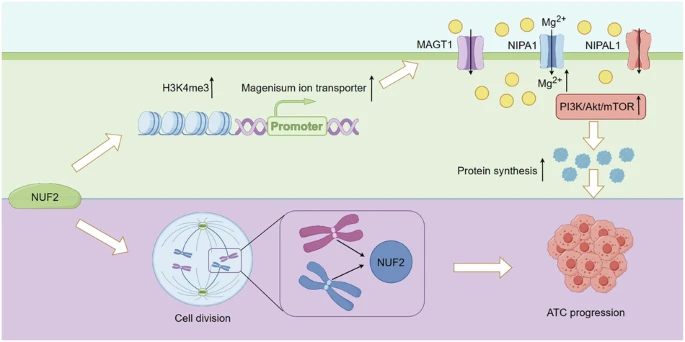
蛋白质合成失调,已被证明是癌症的主要特征之一。为了满足肿瘤微环境中的内部致癌需求和外部因素,癌细胞快速、选择性地合成蛋白质 。镁离子对肿瘤增殖和发展,是必不可少的 ,低镁血症会抑制肿瘤生长和血管生成。研究表明,MAGT1的表达影响癌症的进展 ,NIPA1和NIPAL1与不良预后相关。癌细胞优先翻译致癌蛋白,从而促进肿瘤生长、转移和治疗耐药。在ATC中,蛋白质合成,也受到真核起始因子4E(eIF4E)和核糖体生物发生途径增加的支持,从而增强其侵袭性和化疗耐药性。
作为NDC80着丝粒复合物的组成部分,已知NUF2在有丝分裂染色体排列和建立稳定的着丝粒-微管附着中,发挥作用。NUF2的耗竭,显著阻断了具有活性纺锤体检查点的前中期。NUF2在多种癌症中上调,被认为是一种有前途的抗肿瘤治疗靶点和预后因素。几项研究指出,NUF2在着丝粒蛋白之外,起致癌调节剂的作用。例如,NUF2被确定为一种新的癌症干细胞指标。此外,已发现NUF2通过抑制癌基因TFR1的自噬降解或影响HMGA2的转录,来驱动癌症的发展。研究表明,NUF2不仅通过干扰着丝粒功能来影响G2/M期 ,而且还作用于发生蛋白质合成的S期 。
在这项研究中,团队研究了NUF2在ATC中的作用和机制。团队发现NUF2表观遗传,调控镁转运蛋白的转录,从而通过ATC中的PI3K/Akt/mTOR通路,促进蛋白质合成。研究结果扩展了NUF2在蛋白质合成和ATC进展过程中,作为镁稳态的新兴调节因子的概念。
研究进展
02
NUF2促进ATC肿瘤体内生长和转移
在斑马鱼-CDX模型中,NUF2敲低组ATC异种移植物的荧光大小,在3天后显著降低。8505C和KHM-5M的荧光大小与对照相比,分别减少了2.6倍和10.2倍。小鼠肿瘤组织的IHC染色证实,NUF2敲低降低了增殖核标志物Ki67的表达。此外,团队在裸鼠中建立了原位ATC肿瘤模型,发现NUF2敲低的作用,显著抑制了肿瘤生长;表明NUF2敲低,显著降低了ATC细胞的转移能力。这些结果表明,NUF2在体内促进ATC的进展和转移。
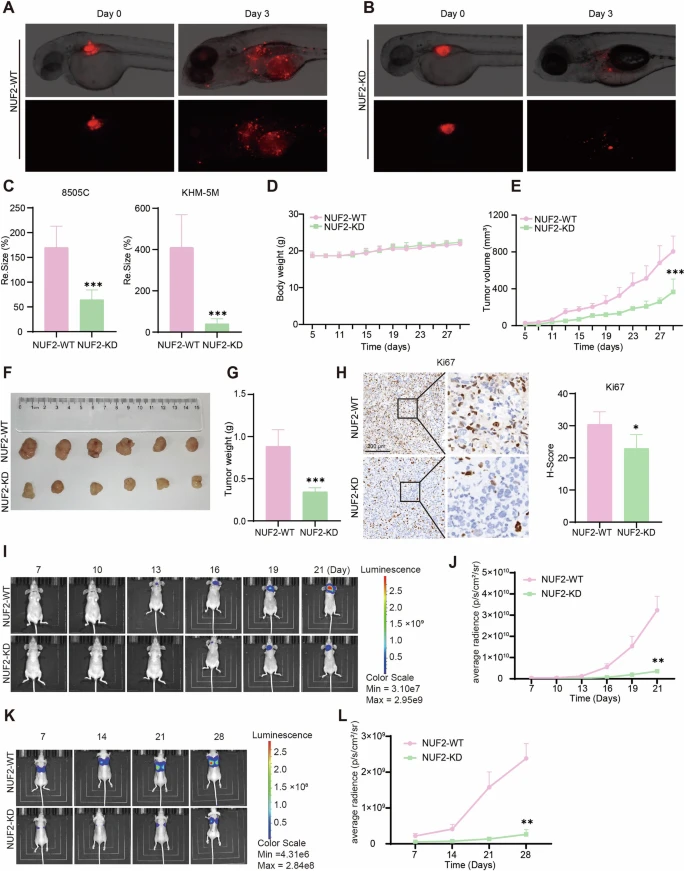
NUF2在体内促进ATC肿瘤生长和转移。
NUF2介导的镁稳态影响蛋白质合成效率
PI3K/Akt/mTOR通路参与了蛋白质合成,Mg2+可以调节PI3K/Akt/mTOR通路的激活。Spearman相关分析表明,ATC样本中NUF2的表达水平,与mTOR信号转导呈正相关。与NUF2-WT组相比,NUF2-KD小鼠异种移植组织中,p-mTOR的表达水平较低。mTOR抑制,可以部分减弱NUF2过表达诱导的蛋白质合成增加。NUF2或MNN的敲除,抑制了ATC细胞中PI3K/Akt/mTOR的磷酸化。此外,团队证明了MNN对NUF2诱导的PI3K/Akt/mTOR通路上调的挽救作用。NUF2过表达对PI3K/Akt/mTOR通路的促进作用,可以部分被MNN敲低逆转。研究结果表明,NUF2介导的镁稳态,影响了PI3K/Akt/mTOR通路,进而影响了蛋白质合成的效率。
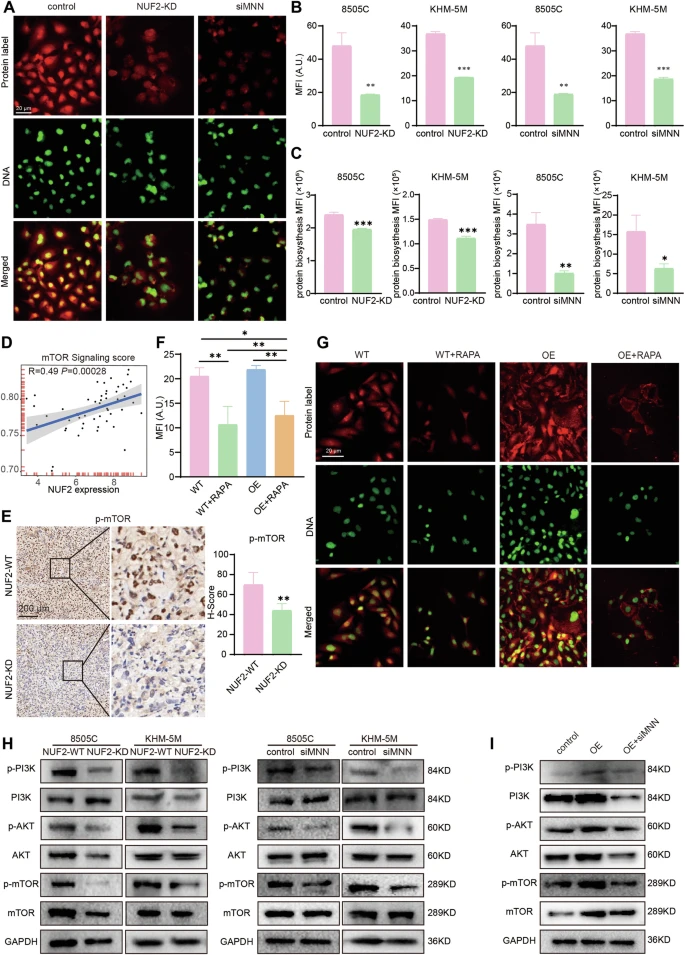
NUF2介导的镁稳态,影响了PI3K/Akt/mTOR通路的蛋白质合成效率。
研究结论
03
在这项研究中,8505C细胞系的NUF2表达水平,高于KHM-5M。与8505C细胞系相比,在KHM-5M细胞系中敲低NUF2,更显著地抑制细胞增殖并诱导细胞凋亡。在斑马鱼的CDX模型中,NUF2的敲低,导致KHM-5M细胞比8505C细胞更显著的肿瘤抑制。
敲低NUF2或镁转运蛋白,显著抑制了PI3K/Akt/mTOR信号传导和蛋白质合成效率。
总之,团队的研究表明,NUF2表观遗传学促进镁转运蛋白的转录,并促进Mg2+通过激活PI3K/Akt/mTOR通路,从而驱动ATC的恶性表型,从而产生依赖性蛋白质合成。
参考资料:
1.Siegel RL, Miller KD, Jemal A. Cancer Statistics, 2017. CA Cancer J Clin. 2017;67:7–30.
2.Saini S, Tulla K, Maker AV, Burman KD, Prabhakar BS. Therapeutic advances in anaplastic thyroid cancer: a current perspective. Mol Cancer. 2018;17:154.
 腾讯登录
腾讯登录









还没有人评论,赶快抢个沙发