有效抑制肿瘤生长!四川大学敖强教授团队发文:开发出新型肿瘤疫苗纳米佐剂
| 导读 | 由于Toll样-9激动剂(CpG)不足以激活抗肿瘤免疫反应,因此其作为肿瘤免疫治疗的佐剂的效果受到限制。 |
9月11日,四川大学敖强教授研究团队在期刊《Advanced Science》上发表了题为“A Multi-Functional Nanoadjuvant Coupling Manganese with Toll-Like 9 Agonist Stimulates Potent Innate and Adaptive Anti-Tumor Immunity”的研究论文,本研究中,研究人员研究了常见的营养金属离子(Mn2+、Cu2+、Ca2+、Mg2+、Zn2+、Fe3+和Al3+),发现Mn2+是增强CpG的关键因子,可通过增强STING-NF-κB通路来介导免疫激活。然后将Mn2+和CpG与EGCG自组装成纳米佐剂MPN/CpG。在B16黑色素瘤小鼠模型中,局部递送MPN/CpG有效抑制肿瘤生长。通过重新极化M2型肿瘤相关巨噬细胞(TAMs)为M1型并增强肿瘤内CD8+/CD4+ T淋巴细胞和DC的浸润,重塑了肿瘤微环境(TME)。此外,与游离CpG相比,MPN/CpG在淋巴结中的积聚程度更高,增强了CpG的摄取和DC的激活,从而诱导出显著的特异性细胞毒性CD8+ T细胞免疫反应和体液免疫。在预防性肿瘤小鼠模型中,研究人员用OVA抗原对MPN/CpG进行免疫接种显著延缓了B16-OVA黑色素瘤的生长并延长了小鼠的生存时间。这些发现强调了MPN/CpG作为一种多功能佐剂平台的潜力,可驱动强大的固有免疫和适应性免疫,并调节TME以对抗肿瘤。

https://onlinelibrary.wiley.com/doi/full/10.1002/advs.202402678
背景知识
01
癌症免疫疗法通过激活人体免疫系统来抑制肿瘤的生长和转移,是癌症治疗中最有效的方法之一。特别是肿瘤疫苗具有诱导肿瘤特异性和长期记忆免疫反应的能力,从而抑制肿瘤生长、转移和复发。然而,抗原呈递细胞(APCs)有限的免疫刺激显著限制了肿瘤疫苗的抗肿瘤效果。此外,免疫抑制的肿瘤微环境进一步阻碍了其有效性。肿瘤微环境是一个有利于肿瘤形成的复杂系统,由间质细胞、成纤维细胞、内皮细胞、固有免疫细胞和适应性免疫细胞组成。肿瘤相关巨噬细胞(TAMs)、髓源性抑制细胞(MDSCs)和调节性T细胞(Treg)是主要的抑制性免疫细胞,其中TAMs是最丰富的,占肿瘤组织的50%以上。肿瘤微环境中的TAMs大多属于M2型,能够表达高水平的免疫检查点配体或招募调节性T细胞来抑制CD8+T细胞活性。因此,越来越多的癌症疫苗正在采用免疫佐剂来解决这一缺陷。佐剂最早于1926年被发现,并于1932年获准用于白喉疫苗。自那时以来,越来越多的佐剂被开发并推向市场。最近,佐剂开发的重点转向了天然免疫系统受体的激动剂,尤其是Toll样受体(TLR)激动剂。这些免疫佐剂可以刺激固有免疫细胞的成熟,增强抗原呈递,并通过激活模式识别受体(PRR)信号通路激活T细胞。具有这些免疫增强作用的佐剂对于提高癌症疫苗的效力至关重要。
MPN/CpG在治疗性小鼠模型中抑制肿瘤生长
02
为了评估MPN/CpG的治疗效果,按照图1A所示的时间表,小鼠皮下接种B16黑色素瘤,随后在瘤内注射MPN/CpG, MPN, CpG。研究人员观察了小鼠体重和肿瘤生长情况。实验期间,所有处理组小鼠体重无明显变化,主要器官H&E染色未显示明显损伤,表明所有处理均未诱导明显毒性。MPN/CpG处理对肿瘤生长有明显的抑制作用,而MPN处理仅表现为中度抑制作用,CpG处理对肿瘤生长无明显影响。令人惊讶的是,MPN/CpG中Mn2+浓度的增加与低浓度相比表现出相似的肿瘤抑制作用。分离肿瘤后,MPN/CpG(低)和MPN/CpG(高)治疗组的平均肿瘤重量仅为PBS治疗组的1 / 3,表明MPN/CpG能有效控制肿瘤生长。随后对肿瘤染色的组织学分析显示,在MPN/CpG(低)和MPN/CpG(高)处理组中,H&E染色显示细胞核密度和细胞核染色均显著减少。TUNEL染色观察到亮绿色荧光,进一步证实了对肿瘤细胞的有效抑制。与MPN/CpG相比,游离Mn2+ + CpG抑制肿瘤生长的效果较差。流式细胞术检测结果显示,MPN/CpG处理组小鼠外周血中颗粒酶B阳性CD8+ T细胞和CD8+ T细胞水平明显高于Mn2+ + CpG处理组。提示MPN/CpG局部递送比Mn2+ + CpG混合液能更有效地激活机体免疫。
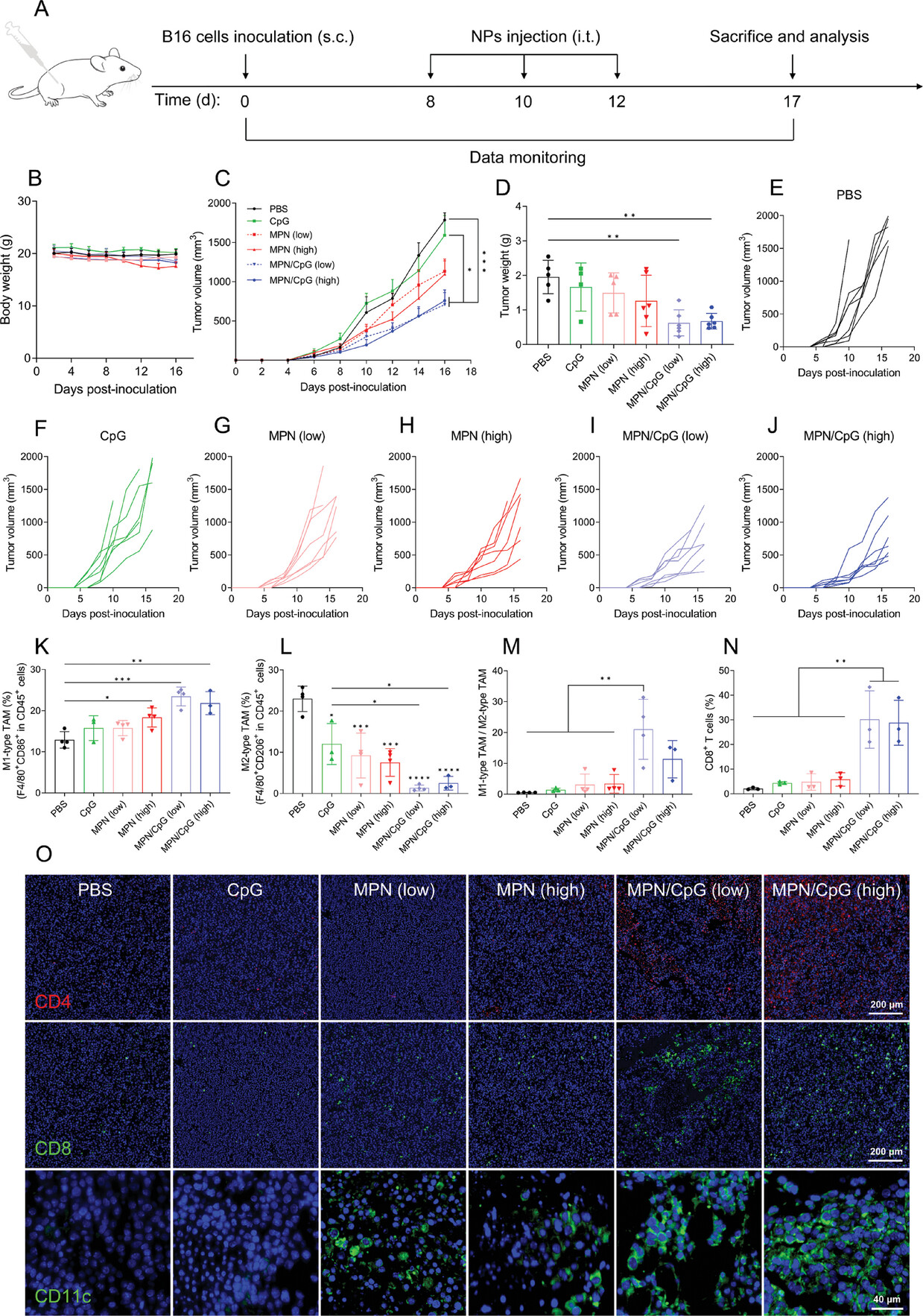
图1:局部注射MPN/CpG可抑制肿瘤生长,重塑肿瘤免疫环境
研究人员通过流式细胞术检测巨噬细胞、T细胞和DCs的数量,探索肿瘤内的免疫微环境。MPN/CpG可上调F4/80+巨噬细胞表面CD86的表达,下调CD206的表达,从而显著提高CD86+/CD206+比值。结果表明,MPN/CpG处理可以将肿瘤相关巨噬细胞的免疫抑制型M2重新编程为免疫刺激型M1。在MPN/CpG(低)和MPN/CpG(高)处理组中,肿瘤微环境中M1型TAMs的百分比分别上升至23.45%和21.83%,而M2型TAMs的百分比下降至1.35%和2.5%。M1/M2比值也明显升高,分别为PBS组的37.3倍和20.2倍。此外,MPN/CpG(低)和MPN/CpG(高)治疗组的肿瘤浸润CD8 T细胞数量显著高于其他治疗组,分别达到30.2%和28.9%。肿瘤组织切片免疫荧光染色进一步证实了这一结果,浸润的CD4、CD8 T细胞和DCs的荧光强度较PBS组明显增强。综上所述,这些结果表明MPN/CpG具有强大的肿瘤治疗作用,并能重塑肿瘤微环境,使“冷”肿瘤转变为“热”肿瘤。
研究小结
03
综上所述,本研究证明了Mn2+作为免疫调节剂的潜力及其与CpG的协同作用。通过与EGCG的成功配合,研究人员开发了一种双佐剂纳米平台,MPN/CpG。该纳米佐剂通过激活STING/TLR9-NF-κB通路在体内外表现出强大的协同作用。与游离佐剂相比,MPN/CpG纳米佐剂更容易被树突状细胞摄取并在淋巴结内聚集。瘤内注射可显著改善免疫抑制性肿瘤微环境,诱导M2型肿瘤相关巨噬细胞向M1型复极化,增强T细胞和树突状细胞在肿瘤中的浸润。MPN/CpG作为肿瘤疫苗佐剂,可诱导强效的特异性T细胞免疫应答,有效抑制肿瘤生长。因此,研究人员利用多酚将金属离子与TLR激动剂结合的策略为金属免疫治疗提供了一个有前景的途径。(转化医学网360zhyx.com)
【参考资料】
https://onlinelibrary.wiley.com/doi/full/10.1002/advs.202402678
【关于投稿】
转化医学网(360zhyx.com)是转化医学核心门户,旨在推动基础研究、临床诊疗和产业的发展,核心内容涵盖组学、检验、免疫、肿瘤、心血管、糖尿病等。如您有最新的研究内容发表,欢迎联系我们进行免费报道(公众号菜单栏-在线客服联系),我们的理念:内容创造价值,转化铸就未来!
转化医学网(360zhyx.com)发布的文章旨在介绍前沿医学研究进展,不能作为治疗方案使用;如需获得健康指导,请至正规医院就诊。
 腾讯登录
腾讯登录


还没有人评论,赶快抢个沙发