2024 WCLC 口头报告 | 臻和科技cfDNA甲基化检测平台助力可切除非小细胞肺癌患者接受新辅助化免治疗疗效评估
| 导读 | 特瑞普利单抗联合化疗用于可切除IIB-IIIB期非小细胞肺癌新辅助治疗疗效及生物标志物分析。 |
该研究不仅证实了新辅助化免治疗的有效性及安全性,还采用臻和科技提供的全甲基化(Whole methylome sequencing,WMS)和靶向甲基化panel(Targeted Methylation)联合测序平台,首次深入探讨了细胞游离DNA(cfDNA)甲基化特征以及染色体非整倍体特征片段在疗效预测及动态评估中的重要价值,为新辅助化免治疗疗效预测及疗效动态监测提供了新思路。

背景
新辅助化疗联合免疫治疗在可切除的NSCLC患者中展现了良好的疗效,但并非所有患者都能从中受益,因此亟需找到可靠的生物标志物,以便准确预测和监测其疗效。本研究拟验证新辅助化免疗法的有效性,并探讨cfDNA特征在疗效评估中的作用。
研究方法
本研究共招募了100名IIB至IIIB期NSCLC患者,接受至少两周期的新辅助特瑞普利单抗联合铂类化疗。我们对其中60名患者的195份血浆cfDNA样本进行了WMS和甲基化panel双平台测序,并分别计算甲基化片段比(MFR)和染色体非整倍体特征片段(CAFF)得分。在每个治疗周期前(C0、C1)及术前(BS)采集样本,评估MFR和CAFF动态变化与病理评效的相关性。
研究结果
1.治疗的安全性和疗效
95.0%的患者出现了不同程度的治疗相关不良反应,其中35%为3级或4级;83.0%的患者最终接受了R0根治性切除,手术并发症的发生率为25.3%;
65.1%的患者达到了主要病理反应(MPR),45.8%达到了病理完全缓解(pCR);
2.基线临床信息和病理评效的相关性
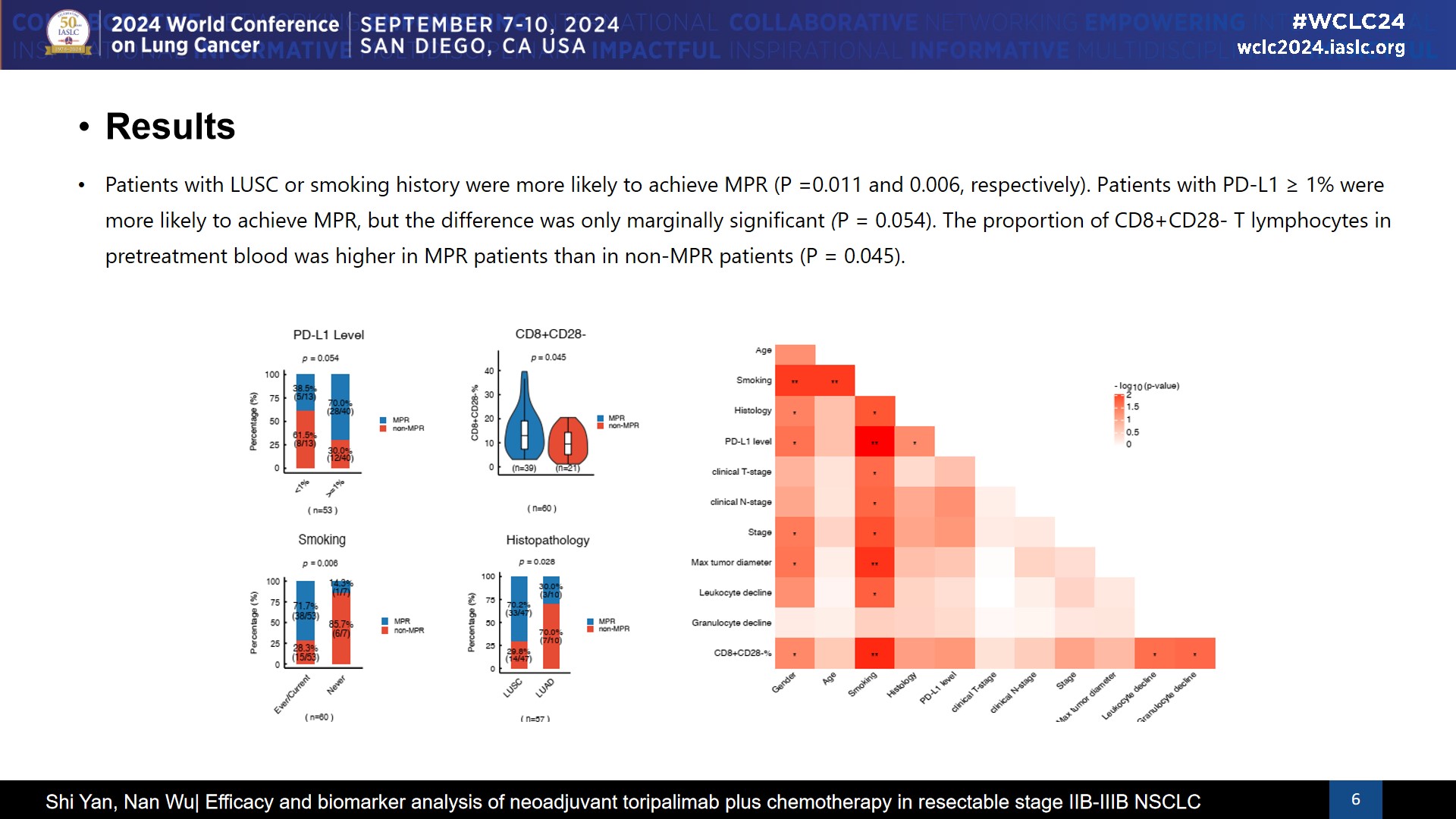
合并吸烟史及鳞状细胞癌(LUSC)患者更可能达到MPR。PD-L1表达≥1%的患者更有可能达到MPR(p = 0.054)。
在治疗前血液中,MPR患者的CD8+CD28- T淋巴细胞比例高于非MPR患者(p = 0.045)。
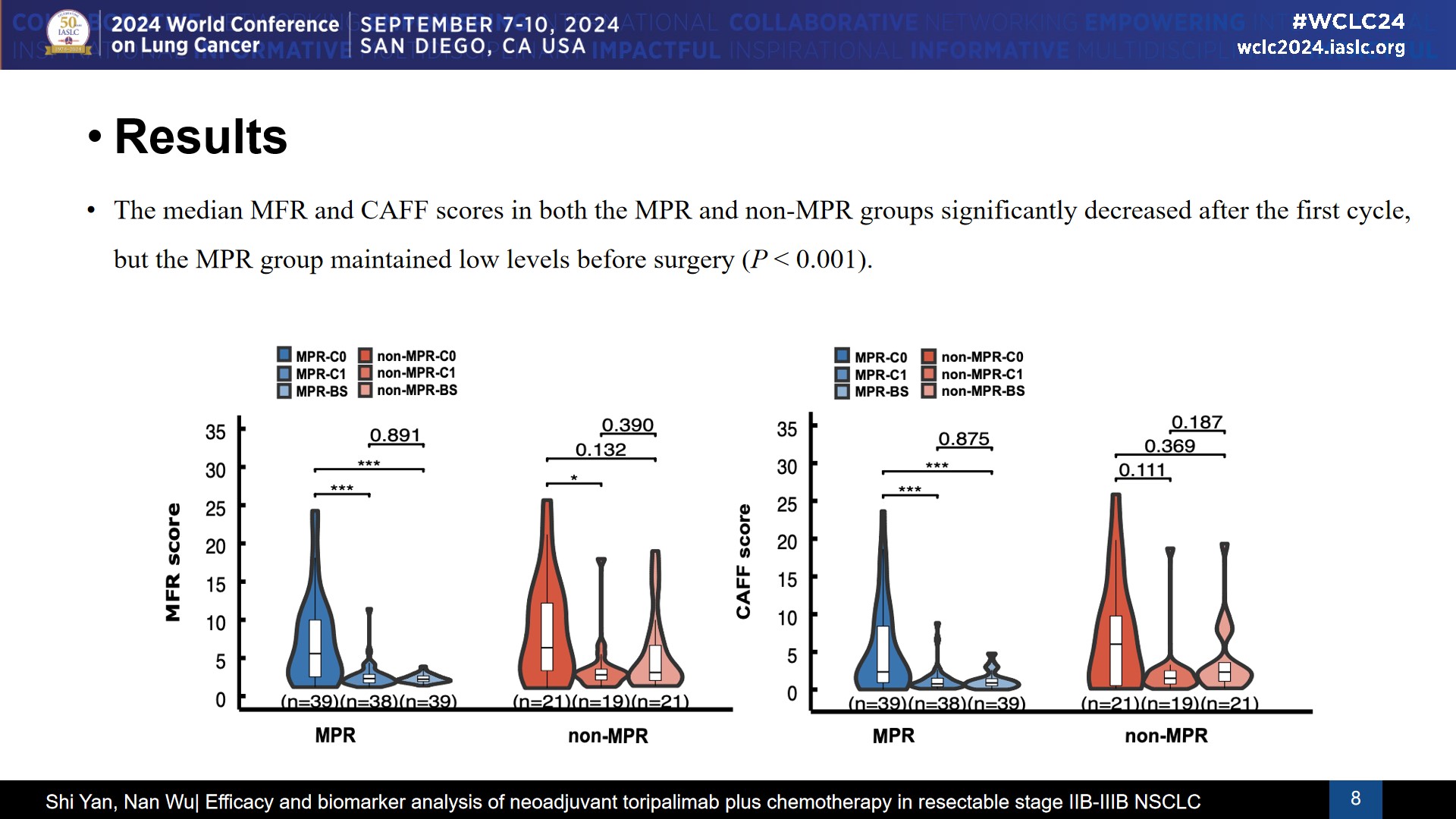
3.cfDNA的动态变化和病理评效的相关性
cfDNA分析表明,MFR和CAFF在治疗前后的变化与患者的病理评效有显著关联(p < 0.001)。MFR和CAFF得分在治疗第一周期后显著降低,且MPR患者在术前能维持低水平的MFR和CAFF。
在术前MFR低的患者更可能达到MPR(74.5% vs. 11.1%,p < 0.001),在C1时CAFF低(73.9% vs. 36.4%,p = 0.031)或术前CAFF低的患者也更容易达到MPR(76.2% vs. 38.9%,p = 0.008)。

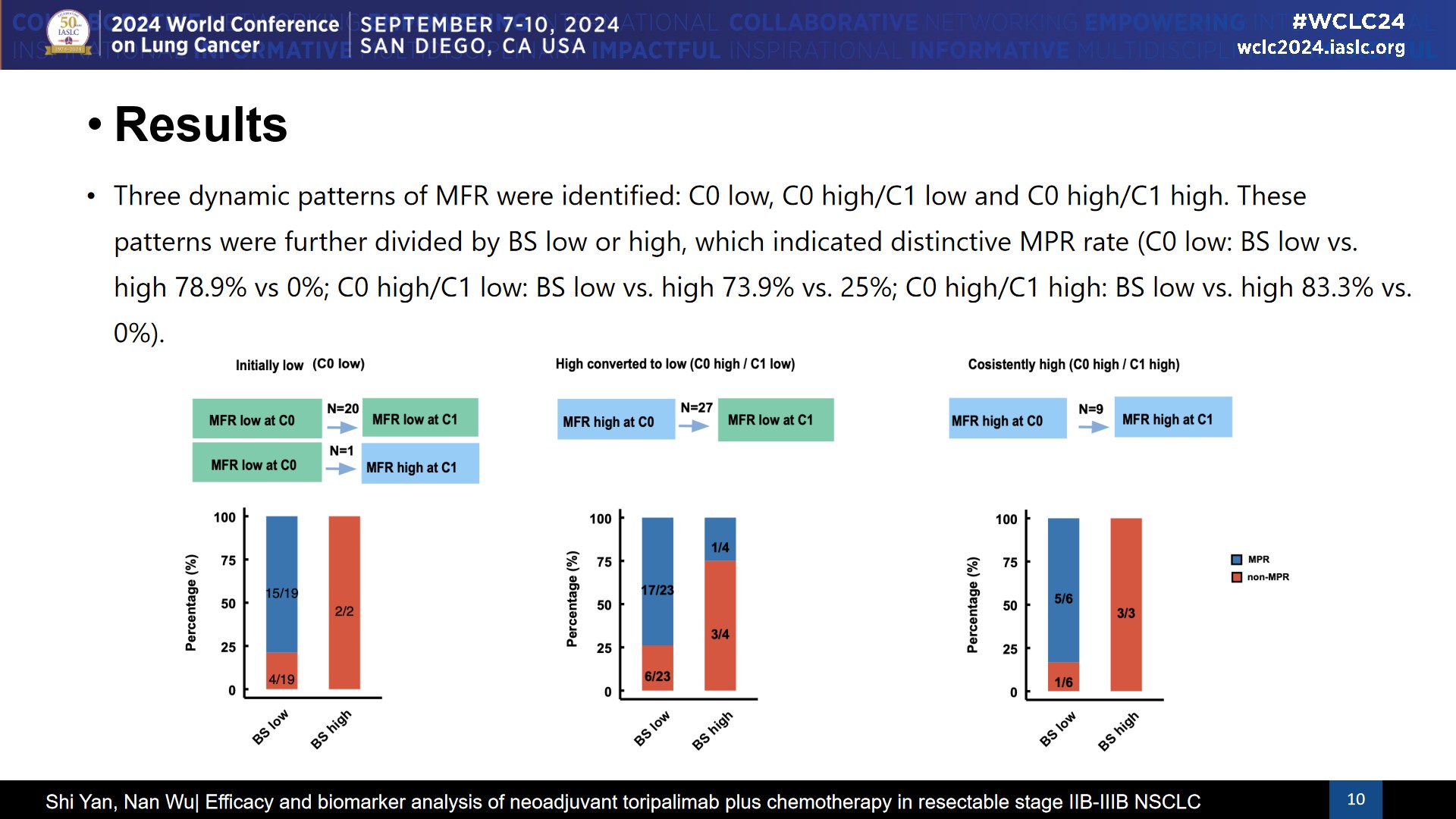
MFR呈现三种动态模式:C0低、C0高/C1低和C0高/C1高,并根据术前BS得分进一步分为低或高,这些模式对应不同的MPR率
① C0低:BS低 vs. 高 78.9% vs 0%;② C0高/C1低:BS低 vs. 高 73.9% vs. 25%;
③ C0高/C1高:BS低 vs. 高 83.3% vs. 0%。
CAFF也有类似的三种动态模式:C0低、C0高/C1低和C0高/C1高,同样根据BS低或高分为不同的MPR率
① C0低:BS低 vs. 高 72.8% vs. 50.0%;② C0高/C1低:BS低 vs. 高 86.7% vs. 50.0%;
③ C0高/C1高:BS低 vs. 高 100.0% vs. 0%。

4.建立cfDNA和临床参数的综合评效模型
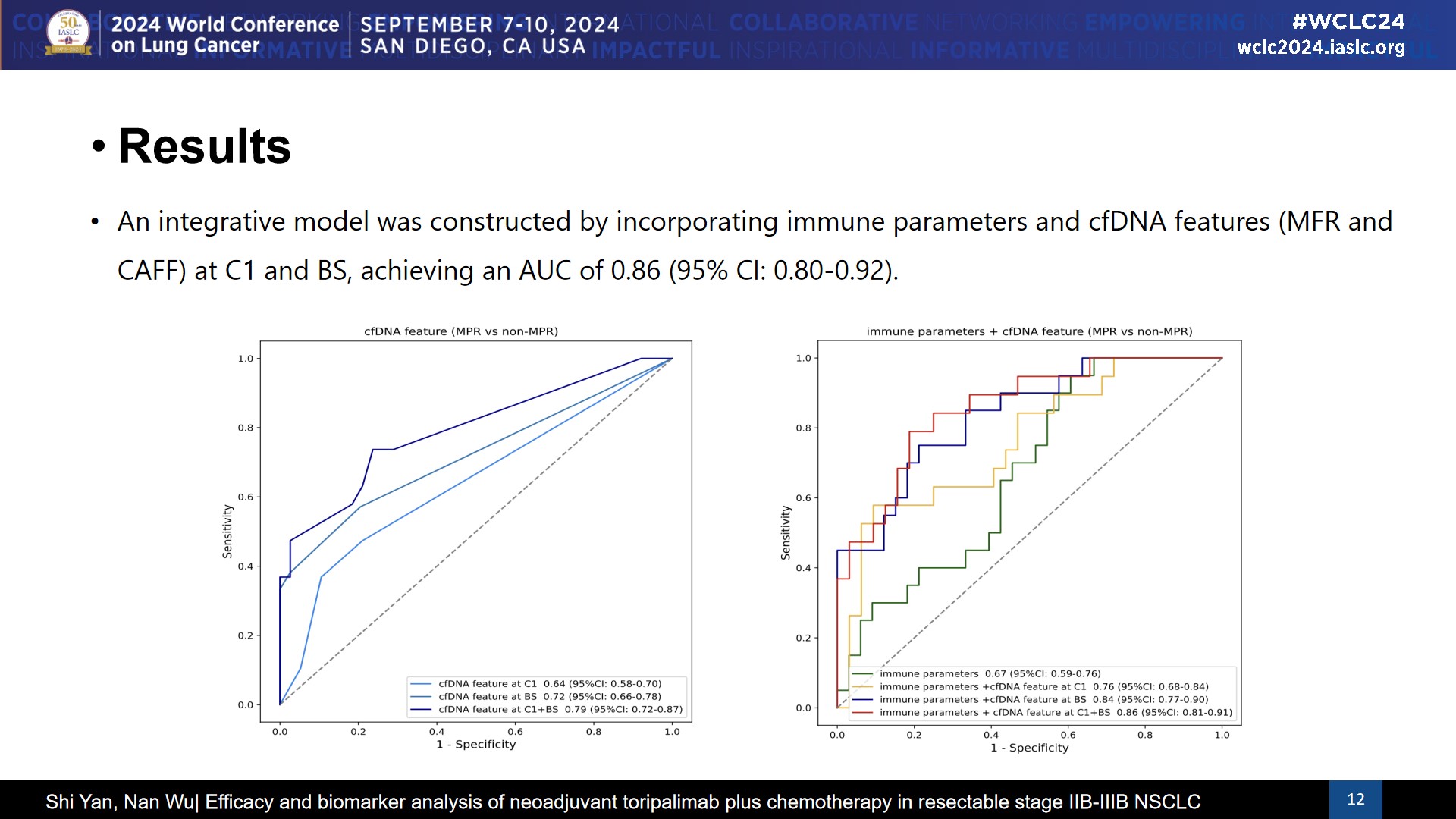
通过整合C1和BS时间点的免疫参数和cfDNA特征(MFR和CAFF),构建了一个综合模型,对MPR的预测效能(AUC)达到0.86(95% CI: 0.80-0.92),显著高于仅基于免疫参数的模型(AUC=0.67,95% CI: 0.59-0.76),也高于基于单个时间点的cfDNA特征模型。这些结果显示,动态监测cfDNA甲基化特征可以助力更好预测新辅助化免治疗的疗效。
研究小结
新辅助化免疗法在可切除IIB-IIIB期NSCLC患者中取得了理想的疗效。通过cfDNA甲基化特征的动态监测,我们可以准确地预测患者的病理评效,进而优化个体化治疗方案。这一发现为NSCLC新辅助治疗领域带来了新的希望和方向。
 腾讯登录
腾讯登录





还没有人评论,赶快抢个沙发