【Science子刊】华中科技大学陶娟团队:揭秘MerTK巨噬细胞在黑色素瘤中的双重作用
| 导读 | 在这项研究中,团队的单细胞RNA测序数据,确定了表达高水平吞噬细胞受体MER原癌基因酪氨酸激酶(MerTK巨噬细胞)的巨噬细胞亚群,这与黑色素瘤进展和免疫治疗耐药性密切相关。 |
2024年10月,华中科技大学同济医学院附属协和医院陶娟团队在期刊《Science Advances》上发表了题为“MerTK macrophages promote melanoma progression and immunotherapy resistance through AhR-ALKAL1 activation”的研究论文。研究结果阐明了MerTK巨噬细胞的调节机制,并为提高黑色素瘤免疫治疗的有效性提供了策略。

https://www.science.org/doi/10.1126/sciadv.ado8366
关于黑色素瘤
01
黑色素瘤是最常见的原发性皮肤恶性肿瘤,全世界的存活率很低。在过去10年中,癌症免疫疗法取得了重大突破。迄今为止,美国食品药品监督管理局已批准将细胞毒性T淋巴细胞抗原-4(CTLA-4)和程序性细胞死亡蛋白-1/配体1(PD-1/PD-L1)阻断疗法用于治疗各种恶性肿瘤。为了克服免疫治疗耐受性,肿瘤诱导的免疫抑制机制近年来一直是大量研究的重点,现在已经确定了TME中的多个抑制细胞群,肿瘤相关巨噬细胞(TAM)已成为恶性癌症免疫治疗的新兴靶标。
TAM是免疫抑制性TME中一个主要且异质性的不同免疫细胞亚群,在增强恶性肿瘤和抑制抗肿瘤免疫方面发挥重要作用。然而,巨噬细胞亚群的功能表型及其潜在机制,尚不完全清楚。
在这项研究中,使用单细胞分析,团队在黑色素瘤中鉴定了MER原癌基因酪氨酸激酶(MerTK)巨噬细胞的亚群,该亚群显示出强大的免疫抑制活性。研究结果表明,AhR-ALKAL1信号传导是MerTK巨噬细胞的关键调节因子,也是黑色素瘤免疫治疗的有前途的靶点。
MerTK巨噬细胞促进肿瘤生长
02
注射氯phosome脂质体后6天,TAM的数量减少。Clophosome脂质体对巨噬细胞的耗竭,如预期般成功地避免了肿瘤生长。无论巨噬细胞耗竭如何,将MerTK巨噬细胞过继转移到受体小鼠中,都恢复了小鼠的肿瘤生长,而MerTK++++++++−巨噬细胞不促进肿瘤生长。去除巨噬细胞后,进行MerTK巨噬细胞过继转移,导致肿瘤生长显著增加,甚至超过小鼠的正常水平。MerTK巨噬细胞过继转移组中,CD8 T细胞百分比降低,同时,IFN-γ和肿瘤坏死因子α阳性(TNF-α)CD4和CD8 T细胞的百分比降低,无论巨噬细胞清除率如何。在MerTK巨噬细胞过继转移组中,也观察到更高水平的免疫检查点PD-1表达。这些数据共同表明,MerTK巨噬细胞通过损害T细胞功能,来加剧肿瘤进展。
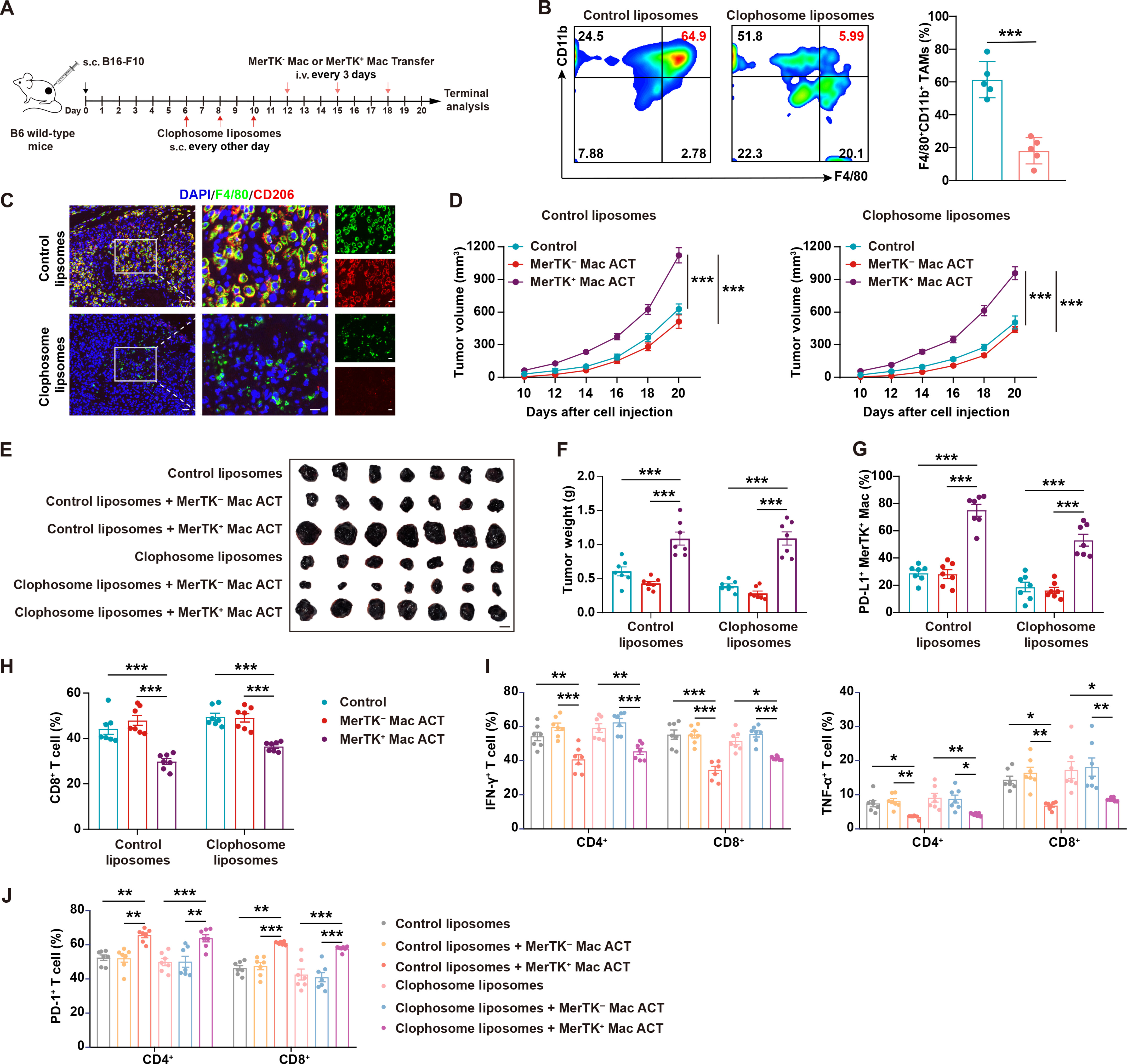
MerTK巨噬细胞促进肿瘤生长。
通过AhR抑制靶向TAM,可防止肿瘤生长并增强aPD-L1疗效
03
研究结果表明,AhR在调节MerTK介导的吞噬作用和免疫抑制巨噬细胞的极化中起关键作用,从而促进肿瘤进展。为了评估是否可以利用这些知识进行癌症免疫治疗,团队开发了一种纳米载体,用于递送AhR拮抗CH223191,使用甘露糖基化胶束(CH223191-MMic),通过CD206特异性靶向MerTK巨噬细胞。
团队表征了CH223191-MMic制剂,并确认其适用于生物医学应用。最初,胶束中CH223191的释放相对较快,由于胶束涂层的部分损伤,12小时后达到60%的累积释放。团队还证实了共孵育6小时后,巨噬细胞有效摄取Cy3标记的CH223191-MMic。即使在100μg/ml的高浓度下,CH223191-MMic也不会诱导显著的毒性,细胞活力在孵育24小时和48小时后,仍保持在90%以上。MMic早在注射后2小时,就在肿瘤部位有效积累和选择性靶向,在24小时达到峰值强度。在其他器官中观察到有限的荧光,包括心脏、肝脏、脾脏、肺和肾脏,表明MMic主要在肿瘤部位积累,此后逐渐代谢。CH223191-MMic的体内生物相容性评估显示肝肾功能正常,血清生化标志物在正常范围内,未观察到正常器官的病理变化。这些结果共同表明,使用CH223191-MMic作为潜在黑色素瘤疗法的安全性。
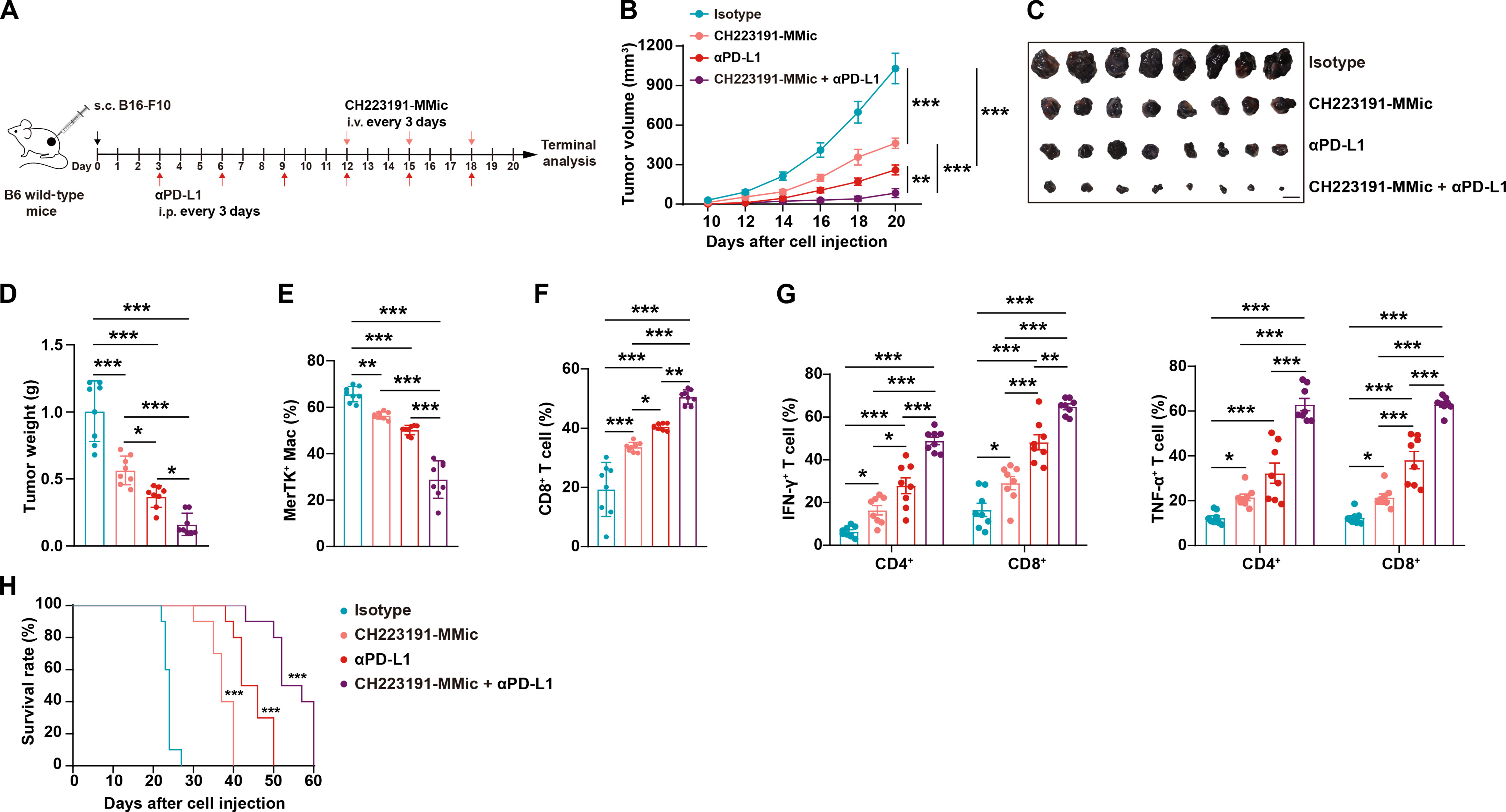
通过AhR抑制靶向TAM,可增强aPD-L1疗效。
结论
04
与许多新的治疗候选药物相比,MerTK的独特之处在于,由于其在肿瘤中的已知功能,它已经是一个既定的药物靶点。已经开发了小分子MerTK抑制剂,用于EGFR突变非小细胞肺癌与奥希替尼的联合治疗,在人体1期试验中显示出逆转奥希替尼耐药性的有效性 (ClinicalTrials.gov, NCT04762199)。此外,MerTK信号转导充当先天免疫检查点。
在这项研究中,团队阐明了MerTK作为TAM浸润TME中靶点的富集,强调了它在抗PD-1治疗失败后作为先天免疫抵抗机制的作用。研究结果为患者分层和选择针对MerTK、PD-1或PD-L1的联合疗法,提供了机制见解。
参考资料:
1.J.Y. Wang, E. B. Wang, S. M. Swetter, What is melanoma? JAMA 329, 948 (2023).
2.I. Mellman, G. Coukos, G. Dranoff, Cancer immunotherapy comes of age. Nature 480, 480–489 (2011).
 腾讯登录
腾讯登录









还没有人评论,赶快抢个沙发