【Nature子刊】北大深圳研究生院曹宇团队创新突破:分体设计CAR-T细胞,提升B细胞恶性肿瘤治疗效果!
| 导读 | 团队提出了一种分体CAR设计,包括在T细胞上表达的通用受体和基于配体的开关分子,这种设计保留了像APRIL和BAFF这样的配体的天然三聚体结构。
|
2024年11月11日, 北京大学深圳研究生院、深圳湾实验室曹宇团队在期刊《Nature Communications》上发表了题为“Split-design approach enhances the therapeutic efficacy of ligand-based CAR-T cells against multiple B-cell malignancies”的研究论文。研究结果表明,团队的CAR-T细胞策略在雌性小鼠中对各种B细胞恶性肿瘤模型显示出抗肿瘤活性,可能预防了传统CAR-T细胞疗法中因抗原丢失或转换而发生的免疫逃逸。这种基于配体的分体CAR设计引入了优化CAR识别的理念,增强了疗效,并有望在临床转化中提高安全性,可能广泛适用于基于天然受体或配体的细胞疗法。

https://www.nature.com/articles/s41467-024-54150-z
关于sCAR细胞策略
01
可切换的CAR-T(sCAR-T)细胞平台,包括在T细胞上表达的通用受体和肿瘤靶向适配分子。这个平台具有独特的分体CAR设计,有可能赋予目标配体强大的天然属性。通过扩展sCAR-T细胞策略,团队和其他团队已经探索了同时设计sCAR铰链和开关标记位点的灵活性,以实现CAR-T细胞激活的最佳距离和方向。sCAR-T细胞平台使CAR-T细胞模块化,为临床肿瘤治疗提供了增强的灵活性。此外,这种策略允许对sCAR-T细胞活性进行剂量可调控制,解决了与传统CAR-T细胞相关的安全问题。
在这项研究中,团队介绍了一种sCAR策略,用于配体介导的CAR-T细胞激活,其中设计的分裂APRIL或BAFF基开关保持它们的天然结构,从而对B细胞恶性肿瘤中的多个目标产生高度敏感的反应。团队的sCAR策略,显示出与FDA批准的治疗方法相当的治疗效果。
体外比较分体设计CAR方法与FDA批准的CAR-T细胞疗法
02
团队观察到基于APRIL的sCAR-T细胞的毒性,与BCMA CAR-T细胞在一系列具有临床相关抗原密度的BCMA/TACI双阳性细胞系中相当。APRIL重定向的sCAR-T细胞的杀伤活性,与BCMA-CAR-T细胞在中等至高抗原密度的细胞系中一致,但在BCMA表达低的细胞系中略有降低。这种差异可能归因于BCMA CAR-T细胞,能够同时靶向BCMA抗原的两个表位。通过比较BAFF重定向的sCAR-T细胞与CD19 CAR-T细胞,团队观察到在BAFFR/BCMA/TACI三阳性IM9细胞系中具有相似的杀伤活性,但在其他具有临床相关抗原密度的细胞系中活性较差。这种差异可能是由于BAFFR/BCMA/TACI抗原的密度,显著低于CD19抗原。尽管BAFF特异性sCAR-T细胞在这些情况下的疗效不如CD19 CAR-T细胞,但BAFF特异性sCAR-T细胞在缺乏CD19靶标的细胞系中具有优势,突出了BAFF作为血液肿瘤靶向域的优势,特别是其克服CD19抗原逃逸的能力。总之,虽然sCAR-T细胞在单一目标能力方面与FDA批准的疗法存在差距,但分体设计CAR方法的多目标能力和灵活性,提供了优势和显著的临床转化潜力。
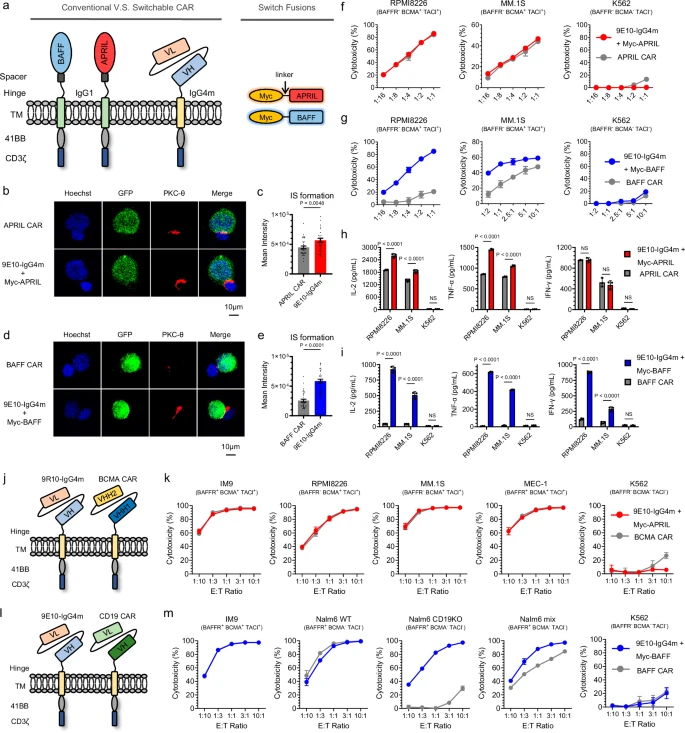
分体式设计CAR方法与传统CAR的体外比较。
分体设计基于配体的CAR-T系统的临床转化潜力
03
与体外研究结果一致,APRIL重定向的sCAR-T显示出与BCMA CAR-T细胞相当的肿瘤清除率和血清细胞因子释放。在治疗过程中未观察到小鼠显著体重减轻,并且在实验结束时,两治疗组的所有小鼠均未出现疾病复发并存活下来,突出了分体设计APRIL基于CAR-T细胞作为MM治疗的有希望的策略。在用Nalm6-WT和Nalm6-19KO细胞建立的B-ALL免疫逃逸模型中,基于BAFF的sCAR-T细胞在涉及CD19抗原逃逸的情况下,显示出优越的肿瘤清除、增加的细胞因子释放、改善的持久性,并显著延长了存活时间。在实验的第18天,只有在CD19 CAR-T治疗的小鼠的外周血中检测到CD19阴性肿瘤细胞,但在sCAR-T治疗的小鼠中未检测到肿瘤细胞。尽管在基于BAFF的sCAR-T细胞治疗后第36天观察到肿瘤复发,但团队未检测到白血病细胞表面BAFFR的丢失,这表明复发可能与开关给药的中断有关,而不是抗原逃逸。在B-NHL免疫逃逸模型中,Raji-WT和Raji-19KO细胞被s.c.移植到小鼠中,结果与白血病模型中观察到的结果一致,强调了BAFF重定向的sCAR-T细胞在克服CD19 CAR-T细胞治疗后抗原逃逸的优势。这些结果进一步证实,分体设计基于配体的CAR-T细胞系统展现出多目标能力、广谱疗效,并与FDA批准的CAR-T细胞疗法相比具有临床相关性。
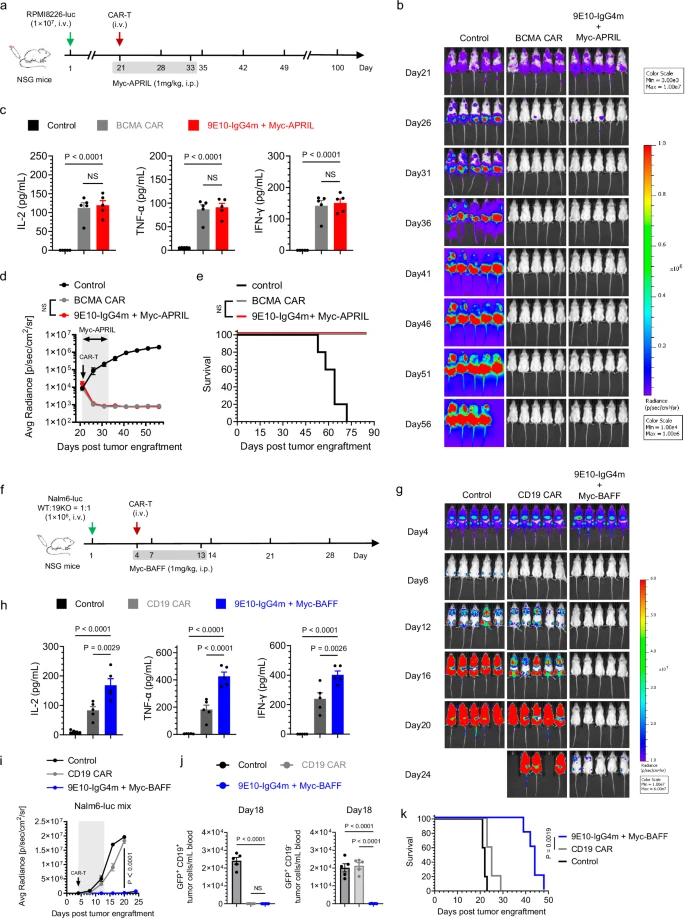
分体式设计CAR方法与FDA批准的CAR的体内比较。
总结
04
1. CAR-T细胞疗法在B细胞恶性肿瘤患者中的复发率较高,需要新的策略来提高疗效。抗体组合或多特异性配体的补偿策略,已在临床试验中成功探索。基于配体的CAR设计,相比基于scFv的设计在某些情况下具有优势,并正在接受临床试验。
2. 分体设计CAR-T细胞利用配体的多特异性,保持天然配体结构和靶向特异性,提供比传统CAR-T细胞方法更明显的优势。
3. 结构优化的sCAR-T细胞在体外和体内对各种B细胞恶性肿瘤,表现出理想的广度和效力。
4. 分体设计CAR方法提供了更广泛的适应症、多目标组合和修改的灵活性,突出了其在临床转化中的显著潜力。
5. 基于APRIL和BAFF的sCAR-T细胞策略,在临床环境中,对于治疗具有异质性抗原表达的B细胞恶性肿瘤具有潜力。
参考资料:
1. Majzner, R. G. & Mackall, C. L. Tumor antigen escape from CAR T-cell Therapy. Cancer Discov. 8, 1219–1226 (2018).
2. Shah, N. N. et al. Bispecific anti-CD20, anti-CD19 CAR T cells for relapsed B cell malignancies: a phase 1 dose escalation and expansion trial. Nat. Med. 26, 1569–1575 (2020).
 腾讯登录
腾讯登录









还没有人评论,赶快抢个沙发