【STTT】中国科学院王莹团队:限制乳腺癌肺转移的潜在治疗靶点
| 导读 | 获得免疫抑制表型的巨噬细胞在建立预转移微环境(PMN)中发挥着关键作用,而预转移微环境对于促进乳腺癌向远处器官转移至关重要。 |
12月18日,中国科学院王莹研究团队在期刊《Signal Transduction and Targeted Therapy》上发表了研究论文,题为“Macrophages promote pre-metastatic niche formation of breast cancer through aryl hydrocarbon receptor activity”,本研究表明,肺巨噬细胞中Aryl hydrocarbon receptor (AHR)的活性在建立乳腺癌的免疫抑制性PMN中起着关键作用。具体来说,AHR激活直接与Pdl1的启动子结合,导致肺巨噬细胞中PD-L1的高表达。PD-L1的上调促进了PMN中调节性T细胞(Tregs)的分化,进一步增强了免疫抑制条件。在Ahr条件敲除的小鼠中,乳腺癌的肺转移减少。PMN巨噬细胞中AHR水平的升高是由乳腺癌细胞分泌的GM-CSF引起的。在乳腺癌患者中,AHR和PD-L1的表达与Treg细胞浸润增加相关,AHR水平越高,预后越差。这些发现揭示了乳腺癌细胞、肺巨噬细胞和Treg细胞通过GM-CSF-STAT5-AHR-PD-L1级联通路进行的交叉通讯,在乳腺癌进展过程中调节肺前转移微环境。

https://www.nature.com/articles/s41392-024-02042-5#Sec9
背景信息
01
远处器官的转移形成是乳腺癌患者死亡的主要原因。转移的发生是一个复杂的多步骤过程。每个步骤都需要癌细胞适应新的微环境并克服许多物理和生物学障碍。越来越多的证据表明,在肿瘤细胞到达远处组织之前,一种被称为“前转移微环境”的特殊微环境已经建立,以支持癌细胞的生存和生长。这些PMN的特点是异常的血管完整性、异常的细胞外基质蛋白分布、基质的重塑和免疫抑制。肿瘤细胞释放的因子在动员和招募骨髓来源细胞以调节PMN的形成中起着关键作用。值得注意的是,在体外和体内预临床模型中,阻断关键分子的PMN形成可以有效地抑制肿瘤转移。因此,了解PMN形成的机制对于识别潜在的治疗靶点以预防或减少转移至关重要。
巨噬细胞在形成免疫抑制性PMN中起着关键作用。PMN中巨噬细胞的激活和积聚是由多种因素驱动的。最近的研究揭示,PMN中的免疫抑制性巨噬细胞可以通过表达树突状细胞受体表达2(TREM2)和程序性死亡配体1(PD-L1)来进行表征。在某些条件下,巨噬细胞中高水平的PD-L1表达可以促进调节性T(Treg)细胞分化,这是免疫耐受的关键调节因子,可以抑制抗肿瘤免疫反应。研究表明,PMN中的Treg细胞可以由肿瘤诱导的调节性B细胞产生的CD4+ T细胞产生。此外,肺癌衍生的外泌体已被证明可以通过CCL1-CCL8趋化因子轴促进Treg细胞分化。这些免疫细胞通过抑制Th1细胞反应、诱导T细胞耗竭、降低自然杀伤(NK)细胞活力、抑制T细胞增殖和细胞因子产生等方式,共同改造和准备环境,以容纳扩散的肿瘤细胞。
表达AHR的巨噬细胞通过调节T细胞分化促进乳腺癌向肺部转移
02
为了探究AHR在巨噬细胞中的活动对乳腺癌肺转移的影响,研究人员采用Cre-Lox重组系统在体内特异性地删除巨噬细胞中的AHR。研究人员将AhrflflLyz2Cre+/-小鼠和对照小鼠通过皮下注射的方式接种4T1细胞至乳腺脂肪垫。研究人员观察到AhrflflLyz2Cre+/-小鼠的4T1细胞肺转移显著受到抑制,这可通过肺组织的宏观和微观分析得到证实。同样,这些AhrflflLyz2Cre+/-小鼠的生存率显著提高。与4T1细胞肺转移类似,Py8119细胞肺转移在AhrflflLyz2Cre+/-小鼠中也得到减少。
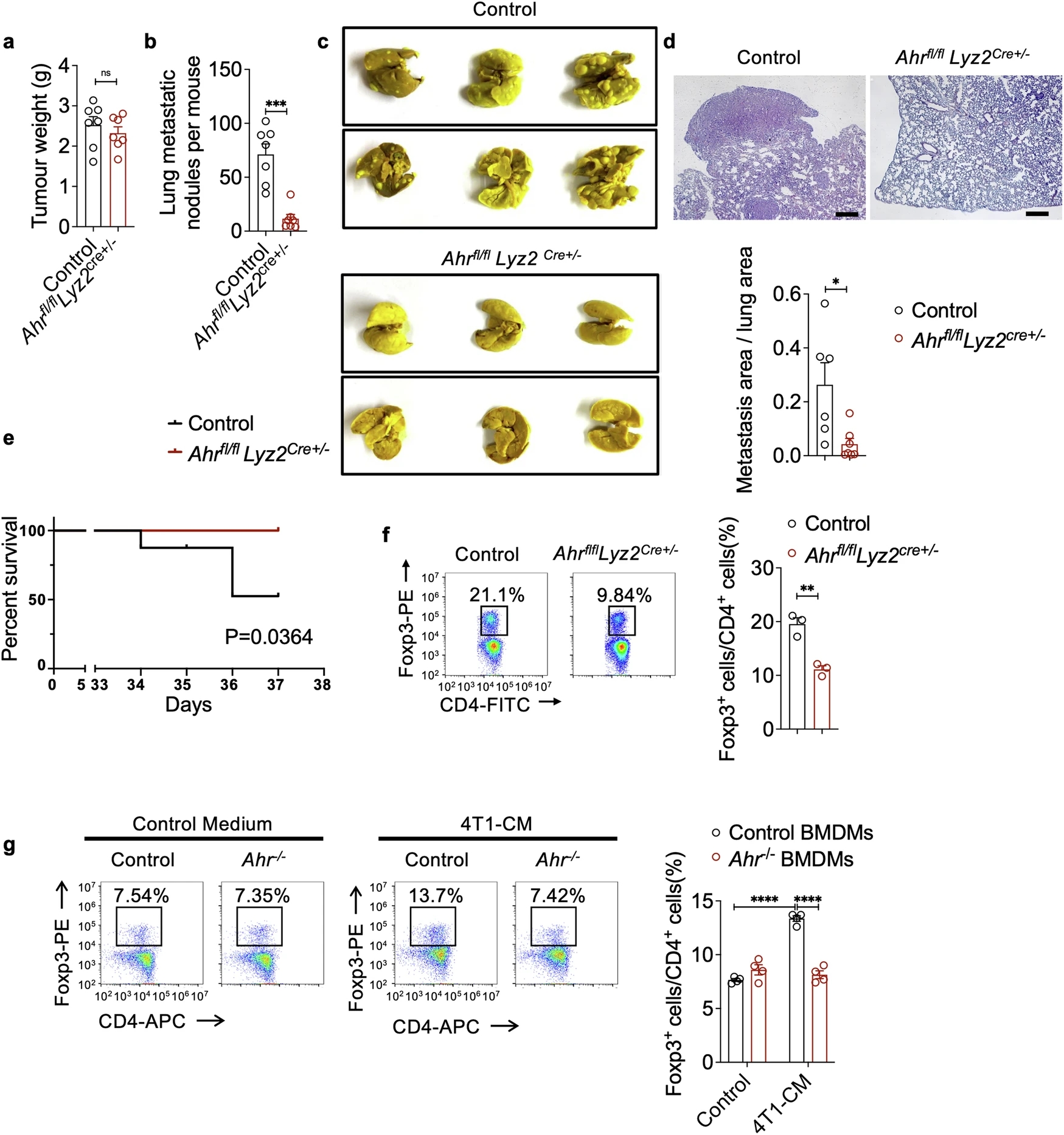
巨噬细胞中的AHR影响乳腺癌转移和调节性T细胞分化
为了确定AHR在巨噬细胞中的活性如何调节免疫抑制性PMN的形成,以促进4T1肿瘤的侵袭和再生长,研究人员在肿瘤形成前检测了肺部的免疫细胞亚群。虽然对照组小鼠和AhrflflLyz2Cre+/−小鼠的CD8+T细胞、CD4+T细胞、NK细胞、B细胞、中性粒细胞和单核细胞水平相似,但AhrflflLyz2Cre+/−小鼠PMN中最显著的变化是Foxp3+Treg细胞水平的显著降低。然而,AHR在巨噬细胞中的缺陷对原发肿瘤中Treg细胞的比例没有影响。
为了评估缺乏AHR的巨噬细胞对Treg细胞的影响,研究人员从野生型(WT)小鼠的脾脏中收集未成熟的CD4+ T细胞,并与WT骨髓源性巨噬细胞(BMDMs)或Ahr−/− BMDMs共同培养,这些BMDMs预先用正常培养基或4T1-CM处理。研究人员发现,与用正常培养基处理的BMDMs相比,用4T1-CM处理的WT BMDMs更能有效地诱导Treg细胞分化。然而,在缺乏AHR的情况下,用4T1-CM预先处理的BMDMs诱导Treg细胞分化的能力显著降低。除了AhrflflLyz2Cre+/−小鼠外,研究人员还在AHR-缺乏(Ahr−/−)小鼠中接种4T1并评估其肺转移情况。与AhrflflLyz2Cre+/−小鼠的乳腺癌进展类似,Ahr−/−小鼠的转移结节数量减少,肺部Treg细胞水平降低,但原发肿瘤生长没有变化。这些结果表明,巨噬细胞中AHR的激活可以调节PMN的免疫抑制,并影响乳腺癌的肺部扩散。
结论
03
综上所述,本研究表明,原发性乳腺癌的GM-CSF诱导的肺巨噬细胞中AHR水平的升高,对于建立一个免疫抑制环境,促进乳腺癌细胞的定植和再生至关重要。研究人员认为PMN中的AHR可能是限制乳腺癌肺转移的潜在治疗靶点。(转化医学网360zhyx.com)
【参考资料】
https://www.nature.com/articles/s41392-024-02042-5#Sec9
【关于投稿】
转化医学网(360zhyx.com)是转化医学核心门户,旨在推动基础研究、临床诊疗和产业的发展,核心内容涵盖组学、检验、免疫、肿瘤、心血管、糖尿病等。如您有最新的研究内容发表,欢迎联系我们进行免费报道(公众号菜单栏-在线客服联系),我们的理念:内容创造价值,转化铸就未来!
转化医学网(360zhyx.com)发布的文章旨在介绍前沿医学研究进展,不能作为治疗方案使用;如需获得健康指导,请至正规医院就诊。
 腾讯登录
腾讯登录









还没有人评论,赶快抢个沙发