驱狼赶虎!疟疾蛋白竟成肿瘤早诊关键!|Nature子刊
| 导读 | 我们知道,肿瘤转移是恶性肿瘤患者死亡的主要原因。恶性肿瘤细胞可自原发癌组织脱落进入血液,形成循环肿瘤细胞(CTC),尽早发现血液CTC,对肿瘤早期诊断、患者预后判断、疗效评价和个体化治疗都有着重要的指导作用。然而,目前CTC的捕获是个难题,大部分技术受限于抗体,导致一些CTC逃脱。能否“无差别”地抓住所 |
作者:Ruthy,Zoe
导 读
我们知道,肿瘤转移是恶性肿瘤患者死亡的主要原因。恶性肿瘤细胞可自原发癌组织脱落进入血液,形成循环肿瘤细胞(CTC),尽早发现血液CTC,对肿瘤早期诊断、患者预后判断、疗效评价和个体化治疗都有着重要的指导作用。然而,目前CTC的捕获是个难题,大部分技术受限于抗体,导致一些CTC逃脱。能否“无差别”地抓住所有的CTC呢?近日,哥本哈根大学的研究人员将疟疾蛋白—VAR2CSA用于捕获CTC,并获得了巨大成功!这种方法与肿瘤表面抗原无关!这让几乎所有肿瘤无所遁形!

想要准确抓住所有CTC,得先知道CTC的特性。脱离原发灶入血的CTC要面临血流剪应力、失巢凋亡、免疫细胞识别杀伤等致命考验,最终只有不足0.01%可顺利存活,而目前常用的CTC分离技术多依赖于抗体混合物。
要知道,很多肿瘤细胞表面并不存在现有抗体能识别的抗原,传统方法只能捕获特定肿瘤类型的CTC,直接漏掉了没有免疫反应的CTC,因此灵敏度一直受到质疑。
CTC量少的问题我们暂时无能为力,所以研究人员致力于将这不到0.01%顺利存活的CTC尽可能地分离出来,而要达成这个目标最重要的就是确认所有CTC共有的可被识别的标记,同时找到可以敏锐识别这种标记的物质。
研究人员发现一种特殊糖蛋白—硫酸软骨素(CS)在超过95%的癌细胞表面过表达!而且不同癌细胞的CS表达量大不相同,也就是说,只要识别这些CS,几乎所有的癌细胞都能被准确分离!

VAR2CSA特异性结合不同类型癌细胞
解决了CTC标记的问题,接下来就要找到可识别CS的物质。研究人员发现,在感染疟疾的胎盘中,疟疾蛋白VAR2CSA可与受寄生虫感染的细胞表面的CS稳定结合,而其对正常细胞CS几乎没有结合效果!
也就是说,VAR2CSA只结合有问题的细胞,其识别能力有保证。那么,VAR2CSA是否可以作为CTC的捕获剂呢?
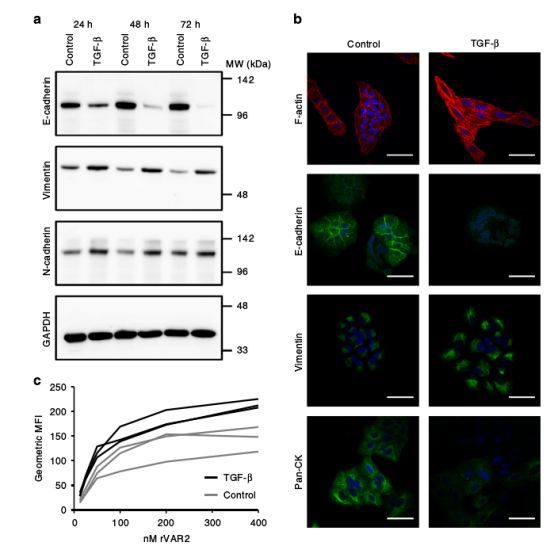
VAR2CSA对肿瘤细胞的高结合能力
答案是肯定的。初步的测试证实,VAR2CSA可以捕获各种临床血液样本的上皮和间充质癌细胞。研究人员发现,在常规血液样本(5 mL)中,VAR2CSA对CTC的捕获率令人十分满意。
当血液样本中含有100个癌细胞时,捕获率达90%,当癌细胞降为6个时,捕获率仍维持76.7%,即使仅有3个癌细胞,捕获率也有60%!简而言之,VAR2CSA对CTC的灵敏度是传统免疫捕获可望而不可及的!
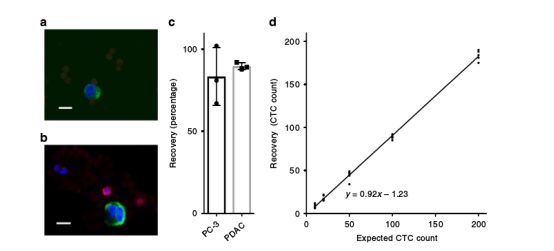
VAR2CSA有效分离CTC
CTC顺利捕获后还要面临的问题是如何准确分离肿瘤细胞。前面说过,不同肿瘤细胞表面CS表达量大不相同,自然结合VAR2CSA的量也不尽相同。
研究人员证实,VAR2CSA子可以有效地分离胰腺癌、肝癌、前列腺癌和肺癌等不同类型的癌症,甚至可以通过VAR2CSA结合状况判定肿瘤分期!而其对正常细胞极低的结合率更是有效解决了假阳性的问题!
VAR2CSA的分离方法不仅为CTC检测提供了更灵敏、更通用的工具,而且还可以分离出更多CTC子集,是一种极佳的下游细胞分析工具。
因此,这项技术有望为癌症患者高转移亚群的研究提供进一步的见解,提高我们对癌症转移的理解,并有助于开发出更有效的治疗方法。
参考文献:
The VAR2CSA malaria protein efficiently retrieves circulating tumor cells in an EpCAM-independent manner
Circulating Tumor Cells Get "Sucked Up" By Malaria Protein
(转化医学网360zhyx.com)
 腾讯登录
腾讯登录

还没有人评论,赶快抢个沙发