靶向“乳酸代谢” !上海交大发文:揭示肿瘤治疗新策略
| 导读 | 免疫疗法已经成为癌症治疗的一种有效的临床方法,但只有一小部分癌症患者可以从中受益。靶向肿瘤细胞中的乳酸代谢(LM)作为增强抗肿瘤免疫反应的方法是一种很有前途的治疗策略。 |
4月25日,上海交大研究团队在期刊《Journal of Experimental & Clinical Cancer Research》上发表了研究论文,题为“Pan-cancer analysis implicates novel insights of lactate metabolism into immunotherapy response prediction and survival prognostication”。本研究中,研究人员揭示了LM与免疫治疗耐药之间的密切相关性,并进一步建立了泛癌症LM. sig,它有可能成为选择适合免疫治疗的患者的有竞争力的工具。

https://jeccr.biomedcentral.com/articles/10.1186/s13046-024-03042-7#Sec30
研究背景
01
免疫疗法的出现标志着癌症治疗的一个变革时代,为患者带来了前所未有的临床优势。然而,有限的应答率和无法预测临床疗效阻碍了它们的进一步应用,这强调了生物标志物检测的迫切需要,以促进精准用药和制定有效的联合策略,以对抗免疫耐药性。传统的生物标志物筛选主要集中在探索来自患者的组学数据。然而,这种方法仅捕获异质细胞群中的平均遗传表达,导致这些研究中预先存在的免疫治疗生物标志物的预测价值有限。单细胞RNA测序(scRNA-Seq)和空间转录组学(ST)的优势使我们能够在单细胞和空间分辨率下检测转录组的表达谱,从而揭示具有优越性能的新靶点。
研究进展
02
为促进LM.SIG的临床应用,迫切需要在泛肿瘤患者中寻找潜在靶点。在此基础上,根据敲除基因的细胞系类型和处理条件,从7个具有敲除基因免疫应答信息的CRISPR研究中分离出17个CRISPR数据集。对入选的22505个CRISPR基因进行z-score排序,将排名最高的基因视为免疫抗性基因。也就是说,排名靠前的基因在敲除后可能会提高抗肿瘤免疫能力,而排名靠后的基因在敲除后可能会抑制抗肿瘤免疫能力。然后,研究人员比较了LM.SIG中排名最高的基因和已发表的免疫抵抗特征中的基因的百分比。如图1B所示,LM.SIG在top-rank基因中所占比例最高。有意思的是,前5%的基因(n = 19)在LM.SIG中被过度代表(Fisher精确检验,p = 0.04)。这些基因在多个独立的CRISPR数据集中得到进一步验证,并作为免疫治疗的潜在靶点。
为了进一步研究同时具有免疫治疗预测和生存预测的靶点,研究人员将CRISPR数据集中选择的19个基因与LM.SIG相关预后模型(LMP基因)中注册的10个基因交叉。最终,LDHA被确定为枢纽基因,LDHA是LM.SIG在多个CRISPR数据集中排名最高的基因。如图1E所示,在17/22 (77.27%)TCGA泛癌数据集中,肿瘤样本中LDHA的表达较正常样本上调。人类蛋白图谱(Human Protein Atlas, HPA)数据集中的IHC也显示LDHA在宫颈癌、肾癌、肺癌和胰腺癌中的蛋白表达水平升高。此外,两个免疫治疗scRNA-seq队列(GSE115978, GSE123813)和一个ST免疫治疗队列显示,在单细胞和空间水平上,与R或TN患者相比,上调的LDHA主要富集在NR中。总之,从LM.SIG中提取的LDHA可能作为一种预后泛癌症的生物标志物,也可以预测免疫治疗反应。
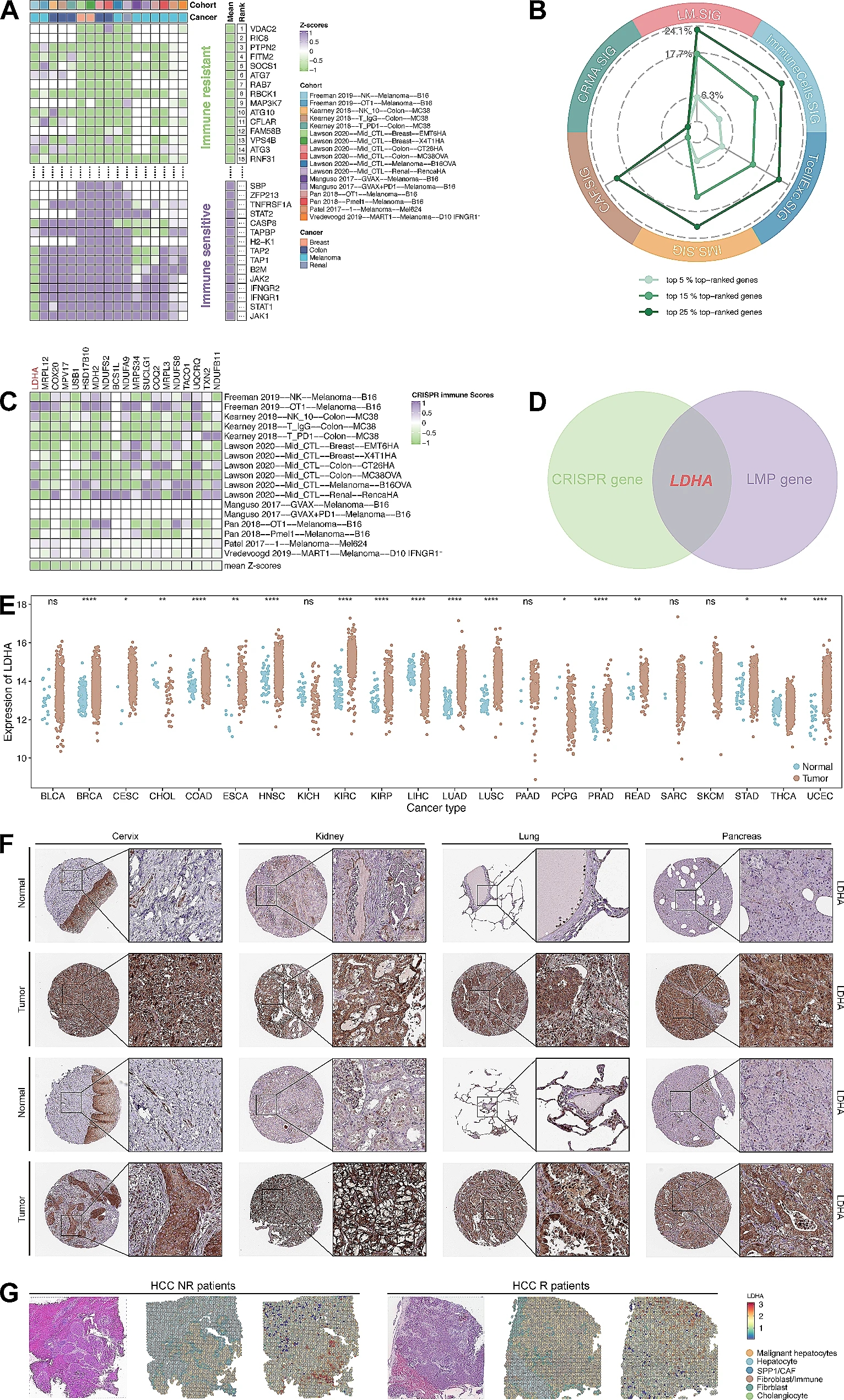
从LM.SIG中识别潜在靶点
研究结论
03
总之,本研究在免疫治疗反应预测和生存预测中对与LM相关的多种分子和代谢过程产生了创新的见解。通过对单细胞和大量转录组数据的全面泛癌症分析,研究人员制定了LM.SIG,并验证了其在不同队列中预测免疫治疗和预后结果的能力。随后对LM.SIG的研究发现LDHA是胰腺癌最有潜力的治疗靶点。本研究为通过靶向代谢重编程来提高肿瘤免疫治疗的有效性提供了新的方向。(转化医学网360zhyx.com)
参考资料:
https://jeccr.biomedcentral.com/articles/10.1186/s13046-024-03042-7#Sec30
注:本文旨在介绍医学研究进展,不能作为治疗方案参考。如需获得健康指导,请至正规医院就诊。
 腾讯登录
腾讯登录
还没有人评论,赶快抢个沙发