《科学》重磅!帕金森症关键毒性物质被找到!
| 导读 | 帕金森病是一种神经退行性疾病。帕金森症患者的生活质量一直很低。而在近期的《Science》期刊上面,一篇新的研究揭示了帕金森症背后的关键毒性物质! |
帕金森病是一种神经退行性疾病。这种疾病的一种关键特征是受损的α-突触核蛋白(alpha-synuclein)在帕金森病患者体内的一种被称作多巴胺能神经元的脑细胞中堆积。
近日,一项发表在《Science》上的研究首次发现帕金森病背后关键性毒性物质。在12月15日《Science》上“Structural basis of membrane disruption and celluar toxicity by а-synuclein oligomers ”发表。

研究人员已经发现与帕金森病相关的毒性蛋白蔟是如何破坏正常脑细胞膜,在细胞膜上产生缺陷并最终引起一系列诱导神经元死亡这一过程的时间。
这项研究检测了这种毒性低聚物,该低聚物是在单个蛋白质分子错误折叠并聚集在一起时的的蛋白质分子蔟。在帕金森病中所涉及的该种蛋白质蔟称为а-突触核蛋白,该蛋白在脑部正常的信号通路中起重要作用。
这些蛋白蔟的形成和延伸被认为是此种进行性疾病潜在性分子机制的关键构成部分。
了解他们是如何进入并损伤细胞为发展新型有效的药物提供了机遇。但直到现在,由于他们的不稳定性,了解这些蛋白是如何损伤脑细胞的仍十分困难。该蛋白在形成后不久便会分解或者组装成对细胞损伤较小的较大蛋白结构。
在这项新的研究中,学者们能够较长时间的稳定该低聚物并在前所未有的细节上明确它们是如何损伤脑细胞膜的。研究人员明确了低聚物具有一种特征,该特征可使其锚定在胞膜上并形成“结构核心”,最终得以穿透细胞膜。
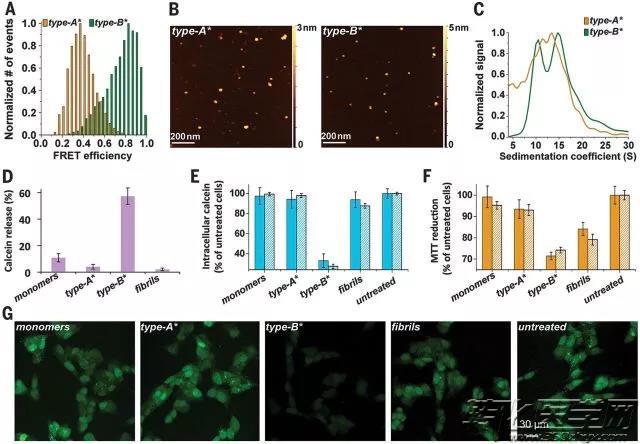
该研究由来自英国、意大利和西班牙的科学家共同进行,并由剑桥大学的Christopher Dobson博士和伦敦帝国理工学院的Alfonso De Simone博士领导。
“低聚物的共同特征是一旦他们结合于脑细胞膜上便开始破坏脑细胞,” o De Simone解释说,“这有点像把一块极热的金属放在塑料表面。在相当短的时间内,它会在塑料上烧出一个洞并穿过它。低聚物与细胞膜接触时会产生类似的作用,这会破坏膜的完整性,这是导致神经元死亡机制中的关键步骤”。
来自剑桥圣约翰学院的博士后研究员Giuliana Fusco博士在她博士研究期间为该研究进行了大量的实验研究工作,她说:“获得这些信息并不意味着我们现在就可以去制造一种新型药物,但显然如果我们能够了解这些蛋白蔟的作用机制,那么我们可以在治疗帕金森病方面取得更快的科学进展,这意味着我们可以采取更合理的方法来研发新药”。
毒性低聚物在导致帕金森病的一系列事件的早期阶段形成,而这应该是在а-突触核蛋白失效并开始粘连时开始的。在这种情况下,他们的出现对神经元的功能是致命性的。一旦低聚体形成并扩散,将导致最初的毒性物质扩散至其他细胞。
在这项研究中,研究人员使用了固态核磁共振光谱学(SSNMR)检测了实验中有毒和无毒形式的低聚а-突触核蛋白寡聚体样本。
这项技术的最新进展使他们能够以前所未有的细节研究这些低聚体。研究小组描述了这些结构的不同特征,然后研究了这些不同特性是如何影响它们与取自大鼠的脑细胞以及从人脑肿瘤中提取的细胞相互作用的。
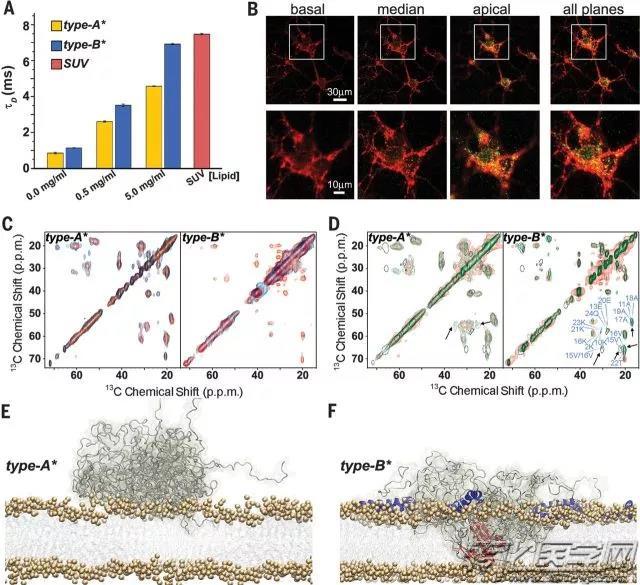
该项研究结果可以用来识别和攻击这些有害性的毒性物质,从而限制他们的作用。今年十月,剑桥大学在化学系设立了一个新的错误折叠所致疾病中心,致力于制定包括帕金森在内的一系列治疗策略。其大部分工作建立在像这样的研究之上,从而加深对神经退化背后机制的认识。由此,可能用于未来药物的分子“候选物”可被识别,并在必要时可根据疾病加以优化。
剑桥大学圣约翰学院硕士兼错误折叠疾病中心主任Dobson教授说:“这项工作真正令人兴奋的的其中之一不仅是尽可能定义了神经退行性疾病的毒性物质的结构,而且我们也设法阐明了毒性物质的作用机制,这将为寻求合理的治疗策略提供了重要的线索。”
参考资料:Structural basis of membrane disruption and cellular toxicity by α-synuclein oligomers by Giuliana Fusco,Serene W. Chen,Philip T. F. Williamson,Roberta Cascella,Michele Perni,James A. Jarvis,Cristina Cecchi,Michele Vendruscolo,Fabrizio Chiti,Nunilo Cremades,Liming Ying,Christopher M. Dobson,Alfonso De Simone
SCIENCE15 DEC 2017 : 1440-1443
(转化医学网360zhyx.com)
 腾讯登录
腾讯登录









还没有人评论,赶快抢个沙发