肿瘤百年谜团被解开!乳腺癌获新突破!
| 导读 | 困扰百年历史的“Warburg 效应”终于被贝勒医学院的研究小组找出答案。肿瘤细胞舍近求远选择糖代谢的目的浮出水面。 |
1924年,德国生理学家Otto.Warburg 提出了以他名字命名的沃伯格效应(Warburg effect),他认为:人体正常的健康细胞依靠线粒体氧化糖类分子释放出有用的能量,而肿瘤细胞则不同,它能不依靠线粒体和氧气,只通过产能率较低的糖酵解为自身供能。同时,它能扭转局势,将其糖酵解率提高至普通细胞的200倍。即使是在氧气充足的条件下肿瘤细胞也会选择该种代谢方式。
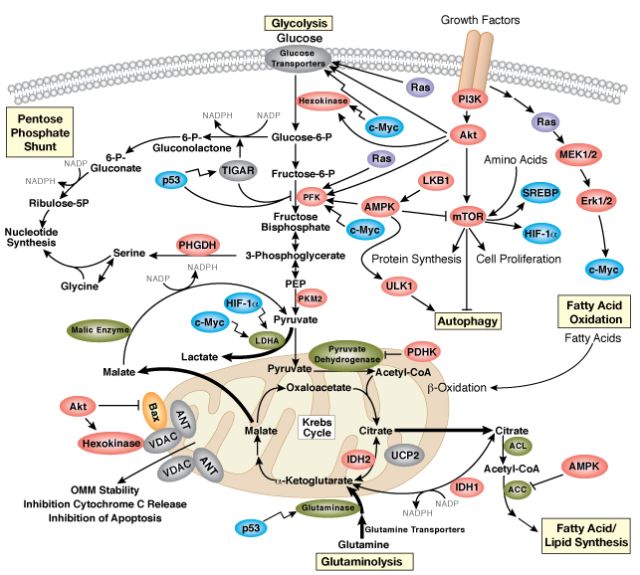
Warburg效应
Warburg提出的假说引起了不断地争议,肿瘤细胞为何要吃力不讨好的选择糖代谢而放弃线粒体代谢呢?到底是这种代谢的转变导致了癌症的产生?还是细胞癌变的产物?
从1924年至今,这个谜团困扰了人们近一百年。而近期发表于《Nature》上的一篇名为“Metabolic Enzyme PFKFB4 Activates Transcriptional Coactivator SRC-3 to Drive Breast Cancer”的文章揭开了肿瘤代谢之谜的神秘面纱!

SRC-3蛋白诱导肿瘤产生
其实早在多年前,来自贝勒医学院的Bert O'Malley教授及其团队就发现了一种名为SRC-3的核受体共激活因子,它在调节基因表达中起着重要的作用。此外,研究人员还发现它通常在乳腺癌中表达和扩增。同时,在大多数的肿瘤细胞中都能观察到SRC-3的磷酸化,并导致其转录活性、蛋白质稳定性和亚细胞定位的改变,从而使蛋白质过度活跃,进一步诱导肿瘤的产生。
代谢激酶PFKFB4
在进一步的研究中,研究小组通过筛选试验找到了影响SRC-3活性的激酶:代谢激酶PFKFB4。PFKFB4作为调控细胞增殖的最主要的激酶,抑制它的表达能降低SRC-3在肿瘤细胞的活性,而它的过度表达会促进SRC-3活性。
说了这么久,SRC-3与“Warburg 效应”到底有什么关系呢?
PFKFB4代谢激酶最主要的功能其实是在Warburg效应的途径中给糖分子添加磷酸基团。
但现在研究人员也发现它能影响SRC-3磷酸化诱导癌症的产生。PFKFB4可谓是与癌症有着千丝万缕的联系。
而在小鼠模型中,研究人员也通过抑制SRC-3的磷酸化或移除PFKFB4成功实现了乳腺癌肿瘤的生长抑制和体积的减少。
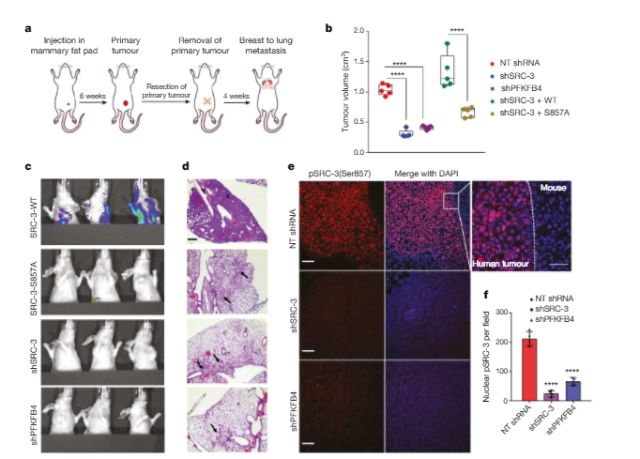
PFKFB4-SRC-3轴的激活能促进乳腺癌的原发生长和转移
果然,肿瘤细胞选中糖代谢另有阴谋!它看中了糖代谢过程中参与的PFKFB4激酶。虽然糖代谢提供的能量不高,但是它能诱导癌症细胞的产生!
O'Malley教授说道:“在这里我们发现了糖酵解通路与转录共激活物SRC-3的致癌激活之间的相互作用。Warburg效应被认为是贯穿癌症的最主要的糖代谢途径之一,它能产生能量和大分子,以维持快速的增殖和肿瘤生长。我们现在发现,糖酵解刺激器,双功能酶PFKFB4磷酸化SRC-3。SRC-3的磷酸化快速增加了其转录活性,促进了驱动葡萄糖通量的基因合成。我们的研究表明,靶向PFKFB4的SRC-3轴可能在乳腺肿瘤中具有治疗价值,明显依赖于糖代谢。”
参考文献:
Metabolic Enzyme PFKFB4 Activates Transcriptional Coactivator SRC-3 to Drive Breast Cancer.Nature(2018)
(转化医学网360zhyx.com)
 腾讯登录
腾讯登录








还没有人评论,赶快抢个沙发