Cell:刷新认知!肥胖竟会导致肝癌!
| 导读 | 今年初,国家癌症中心发布了最新一期的全国癌症统计数据,原发性肝癌全球每年新发病例85.4万例,中国46.6万,约占全球的55%;每年因原发性肝癌死亡81万,中国为42.2万,约占全球45%~50%。 |
今年初,国家癌症中心发布了最新一期的全国癌症统计数据,原发性肝癌全球每年新发病例85.4万例,中国46.6万,约占全球的55%;每年因原发性肝癌死亡81万,中国为42.2万,约占全球45%~50%,触目惊心的发病率和死亡率给我国社会和医疗带来了沉重的负担。很多人知道肝癌的发生与肝炎有关,但其实随着生活水平的提高,肥胖已经成为新的肝癌诱发新源头,美国疾病控制和预防中心2017年的一份报告显示,在过去的十年中,40%的癌症与肥胖有关,超过种子选手“吸烟”成为癌症发生发展的主要原因。
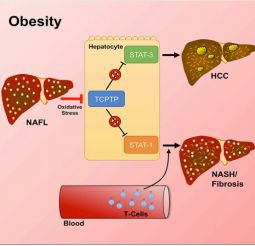
我们所了解的是肥胖会导致脂肪肝,脂肪肝演变成肝硬化,而肝硬化又很可能恶化为肝癌。我们所不知道的是,肥胖的真正可怕之处在于“不走寻常路”,其更多的是通过诱发非NAFLD(非酒精性脂肪性肝病)途径而导致肝癌发生发展,这一发现以“Obesity Drives STAT-1-Dependent NASH and STAT-3-Dependent HCC”为题发表核心期刊《Cell》上。

大多数患有肝癌的肥胖者首先发展为非酒精性脂肪性肝病(NAFLD),然后是更严重的非酒精性脂肪性肝炎(NASH),进而导致肝硬化和肝衰竭,在某些情况下甚至导致肝癌的发生。然而,目前大多数指南将肥胖患者的肝癌检测限制在仅针对肝硬化患者。
这一发现意味着有一群可能有患肝癌风险的人,他们并没有接受过该疾病的筛查。换句话说,目前肥胖患者的肝癌筛查可能会遗漏一群有风险的人。Tiganis教授表示,“如果患有NASH或肝硬化并不是肥胖人群肝癌发生的唯一途径,我们就迫切需要开发生物标记物,以帮助确定哪些NAFLD患者可能有发生HCC的风险”。
为了弄清这一问题,该研究使用了动物模型和人体组织活检组织,这些组织活检由Wendy Brown教授及其来自莫纳什大学外科学系的团队提供。研究显示,肥胖-NASH-肝硬化途径是由一种名为STAT-1的蛋白触发所驱动的。
然而,那些非NASH途径的肝癌的老鼠,他们的癌症是由一种不同的蛋白质触发的,叫做STAT-3。STAT3是在各种生理过程中起重要作用的转录因子,其失调会导致包括癌症在内的严重疾病。
《Nature Communications》也曾以“TRIM27 mediates STAT3 activation at retromer-positive structures to promote colitis and colitis-associated carcinogenesis”为题揭示了调节STAT 3活化、炎症和炎症相关癌症发展的逆转录依赖性机制。
不仅高脂饮食的小鼠会发展为肝癌,促进STAT-3信号传导也足以驱动肥胖小鼠中的肿瘤发展,且该发展完全独立于NAFLD之外,该研究为肥胖小鼠中NASH-肝硬化与肝癌的发展定义了两种不同的分子途径,为预防肥胖患者发生肝硬化或肝癌的进展开辟了道路。
目前有一些药物被批准用于针对STAT-1和STAT-3途径的其他疾病,然而,Tiganis教授表示,现在认为这些药物可以对预防肥胖人群肝癌的发展产生有益影响还为时过早。肝癌的标准化学治疗反应较差,在大多数情况下对总生存率没有影响。目前我们迫切需要的还是开发有针对性的治疗方法。
参考文献:
Marcus Grohmann, Florian Wiede,Garron T. Dodd,Obesity Drives STAT-1-Dependent NASH and STAT-3-Dependent HCC
(转化医学网360zhyx.com)
 腾讯登录
腾讯登录









还没有人评论,赶快抢个沙发