Nature子刊:新模型深度分析膜蛋白,助力肿瘤治疗新靶点诞生!
| 导读 | 肿瘤是基因病,这几乎已经成为了共识。诸多肿瘤相关基因参与了肿瘤的发生发展,这些基因表达的产物多为膜蛋白(MPs),与肿瘤细胞的恶性行为密切相关。目前市场上销售的药物80%作用于MPs,但由于MPs的溶解、分离、鉴定十分困难,造成肿瘤相关蛋白组学研究严重滞后。 |
肿瘤是基因病,这几乎已经成为了共识。诸多肿瘤相关基因参与了肿瘤的发生发展,这些基因表达的产物多为膜蛋白(MPs),与肿瘤细胞的恶性行为密切相关。目前市场上销售的药物80%作用于MPs,但由于MPs的溶解、分离、鉴定十分困难,造成肿瘤相关蛋白组学研究严重滞后。近日,台北医科大学何元顺教授作为通讯作者在《Nature Communications》发表的文章中,研究人员建立了一个全新的癌膜蛋白调节网络(CaMPNets)模型,系统整合了MPs相互作用、基因组学和临床结果研究,建立了“MPs社区”,并成功鉴定了新型乳腺癌预后生物标记物和可药物靶标!
“MPs社区” vs MPs——
系统化助力肿瘤相关分析
肿瘤相关研究历来是科研领域的重点与难点,MPs的过表达/缺失/修饰可导致肿瘤细胞的信号传导、物质运输、黏附作用、免疫原性等发生改变,从而影响了肿瘤的发生发展和转移,因此,肿瘤MPs的单克隆抗体在肿瘤诊断、治疗以及探索肿瘤相关基因等研究领域中有重要意义。MPs是理想的药物靶点,MPs的功能决定了膜的功能,但因技术限制,仅针对MPs的研究难以有实质性进展。既然将MPs脱离细胞有难度,那么能否在细胞环境中探明MPs的功能呢?
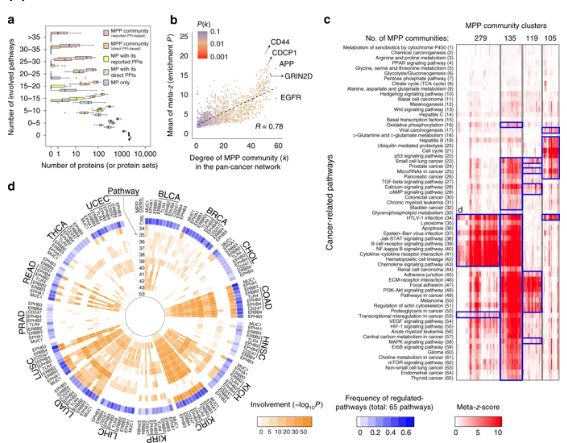
CaMPNets调解网络
研究人员选择不将MPs剥离所在环境,反而将MPs和相关基因、调控的通路组成了一个“社区”,建立了CaMPNets模型,从而系统地分析MPs的作用。他们证实,与单纯分析MPs相比,CaMPNets可准确鉴定和分析出MPs相互作用的蛋白质,同时发现了许多MP相互作用的未知蛋白。
另外,研究人员通过CaMPNets理清了MPs调控的15种癌症类型通路,并将其用于泛癌分析,系统全面地绘制了“MPs社区”中组成差异/相似性及其跨人类癌症的调节途径,有助于探索肿瘤异质性和新靶点。更重要的是,他们利用CaMPNets探索了肿瘤预后图景,为开发基因组预后生物标记物提供了获取途径。换言之,系统化的“MPs社区”研究拓宽了新靶点新标志物的获取途径。
乙酰胆碱受体(CHRNA9):
CaMPNets探索下的多肿瘤靶点
CHRNA9是作为神经递质和离子通道的MPs,研究人员用CaMPNets探索了其肿瘤相关作用。他们发现CHRNA9群落在肿瘤形成,进展和转移中起重要作用,尤其在乳腺癌中,CHRNA9可与ERBB2和EGFR相互作用,介导细胞间黏附,从而降低乳腺癌转移,有利于肿瘤预后。他们表示CHRNA9调节的粘附连接通路不仅与乳腺癌转移相关,同时还是多种实体瘤有利预后的重要预测因子。而且,研究人员还发现CaMPNets可用于鉴定各种癌症类型中与CHRNA9相关的潜在蛋白质。
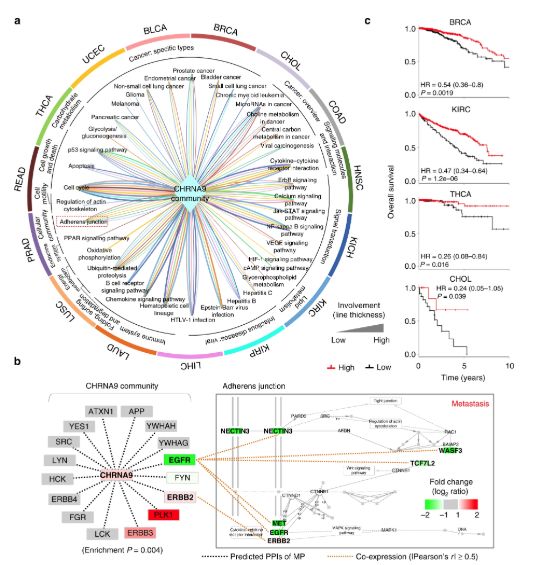
CaMPNets探索下的CHRNA9网络
进一步的研究指出,尼古丁可强烈解离CHRNA9 / ERBB2复合物的形成,激活ERBB2的细胞信号转导,这就意味着CHRNA9可能是尼古丁诱导的乳腺癌的潜在治疗靶标,而体外研究发现安非他酮的预处理可以显着抑制CHRNA9 / ERBB2复合物的解离,抑制尼古丁的信号传导恢复细胞粘附性,降低乳腺癌的转移,也就是说,安非他酮可作为CHRNA9的变构抑制剂抑制乳腺癌的转移!
同时,CaMPNets模型分析显示安非他酮还可抑制肺癌转移相关途径中CHRNA9的信号级联,并减弱尼古丁诱导的细胞转移,实现尼古丁阻断。换言之,CHRNA9可同时作为乳腺癌、肺癌转移的预测因子和药物靶点,而安非他酮正是该靶点的有效变构抑制剂。
该研究揭示了“MPs社区”癌症范围图谱和预后情况,为进一步研究和临床翻译提供了大量线索,为新生物标志物和治疗靶标发展提供了新希望,为进一步的临床应用拓宽了道路。更多的新靶点,能带来更多有希望的肿瘤药物,希望这一天不会太远。(转化医学网360zhyx.com)
参考文献:
Chun-Yu Lin,et al.Membrane protein-regulated networks across human cancers.Nature Communicationsvolume 10, Article number: 3131 (2019) .
 腾讯登录
腾讯登录









还没有人评论,赶快抢个沙发