【Nature子刊】「巨胞饮」导致肿瘤耐药:「饿不死」的癌细胞还能吃自己!
| 导读 | 目前,化疗是癌症治疗的重要手段之一,许多药物通过阻断癌细胞的DNA合成和其他代谢过程,或减少肿瘤血管新生和营养供应,以达到“饿”死癌细胞的目的。但是,多数化疗均以失败告终。临床上已经采取了多药合用、靶向治疗等手段,多角度围攻癌细胞,但对于癌症的耐药性,至今尚无有效的解决办法。 |
近日,加州大学的生物学家Aimee Edinger和Vaishali Jayashankar发现,尽管生物合成过程多被药物阻断,癌细胞仍能通过巨胞饮过程从肿瘤死细胞碎片中摄取必需的生物材料,以维持自身的扩张。除了此前报道的氨基酸之外,脂质和糖类均能被重复利用。研究者们认为,巨胞饮抑制剂可能是肿瘤耐药的新的治疗方案,这一工作发表在Nature Communications上。

巨胞饮是内吞的一种形式,在某些因素的刺激下,细胞膜褶皱形成大而不规则的内吞囊泡,直径巨大,为非选择性地摄入细胞外的蛋白、液体和颗粒提供有效途径。

由于肿瘤细胞疯狂地急剧扩张以及异常的血管微环境,肿瘤组织内部细胞通常得不到充分的氧气和营养物质供应,因此自噬和巨胞饮就成了癌组织得过且过的“续命大法”。研究者发现肿瘤组织内部分散着大量死细胞(70-80%),它们通过发生凋亡,从而刺激周围细胞的增殖。进而,活细胞反过来通过巨胞饮摄取死细胞中已经存在的生物大分子,大大提高了细胞的资源利用率。

巨胞饮促进了乳腺癌细胞在氧糖剥夺条件下的存活
此前研究认为,巨胞饮过程仅摄取氨基酸,为活细胞提供生物燃料和基础分子。研究者通过点击化学的流量分析,证实乳腺癌细胞还能通过巨胞饮过程回收糖类、脂肪酸等生物大分子。这个过程与癌细胞中PTEN和PIK3CA等基因突变有关。
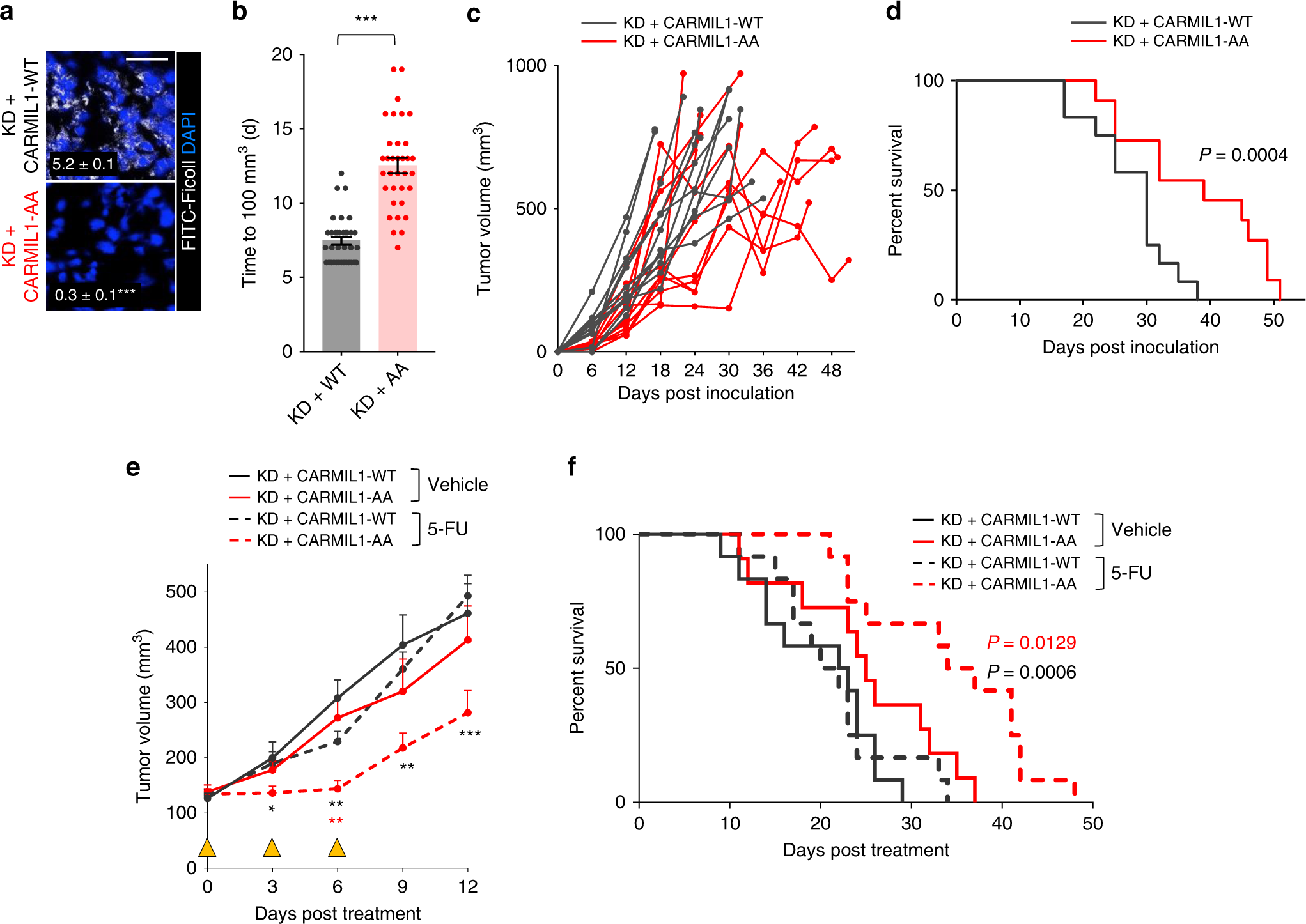
研究者还证实了阻断巨胞饮过程能够恢复癌细胞对药物的敏感性,逆转耐药过程。研究者们选择性敲除了巨胞饮过程密切相关的肌动蛋白封端蛋白调节剂CARMIL1-AA,发现癌细胞对营养剥夺和5-FU抗癌药物的响应回升。
参考文献:
NVaishali Jayashankar, et al. Macropinocytosis confers resistance to therapies targeting cancer anabolism. Nature Communications. 28 Feb, 2020.
(转化医学网360zhyx.com)
 腾讯登录
腾讯登录









还没有人评论,赶快抢个沙发