“双突破”!山东大学马春红团队揭示肝癌进展新发现 提供肝癌治疗新策略
| 导读 | 导读:在我国,肝细胞癌(hepatocellular carcinoma, HCC)是常见高发病率和致死率的恶性肿瘤之一。代谢重塑(metabolism reprogramming)是肿瘤的标志特征,因此干预代谢重塑成为治疗肿瘤的热点。谷氨酰胺(Glutamine)是肿瘤生长的必需氨基酸,通过限制谷氨酰胺利用是一项极具潜力的治疗肿瘤手段。 |
近日,山东大学基础医学院马春红教授团队在知名期刊 《Redox Biology》上发表了题为“Lipophagy-mediated cholesterol synthesis inhibition is required for the survival of hepatocellular carcinoma under glutamine deprivation”的研究论文。本研究以肝癌为模型,深入探讨了肿瘤适应谷氨酰胺限制的分子机制。研究发现,谷氨酰胺限制能够诱导肝癌细胞发生脂滴自噬(lipophagy),从而将胆固醇从脂滴转运到内质网上,通过抑制胆固醇合成来降低 NADPH 的消耗,进而维持胞内氧化还原平衡,有利于肝癌细胞存活。更为重要的是,通过基因工程手段或药物处理解除胆固醇合成抑制显著增强了谷氨酰胺限制抑制肝癌的效果。

https://www.sciencedirect.com/science/article/pii/S2213231723001337?via%3Dihub
研究背景
01
代谢重塑是癌症的一个标志特征,它为癌细胞的高增殖和存活提供了能量和基础。越来越多的证据表明,谷氨酰胺是肿瘤的生长必需氨基酸,对肿瘤的生物能量和生物合成过程至关重要。限制谷氨酰胺利用的策略正在成为癌症的潜在治疗方法。然而,由于代谢的可塑性,癌细胞能够适应谷氨酰胺的缺乏。作为一种肿瘤抑制因子,p53的活性在谷氨酰胺饥饿的反应中增加。在癌细胞中保留野生型p53可以帮助它们通过代谢改变来适应营养应激,如降低能量需求、平衡氧化还原和增加脂肪酸氧化(FAO)。此外,补充天冬酰胺已被证明可以减少谷氨酰胺耗竭时癌细胞的细胞死亡。到目前为止,癌细胞适应谷氨酰胺剥夺的机制尚未完全阐明。探索这一新机制成为制定有效治疗策略的迫切需要。
胆固醇在肿瘤生长中起着重要作用。越来越多的证据表明,胆固醇代谢在许多方面促进了癌症的发展,包括细胞增殖、耐药、迁移和侵袭。甾醇调节元件结合转录因子2 (SREBF2)是胆固醇代谢的主要调节因子,据报道在HCC患者中高表达,并与患者预后不良相关。SREBF1与SREBF2同属一个家族,主要调控脂肪酸代谢。近期研究表明,谷氨酰胺剥夺降低SREBF1活性,抑制脂肪酸合成,有助于谷氨酰胺剥夺下肺癌细胞的存活。srebf2调节的胆固醇代谢是否也在癌细胞对谷氨酰胺剥夺的适应中起作用尚不清楚。
自噬,即“自我吞噬”,降解细胞内碎片,为细胞在压力条件下生存提供能量和必要的基质。脂噬是一种依赖溶酶体的脂溶途径,通过脂滴(ld)被选择性地分解以维持细胞脂质稳态。先前的研究表明,脂质吞噬具有促进和抗癌的作用。雷帕霉素靶蛋白1 (mTORC1)可以感知癌细胞的营养和能量水平,从而调节应激条件下细胞的生长。然而,脂噬和mTORC1信号在谷氨酰胺剥夺反应中的相互作用仍不清楚。
在这里,研究人员发现谷氨酰胺剥夺诱导脂噬增加内质酶胆固醇水平,导致抑制胆固醇合成。抑制胆固醇合成可防止NADPH耗尽和脂质过氧化,使HCC细胞在谷氨酰胺剥夺下存活。这些发现为HCC提供了潜在的治疗策略。
研究过程
02
为了评估胆固醇合成对HCC适应谷氨酰胺剥夺的影响,在指定条件下通过量化Sub G1群体来测量细胞死亡。结果显示,silnsig -1能提高转染谷氨酰胺或不转染谷氨酰胺的HepG2细胞中HMGCR和SQLE的表达,而siSREBF2能逆转谷氨酰胺剥夺条件下silnsig -1转染HepG2细胞中HMGCR和SQLE的升高。所有这些数据表明,谷氨酰胺剥夺对胆固醇合成的抑制可防止HCC细胞死亡。
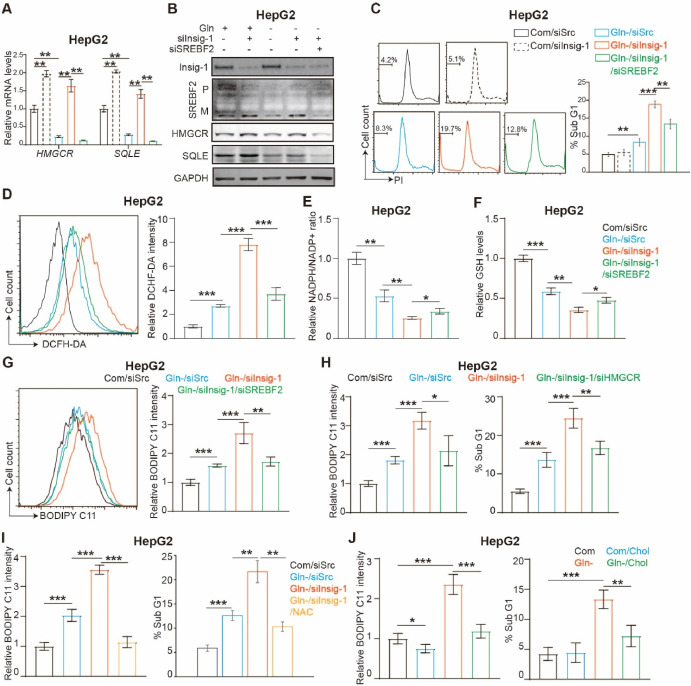
逆转胆固醇合成抑制可增强谷氨酰胺剥夺诱导的细胞死亡
由于SREBF2是胆固醇合成的主要调节因子,研究人员进一步研究了谷氨酰胺剥夺是否会改变SREBF2状态。

谷氨酰胺剥夺通过NPC1增加 ER 胆固醇
为了阐明谷氨酰胺剥夺下细胞内质网胆固醇升高的分子机制,研究人员检测了介导胆固醇转运至内质网的Niemann-Pick型C1 (NPC1)在谷氨酰胺剥夺下的表达。
为了进一步解释谷氨酰胺剥夺下内质网胆固醇升高的原因,研究人员研究了胆固醇稳态的途径。由于胆固醇合成在谷氨酰胺剥夺下受到抑制,研究人员测试了ldlr介导的LDL摄取是否有助于内质网胆固醇升高。
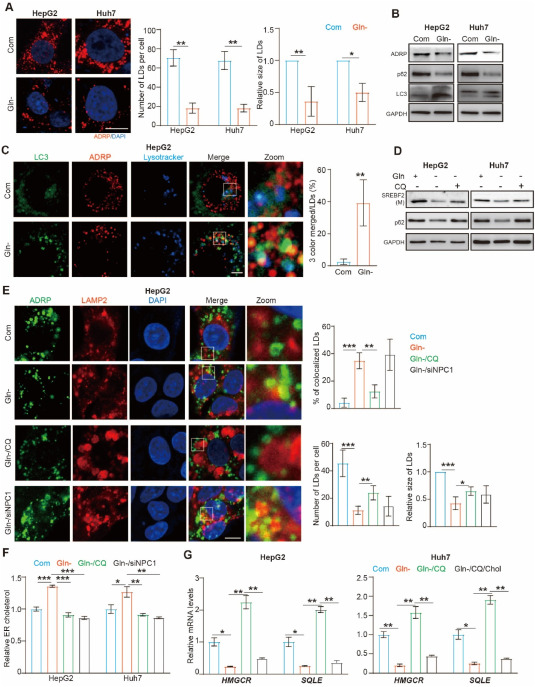
谷氨酰胺剥夺通过脂肪吞噬作用抑制胆固醇合成
抑制mTORC1活性可促进脂肪吞噬,氨基酸饥饿可降低mTORC1活性。因此,研究人员研究了mTORC1是否调节谷氨酰胺剥夺下的脂噬和胆固醇合成。总的来说,mTORC1信号在谷氨酰胺剥夺诱导的脂肪吞噬和胆固醇合成抑制中起到一定作用。
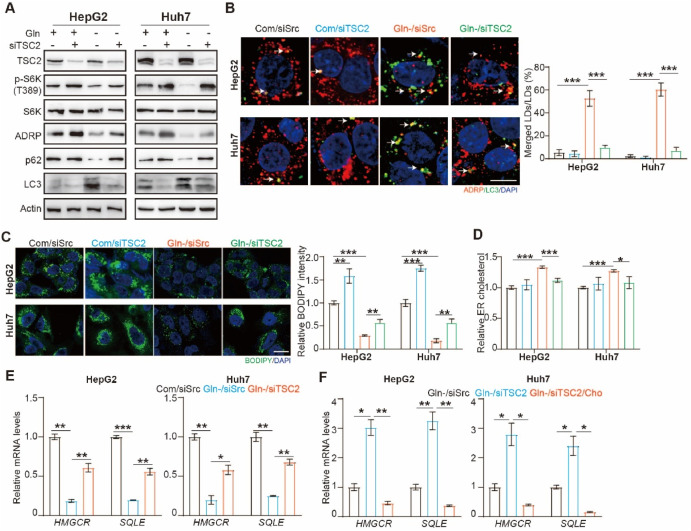
mTORC1 的激活可逆转谷氨酰胺剥夺诱导的脂肪吞噬和胆固醇合成抑制
鉴于研究结果表明谷氨酰胺剥夺抑制胆固醇合成,研究人员下一步研究阻断胆固醇合成抑制对细胞增殖的影响。数据表明,阻断胆固醇合成抑制使gpna治疗诱导的肿瘤体积大为减少。
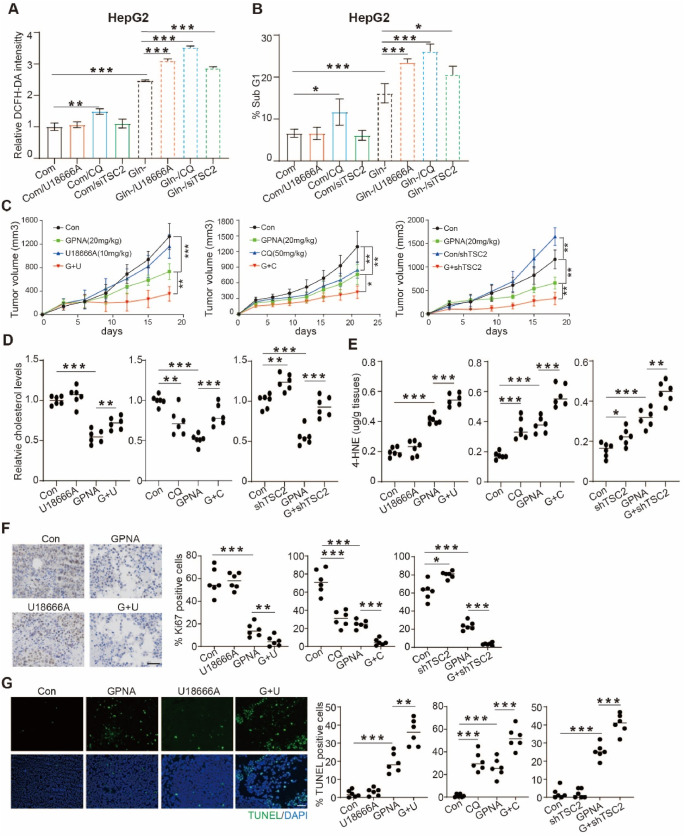
阻断胆固醇合成抑制进一步增强了 GPNA 诱导的肿瘤生长抑制
为了验证胆固醇合成与谷氨酰胺利用在人肝癌中的关联,研究人员用免疫组化方法检测了SREBF2、GLS和SLC1A5在肝癌组织中的表达。
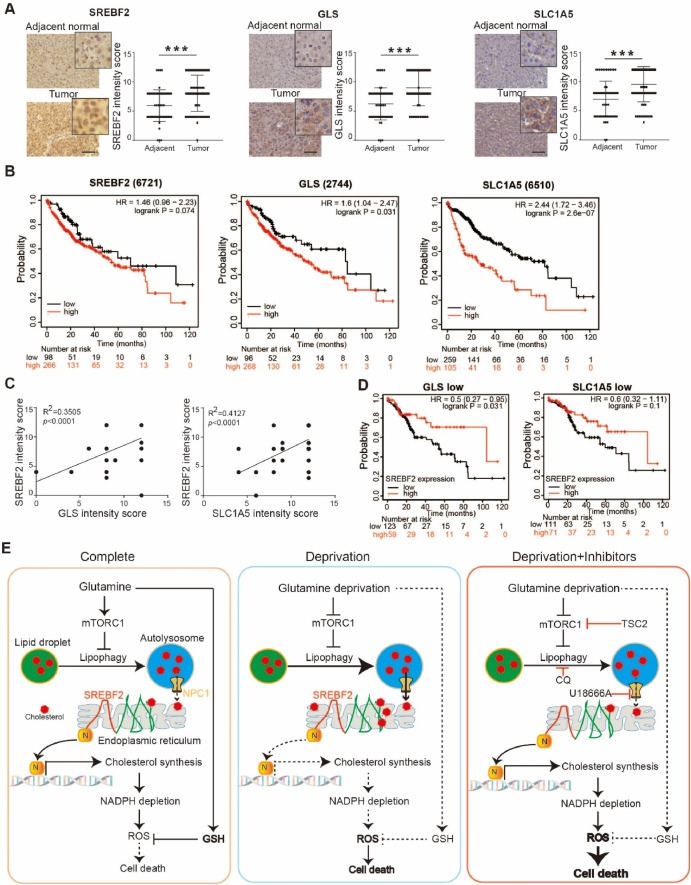
SREBF2 与人类 HCC 标本中的 GLS 或 SLC1A5 高度相关
总的来说,这些临床样本分析提供了强有力的证据,证实在谷氨酰胺缺失的肿瘤微环境下,胆固醇合成在HCC受到抑制。
研究意义
03
总之,本研究揭示了胆固醇合成抑制促成了谷氨酰胺剥夺下HCC细胞的存活。由于胆固醇合成需要消耗大量NADPH,维持氧化还原平衡和防止脂质过氧化在这一过程中发挥了一定作用。本研究确定了HCC适应谷氨酰胺限制微环境的新机制,为谷氨酰胺限制在肝癌临床治疗上的应用提供了新的应用策略。(转化医学网360zhyx.com)
参考资料:
https://www.sciencedirect.com/science/article/pii/S2213231723001337?via%3Dihub
注:本文旨在介绍医学研究进展,不能作为治疗方案参考。如需获得健康指导,请至正规医院就诊。
 腾讯登录
腾讯登录









还没有人评论,赶快抢个沙发