突破瓶颈!复旦大学等合作发文:发现胃癌晚期患者潜在治疗新策略
| 导读 | 治疗耐药是晚期胃癌治疗中的瓶颈。铁依赖性细胞死亡形式——铁死亡与抗癌治疗的疗效相关。需要进一步的研究来阐明其潜在的机制。 |
5月20日,复旦大学与非编码RNA基础与临床转化安徽省重点实验室以及皖南医学院第一附属医院(弋矶山医院)合作在期刊《Nature Communications》上发表了题为“Targeting SOX13 inhibits assembly of respiratory chain supercomplexes to overcome ferroptosis resistance in gastric cancer”的研究论文,在本工作中,基于之前在肿瘤代谢方面的研究,研究人员提出了一种潜在的导致铁死亡、化疗和免疫治疗耐药的代谢机制。研究人员证明靶向SOX13/SCAF1可抑制呼吸链超复合物(SCs)的装配,从而克服铁死亡介导的胃癌抗癌治疗耐药。

https://www.nature.com/articles/s41467-024-48307-z#Sec10
研究背景
01
胃癌(GC)在全球范围内是第五大常见癌症,也是第四大导致癌症相关死亡的病因。尽管在胃癌管理方面取得了巨大进步,但晚期胃癌患者的预后仍然不佳。基于顺铂的化疗仍然是晚期或辅助性胃癌的首选疗法,但对化疗耐药的认识仍然是影响临床疗效的一个障碍。癌症免疫疗法,包括免疫检查点抑制剂,在多种癌症中显示出有效的治疗效果。然而,由于耐药性,只有一小部分(约15%)胃癌患者对免疫疗法有反应。因此,应该进行更多的研究以阐明化疗和免疫耐药的机制。
铁死亡被认为是一种普遍存在的非凋亡细胞死亡途径,由于异常代谢导致过度脂质过氧化。铁死亡与多种抗癌疗法的疗效有关,包括放疗、化疗、靶向疗法和免疫疗法。埃拉斯汀是一种强效的系统Xc-抑制剂,RSL3是典型的GPX4抑制剂。它们作用于不同的内源性铁死亡抑制系统,因此选择它们进行后续实验。代谢重编程是癌症的标志性特征之一,可能是克服药物抵抗的潜在治疗策略。
研究进展
02
为了确定SOX13在铁死亡抵抗表型中的作用,研究人员敲低了SOX13的表达,然后检测细胞活力,脂质过氧化和丙二醛浓度。通过共转导抗性SOX13 cDNA (SOX13resis)可逆转SOX13敲低诱导的致敏效应。研究人员在786-O(人肾透明细胞癌)细胞系中验证了SOX13高表达与铁死亡抵抗之间的关系,该细胞系显示出对铁死亡诱导剂的高度敏感性。SOX13过表达的786-O细胞对铁死亡诱导性药物(包括埃拉斯汀和RSL3)的敏感性较低。大量研究表明铁死亡与顺铂的敏感性相关。研究人员还发现,与亲本细胞相比,rsl3耐药(RSL3resis) SNU-484细胞和埃拉斯汀耐药(erasinresis) SNU-668细胞对顺铂具有耐药性。敲低SOX13增加了RSL3resis SNU-484和erasinresis SNU-668细胞对顺铂的敏感性,这种敏感性被SOX13的抗性cDNA (SOX13resis)或铁死亡抑制剂Fer-1的共转导所逆转。为了便于将埃拉斯汀或RSL3耐药转化到临床,研究人员按照之前报道的程序建立了顺铂耐药(DDPresis) SNU-668细胞系,用于进一步的实验。大量研究表明,铁死亡参与了常用化疗药物5-FU和奥沙利铂的耐药。研究人员发现SOX13过表达降低了SNU-668细胞对5-FU和奥沙利铂的敏感性。
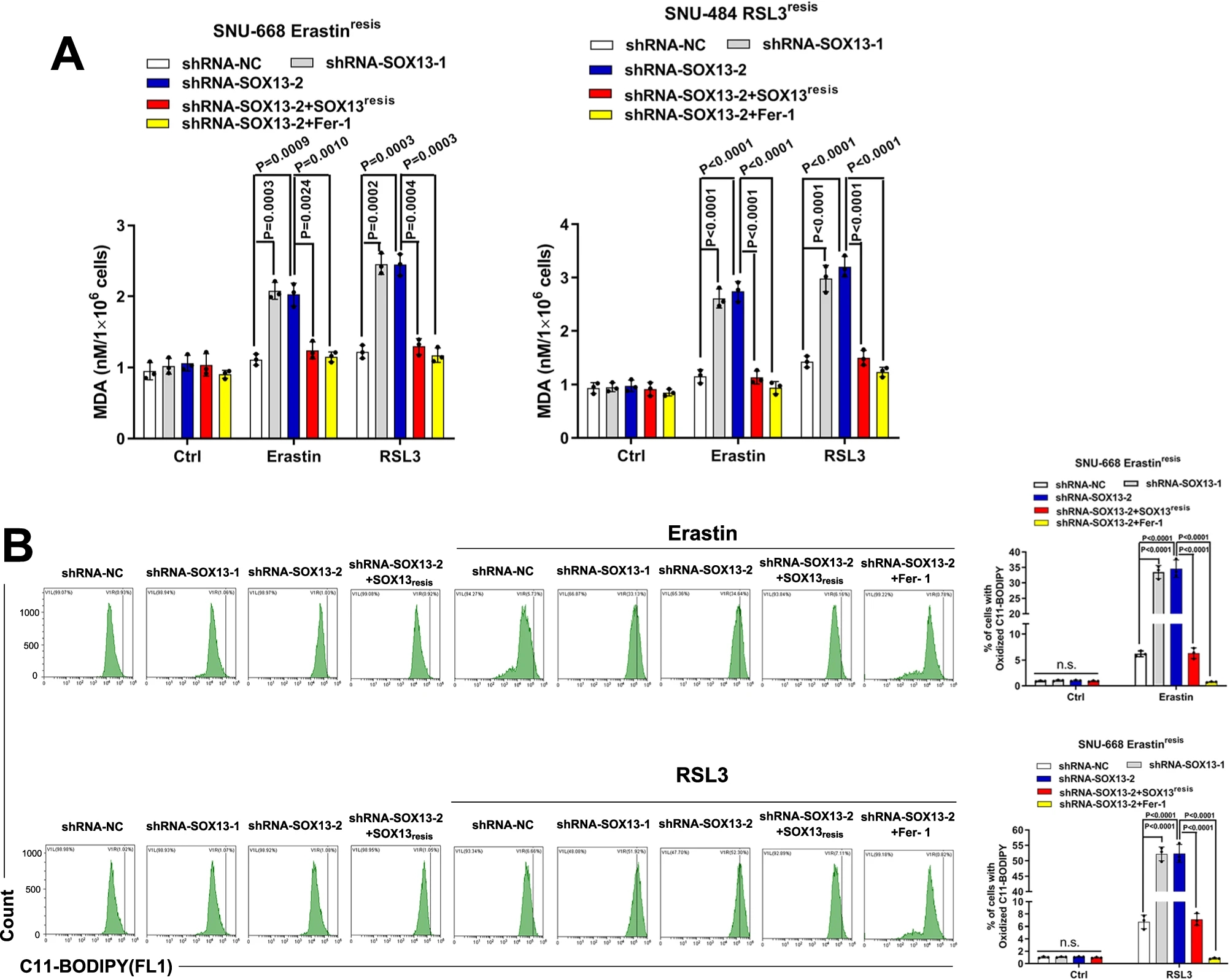
SOX13在抵抗铁死亡的胃癌中的依赖性
研究结论
03
综上所述,本研究报告了驱动FINs耐药的药理学靶向机制。SOX13直接靶向SCAF1并可能通过诱导NADPH的产生来抑制铁死亡,这是一种潜在的增加晚期胃癌患者化疗敏感性的治疗策略。(转化医学网360zhyx.com)
参考资料:
https://www.nature.com/articles/s41467-024-48307-z#Sec10
注:本文旨在介绍医学研究进展,不能作为治疗方案参考。如需获得健康指导,请至正规医院就诊。
 腾讯登录
腾讯登录









还没有人评论,赶快抢个沙发