【Cell子刊】中国药科大学等合作发现癌症免疫治疗新型策略
| 导读 | 免疫抑制性肿瘤微环境中肿瘤相关巨噬细胞(TAM)的高浸润显著削弱了免疫检查点阻断(ICB)疗法的疗效,但其潜在机制尚不完全清楚。 |
6月2日,中国药科大学杨勇、李娴静和复旦大学叶丹共同通讯在期刊《Cell Reports》上在线发表题为“Blockage of L2HGDH-mediated S-2HG catabolism orchestrates macrophage polarization to elicit antitumor immunity”的研究论文,研究发现揭示了S-2HG作为免疫代谢物的作用,为重编程TAM和提高现有ICB疗法的疗效提供了潜在的策略。

https://www.cell.com/cell-reports/fulltext/S2211-1247(24)00628-4
研究背景
01
免疫疗法,特别是免疫检查点阻断(ICB)疗法,在治疗恶性肿瘤方面取得了显著的临床成功。ICB疗法通过阻断免疫抑制受体(如PD-1和CTLA4)或配体(如PD-L1)发挥作用,从而调动抗肿瘤细胞毒性T细胞免疫。然而,目前的ICB疗法仅对一定比例的患者有效,限制了其广泛的疗效。最近,现有证据表明,肿瘤相关巨噬细胞(TAM)介导的免疫抑制的高度浸润极大地限制了ICB治疗的有效性。在许多肿瘤类型中,TAM的丰度与细胞毒性T细胞活性受损和不良临床结果相关。然而,在某些情况下,HLA-DR和CD86表达水平升高的CD169+巨噬细胞的存在与T细胞和有利的结果相关。现在很明显,TAM表现出连续的表型,从免疫刺激到免疫抑制。因此,确定控制巨噬细胞活化的关键因素可以加快癌症免疫治疗的进展。
越来越多证据表明,代谢途径正在成为巨噬细胞活化的关键调节因子。然而,TAM的代谢特征仍未完全表征,并且尚未实现代谢重新布线。为了深入了解代谢如何引导TAM状态,研究人员对代谢途径中分选的肿瘤浸润髓系细胞和外周血单核细胞之间的转录谱进行了比较分析。引人注目的是,研究人员观察到L-2-羟基戊二酸脱氢酶(L2HGDH)的高表达水平,这是一种代谢酶,用于对抗乳酸脱氢酶和苹果酸脱氢酶生成的S-2-羟基戊二酸(S-2HG,也称为L-2HG)在缺氧和酸性条件下对α-酮戊二酸(α-KG)的脱靶效应,在TAM中。手性代谢物2-HG已在其R-对映异构体(R-2HG,也称为D-2HG)中进行了广泛研究,该对映异构体在异柠檬酸脱氢酶(IDH)突变的肿瘤中表现出高积累,可作为肿瘤代谢物。最近,人们越来越关注肿瘤细胞的非自主作用。然而,对S-2HG的免疫功能以及L2HGDH介导的S-2HG分解代谢的潜在作用的关注仍然有限。
研究发现
02
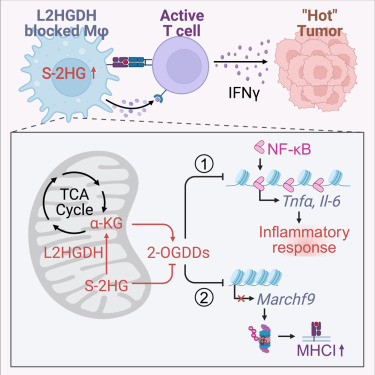
在研究中,研究人员研究了TAM的代谢特征,并将S-2-羟基戊二酸(S-2HG)鉴定为一种潜在的免疫代谢物,可将巨噬细胞塑造成抗肿瘤表型。L-2-羟基戊二酸脱氢酶(L2HGDH)介导的巨噬细胞中S-2HG分解代谢的阻断促进肿瘤消退。机制上,基于其与α-酮戊二酸(α-KG)的结构相似性,S-2HG有可能阻断2-氧戊二酸依赖性双加氧酶(2-OGDDs)的酶活性,从而重塑染色质的可及性。此外,S-2HG处理的巨噬细胞增强了CD8+ T细胞介导的抗肿瘤活性和对抗PD-1治疗的敏感性。总体而言,研究揭示了阻断L2HGDH介导的S-2HG分解代谢在协调巨噬细胞抗肿瘤极化中的作用,并进一步提供了S-2HG重极化巨噬细胞以克服对抗PD-1治疗耐药性的潜力。
研究结论
03
综上所述,研究发现揭示了S-2HG作为免疫代谢物的作用,为重编程TAM和提高现有ICB疗法的疗效提供了潜在的策略。(转化医学网360zhyx.com)
参考资料:
https://www.cell.com/cell-reports/fulltext/S2211-1247(24)00628-4
注:本文旨在介绍医学研究进展,不能作为治疗方案参考。如需获得健康指导,请至正规医院就诊。
 腾讯登录
腾讯登录









还没有人评论,赶快抢个沙发