【JECCR】中国医科大学赵明芳团队:发现肺癌精准治疗潜在靶点
| 导读 | 非小细胞肺癌(NSCLC)在世界范围内具有发病率高、预后差的特点。深入了解非小细胞肺癌的发病机制,寻找新的治疗靶点,对改善非小细胞肺癌的预后至关重要。 |
8月1日,中国医科大学赵明芳研究团队在期刊《Journal of Experimental & Clinical Cancer Research》上发表了研究论文,题为“FGL1: a novel biomarker and target for non-small cell lung cancer, promoting tumor progression and metastasis through KDM4A/STAT3 transcription mechanism”,在这项研究中,研究人员发现纤维蛋白原样蛋白1 (FGL1)促进非小细胞肺癌细胞的增殖、迁移和侵袭。在机制上,研究人员发现Stat3作为一种转录因子,可以被募集到FGL1启动子上,增强FGL1启动子的活性。赖氨酸特异性去甲基化酶4A (KDM4A)与Stat3相互作用,促进甲基从H3K9me3中去除,从而增强Stat3介导的FGL1转录。此外,研究人员观察到Stat3和KDM4A部分通过上调FGL1的表达来促进NSCLC细胞的增殖、迁移和侵袭。另外,FGL1在癌组织(n = 90)中的表达明显高于癌旁非癌组织(n = 90)。而且,与FGL1低表达的患者相比,FGL1高表达的患者总生存期(OS)更短。这些发现提示FGL1表达的动态变化可以作为预测非小细胞肺癌治疗效果的潜在生物标志物。总之,本研究揭示了FGL1在非小细胞肺癌发生发展中的重要作用及其调控机制,提示其可能成为非小细胞肺癌患者的治疗靶点。

https://jeccr.biomedcentral.com/articles/10.1186/s13046-024-03140-6#Sec10
背景知识
01
肺癌在所有恶性肿瘤中的死亡率排名第一,约占所有癌症相关死亡病例的21%。根据其组织病理类型,肺癌可分为小细胞肺癌(SCLC)和非小细胞肺癌(NSCLC),其中后者约占所有病例的85%。尽管诊断方法有了显著进步,但相当一部分患者在晚期才被诊断出来,失去了手术机会。近年来,治疗模式的进步,特别是酪氨酸激酶抑制剂(TKIs)和免疫检查点抑制剂(ICIs)的引入,显著提高了晚期肺癌患者的生存率。然而,靶向治疗和免疫治疗的疗效仅限于特定人群。此外,不可避免地会出现药物耐药性,导致治疗失败。因此,探索新的治疗靶点仍然是未来努力的关键方向。
2019年,研究人员在Cell上发表了一项研究,强调了纤维蛋白原样蛋白1 (FGL1)作为一种新型免疫检查点的作用,它以受体-配体的方式抑制T细胞活性,可能调节对PD-1/PD-L1治疗的耐药性。同时靶向PD-L1和FGL1可增强肺癌患者的免疫应答和抗癌作用,FGL1作为一种新的免疫治疗靶点,有望成为预测PD-1/PD-L1治疗疗效的生物标志物。除了免疫抑制作用,FGL1还影响肿瘤过程,如上皮-间质转化(EMT)、增殖和耐药性。然而,FGL1更广泛的生物学功能及其在非小细胞肺癌中的作用尚未完全阐明。因此,FGL1在NSCLC中的生物学功能有待进一步研究。以往关于FGL1在肿瘤组织中异常表达的研究表明,IL6/Stat3信号通路、YY1、HNF1a等因素可能影响FGL1的转录。为了阐明FGL1在NSCLC中异常表达的原因,需要进一步研究FGL1的上游调控机制。
FGL1敲低抑制NSCLC的增殖和转移
02
研究人员通过表型实验来阐明FGL1对NSCLC细胞恶性行为的影响。在NSCLC细胞系中,研究人员发现A549和H1975细胞FGL1水平差异最大。因此,以A549和H1975细胞为实验模型,建立了稳定的FGL1沉默细胞系。采用MTS法和集落形成法评价了FGL1对NSCLC细胞增殖能力的影响。抑制FGL1表达可减少菌落形成,显著抑制增殖能力。随后研究人员对A549和H1975细胞进行迁移实验,发现抑制FGL1表达可抑制细胞迁移和侵袭。相反,FGL1在H1299细胞中的过表达增强了NSCLC细胞的增殖、迁移和侵袭。
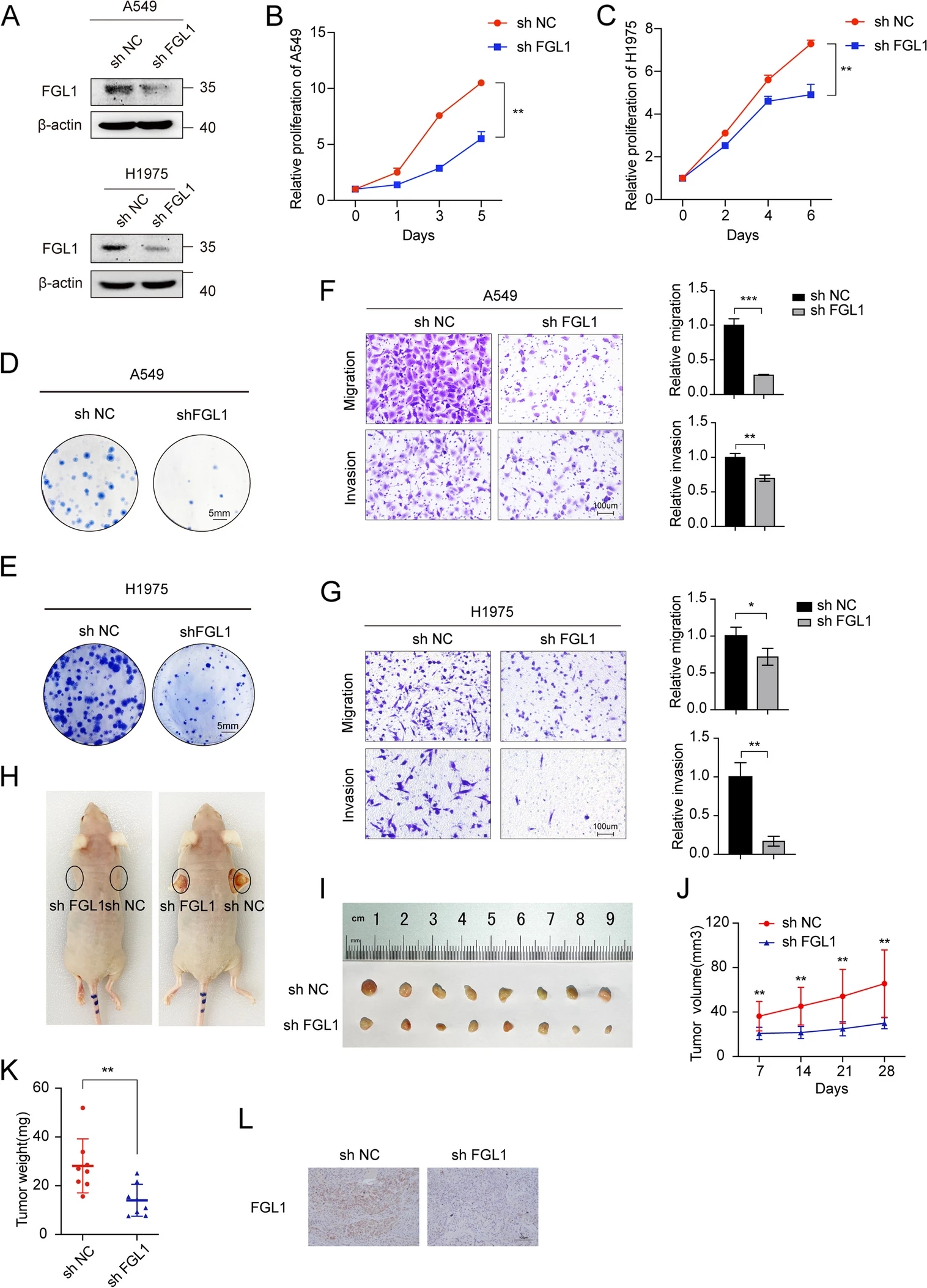
FGL1敲低抑制NSCLC的增殖和转移
为探讨FGL1在体内的作用,研究人员将携带sh FGL1的慢病毒感染A549细胞建立异位异种移植瘤模型,并将其作为阴性对照慢病毒(sh NC)。这些结果表明,与对照组相比,FGL1敲低组的肿瘤生长显著下降。因此,FGL1通过促进肿瘤细胞的增殖和转移促进NSCLC的进展。FGL1可作为NSCLC新的治疗靶点和预测疗效的生物标志物,具有良好的临床应用潜力。
FGL1可预测NSCLC的疗效
03
研究人员收集了65例局部晚期或转移性NSCLC患者的外周血样本。患者的基线特征见表3。所有患者均接受标准一线ICI治疗,每2个周期进行1次疗效评估。非疾病进展(Non-PD)包括CR、PR和SD患者。共有42例患者采集了2次及以上的外周血标本。截至2024年1月31日,32例患者仍处于非PD状态,10例患者出现疾病进展(PD)。研究人员从外周血中提取CTCss并进行免疫荧光染色。结果显示,所有患者外周血CTCs中均可检测到FGL1。与基线相比,非PD组患者CTCs的FGL1表达显著降低。另一方面,与基线相比,PD组患者CTCs中FGL1的表达显著增加。更重要的是,研究人员发现随着治疗的进展,非PD组中FGL1的表达逐渐降低。相反,在PD组中,随着疾病的进展,患者的FGL1水平显著高于基线和2个周期的时间点。影像学结果显示,患者1接受以替雷利珠单抗为基础的一线治疗,治疗期间获得良好反应。随着FGL1+ CTCs比例的下降,患者的肿瘤评估显示为PR (PFS = 10.3个月)。而接受替雷利珠单抗一线治疗的患者2在治疗期间FGL1+ CTCs比例升高。肿瘤评估提示PD (PFS = 0.9个月)。患者3接受基于信迪利单抗一线治疗2个周期后,FGL1+ CTCs比例下降,肺部病灶减少。随后,FGL1+ CTCs比例增加,导致PD的肿瘤评估(PFS = 6.8个月)。此外,研究人员发现在CTCs中,KDM4A或Stat3的表达与FGL1呈正相关。FGL1与NSCLC预后密切相关,可作为预测NSCLC治疗后进展的生物标志物。
研究小结
04
综上所述,本研究结果表明FGL1在NSCLC组织中异常高表达,促进了NSCLC细胞的恶性行为。组蛋白去甲基化酶KDM4A作为Stat3信号通路的新型共激活因子,激活FGL1启动子,增加FGL1和其他Stat3靶基因的表达。CTCs上FGL1的表达可无创、实时监测NSCLC的疗效和预后,有望成为NSCLC精准治疗的潜在靶点。综上所述,本研究结果为开发新的靶向FGL1的NSCLC治疗策略提供了强有力的理论基础。(转化医学网360zhyx.com)
参考资料:
https://jeccr.biomedcentral.com/articles/10.1186/s13046-024-03140-6#Sec10
【关于投稿】
转化医学网(360zhyx.com)是转化医学核心门户,旨在推动基础研究、临床诊疗和产业的发展,核心内容涵盖组学、检验、免疫、肿瘤、心血管、糖尿病等。如您有最新的研究内容发表,欢迎联系我们进行免费报道(公众号菜单栏-在线客服联系),我们的理念:内容创造价值,转化铸就未来!
转化医学网(360zhyx.com)发布的文章旨在介绍前沿医学研究进展,不能作为治疗方案使用;如需获得健康指导,请至正规医院就诊。
 腾讯登录
腾讯登录









还没有人评论,赶快抢个沙发