重要致癌因子!温州医科大学苏志鹏团队:发现胶质瘤患者治疗新策略
| 导读 | 通过对生存超过3年的胶质母细胞瘤(GB)患者与生存不到1年的患者的肿瘤组织进行蛋白质组学分析,研究人员发现生存时间较短的患者SelK显著上调。因此,研究人员推测SelK可能是与GBM发生发展相关的重要指标。 |
8月19日,温州医科大学苏志鹏研究团队在期刊《Journal of Experimental & Clinical Cancer Research》上发表了研究论文,题为“SelK promotes glioblastoma cell proliferation by inhibiting β-TrCP1 mediated ubiquitin-dependent degradation of CDK4”,本研究中,研究人员发现与长期存活者(≥3年)相比,SelK在短期存活者(≤1年)的GB样本中显著上调,且其表达水平与临床预后呈负相关。抑制SelK表达降低裸鼠GB细胞活力,诱导G0/G1期阻滞,损害移植胶质瘤细胞的生长。Selk诱导的内质网应激下调导致SKP2表达降低,β-TrCP1表达上调。上调β-TrCP1,从而加速泛素依赖性CDK4的降解,最终抑制GB细胞的恶性增殖。

https://jeccr.biomedcentral.com/articles/10.1186/s13046-024-03157-x#Sec13
背景知识
01
胶质母细胞瘤(GB)是中枢神经系统最致命、最顽固的恶性实体肿瘤之一。尽管外科、药物和放疗治疗取得了进展,但GB患者的预后仍然极差,中位生存期为14.6个月,1、2、3和5年生存率分别仅为39.3%、16.9%、9.9%和5.5%。少数存活≥3年的GB患者被称为长期生存者(long-term survivors, LTS)。在研究当前治疗产生持久疗效的能力的决定因素时,这一患者群体仍然很重要。
靶向治疗正在成为改善GB患者预后的可行治疗选择。研究表明,贝伐珠单抗(VEGF抑制剂)和达可替尼(EGFR抑制剂)在临床实践中显示出前景。然而,GB是一种高度异质性的肿瘤,单靶点治疗的疗效有限。因此,识别多个靶点,采用多模式联合治疗是GB治疗的未来。因此,迫切需要探索靶向肿瘤细胞的新的、高度特异的治疗靶点,以提高当前治疗的敏感性,为GB患者的长期获益提供更多希望。
肿瘤细胞的恶性增殖是对患者健康产生负面影响的关键因素。尽管研究取得了进展,发现了许多基因和蛋白质的异常,但信号转导通路的失调和细胞周期控制的丧失仍然是GB的突出问题。多项研究表明,减小肿瘤组织体积和抑制肿瘤细胞增殖既可以缓解神经症状,又可以优化放化疗的疗效。
SelK在人GB细胞株中表达上调,敲低SelK表达可抑制GB细胞的生长
02
研究人员通过蛋白质免疫印迹实验检测了SelK在人正常星形胶质细胞(NHA)和不同人GB细胞系中的表达,探讨了SelK在GB发育中的潜在作用。SelK在人GB细胞株中的表达高于NHA细胞。研究人员通过光密度分析进一步证实了SelK的表达水平明显升高,尤其是在LN229和U251细胞株中。随后,在LN229和U251细胞中使用shRNA敲低SelK,构建稳定敲低SelK的细胞株。研究人员还通过蛋白质免疫印迹实验验证了敲低效果,并选择shSelK#1和shSelK#2来研究SelK在GB发育中的作用。通过ATP实验、软琼脂实验、平板克隆形成实验和EdU实验评估SelK对细胞增殖和肿瘤生长的潜在作用。结果表明,敲低SelK可显著抑制GB细胞的恶性增殖能力。实验结果还表明,SelK过表达显著促进GB细胞的恶性增殖。这些结果表明,SelK可能在GB细胞的体外发育中发挥关键作用。
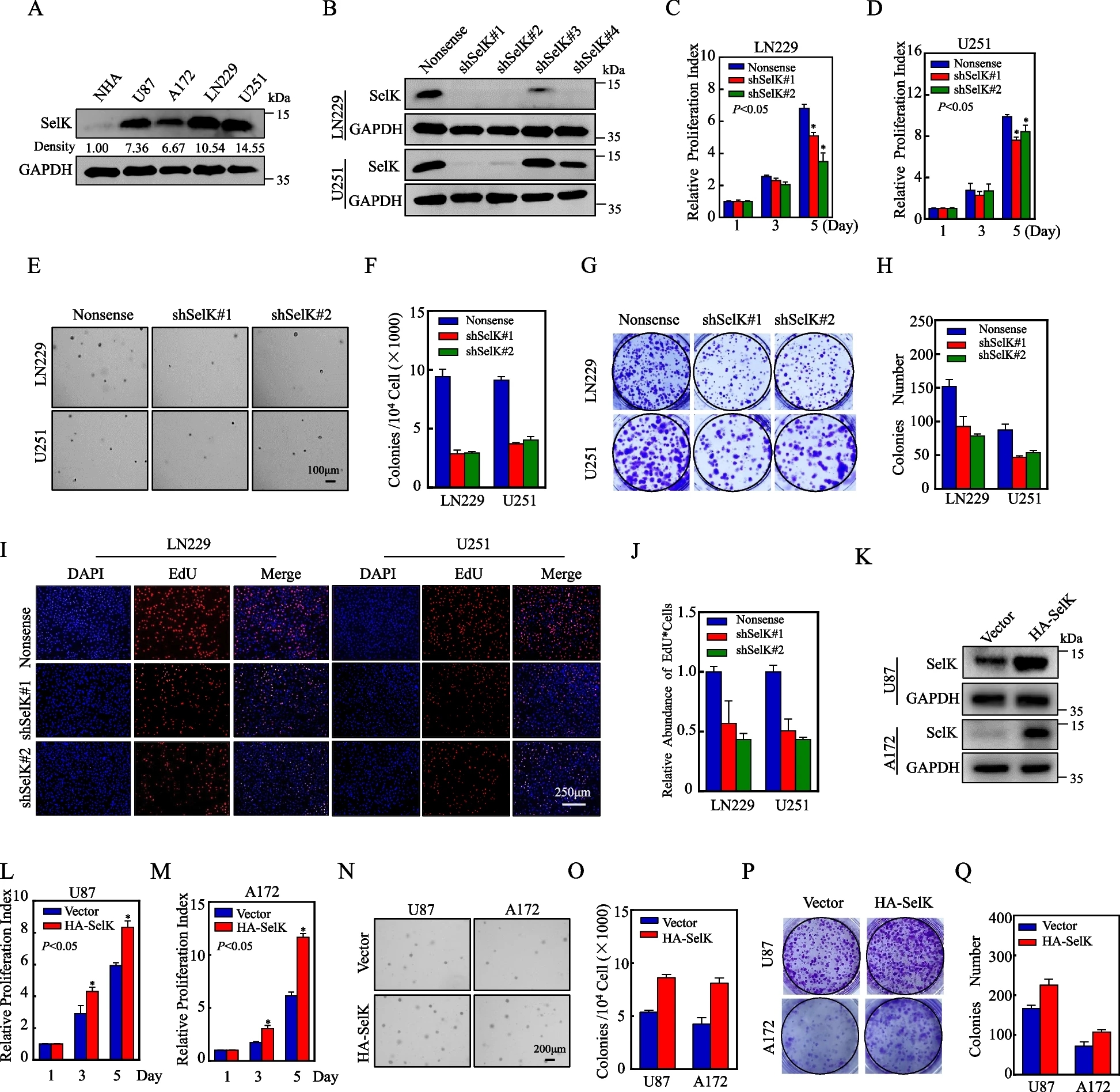
SelK在人GB细胞株中表达上调,敲低SelK表达可抑制GB细胞的生长
敲低SelK显著抑制体内胶质母细胞瘤细胞的恶性增殖能力
03
为了评估SelK对GB体内增殖能力的影响,研究人员将SelK敲低细胞LN229、U251或非义控制细胞通过皮下注射注入BALB/c-裸鼠体内,建立异种移植肿瘤模型。28天后,评估小鼠及其肿瘤的生长和体积。分析表明,体内敲低SelK显著抑制了LN229和U251细胞的增殖能力,表现为肿瘤体积和重量的减少。同时分析肿瘤中增殖标记物Ki67(IHC)的蛋白表达水平,研究人员发现来自SelK敲低细胞的肿瘤组织中SelK和Ki67的蛋白表达水平显著降低。这些结果表明,体内敲低SelK可能抑制GB细胞的增殖能力。
上调SKP2表达并促进SKP2介导的β-TrCP1泛素化
04
上述结果表明,β-TrCP1在GB细胞的生长中起着关键作用,在SelK的影响下,它是CDK4的关键调节因子。此外,定量PCR分析显示,SelK主要在蛋白质水平上调节β-TrCP1,因为在敲除SelK的GB细胞中,β-TrCP1的转录水平没有明显变化。
为了进一步探究SelK对GB细胞生长进程的影响,研究人员进行了蛋白质降解实验,以评估SelK对β-TrCP1稳定性的影响。实验结果表明,与对照组细胞相比,SelK敲除细胞中的β-TrCP1更稳定,这表明SelK抑制了β-TrCP1的降解速率。研究人员还评估了SelK敲除GB细胞中SKP2和SMURF2的表达。数据显示,SMURF2蛋白水平没有明显变化,而SKP2水平在上述细胞中持续下调。因此,这些数据表明SelK可能通过增加SKP2蛋白水平和降低β-TrCP1表达来促进CDK4蛋白表达。
为了研究SKP2与β-TrCP1之间的相互作用,并确定SelK介导的SKP2调节是否影响恶性GB细胞的增殖,在LN229细胞和稳定细胞系中过表达SKP2。有趣的是,在SKP2过表达的SelK敲除细胞中,β-TrCP1蛋白水平降低。进一步分析显示,与对照细胞相比,SKP2过表达导致LN229细胞的增殖增加,无论是在ATP或软琼脂培养基中均是如此。蛋白质降解实验表明,在SelK敲除和SKP2过表达的细胞中,β-TrCP1蛋白降解速度高于对照细胞。此外,蛋白质降解实验还表明,在SelK敲除和SKP2过表达的细胞中,CDK4比对照细胞更稳定。综上所述,这些结果共同表明,SelK通过增加SKP2的蛋白质水平来增强β-TrCP1的泛素化,导致β-TrCP1蛋白表达降低和CDK4蛋白表达增加,最终促进GB细胞增殖。
研究小结
05
总之,本研究证明了SelK/内质网应激/SKP2/β-TrCP1/CDK4轴在GB增殖中的重要作用。从这些发现来看,可以清楚地看出SelK是GB细胞发育和/或维持过程中的一个重要致癌分子。因此,开发能够靶向SelK及其下游效应物的小分子抑制剂或激动剂,可能会有助于指导GB患者的治疗策略。(转化医学网360zhyx.com)
【参考资料】
https://jeccr.biomedcentral.com/articles/10.1186/s13046-024-03157-x#Sec13
【关于投稿】
转化医学网(360zhyx.com)是转化医学核心门户,旨在推动基础研究、临床诊疗和产业的发展,核心内容涵盖组学、检验、免疫、肿瘤、心血管、糖尿病等。如您有最新的研究内容发表,欢迎联系我们进行免费报道(公众号菜单栏-在线客服联系),我们的理念:内容创造价值,转化铸就未来!
转化医学网(360zhyx.com)发布的文章旨在介绍前沿医学研究进展,不能作为治疗方案使用;如需获得健康指导,请至正规医院就诊。
 腾讯登录
腾讯登录









还没有人评论,赶快抢个沙发