心肌再灌注损伤治疗新希望:瑞金医院发现脾IRF7纳米治疗靶点
| 导读 | 在这项研究中,研究人员通过开辟另一条途径,将纳米药物重新定向到脾脏,利用其作为远程调节或远程调节心肌再灌注损伤的高效和靶向部位的潜力,重振心血管纳米疗法。 |
2025年2月24日,上海交通大学医学院附属瑞金医院和丹麦赫尔辛基大学的研究团队在期刊《Nature Communications》上合作发表了题为“Identification of splenic IRF7 as a nanotherapy target for tele-conditioning myocardial reperfusion injury”的研究论文。

https://www.nature.com/articles/s41467-025-57048-6
在这项研究中,研究人员通过开辟另一条途径,将纳米药物重新定向到脾脏,利用其作为远程调节或远程调节心肌再灌注损伤的高效和靶向部位的潜力,重振心血管纳米疗法。
研究结果揭示了脾脏在心肌再灌注损伤中的远程调节作用,特别是IRF7作为关键靶点的发现,以及通过纳米技术实现精准干预的创新策略。
01
研究背景
以前的研究,包括团队自己的研究,都试图利用免疫细胞作为天然载体,渗透和定位到病变部位的内在能力,来促进NPs的心脏滋养功能。在所有白细胞中,作为潜在 “靶框架 ”的单核细胞因其高流动性、先天性吞噬倾向和广泛参与免疫反应调节而受到越来越多的关注。然而,循环中单核细胞的数量是高度动态的,仅占血液白细胞总数的2-8%。此外,驻留在MPS或单核细胞储库中的单核细胞数量超过其在血液池中的同等数量,并且在受到创伤性挑战时不断被激活和动员。这些特点加上MPS对NPs的自发封存,使MPS成为最大限度发挥单核细胞靶向纳米疗法治疗潜力的有利替代功能位点。然而,要利用这种策略,需要解决两个基本问题。虽然之前的研究已经确定脾脏是急性心肌梗死(MI)时的主要单核细胞库,但对心肌缺血再灌注(IR)的研究相对较少,而IR与心肌梗死的病理和生物学特征截然不同。其次,单纯采用 “抗炎 ”概念的广泛治疗策略对心肌缺血再灌注的治疗效果不佳;因此,进一步了解如何有选择性地针对破坏性因素,同时保持有益的免疫平衡,可能会产生更有希望的结果。
02
STEER-HS38可改善心肌再灌注结果
研究人员测试了STEER-HS38对急性心脏损伤和心肌再灌注后左心室长期重构的治疗效果。STEER-HS38的单次预处理,减少了损伤心肌中巨噬细胞和中性粒细胞的浸润。相比之下,游离HS38处理组免疫细胞浸润的减少并不明显。再灌注后24小时,STEER-HS38治疗组的左心室梗死面积减小至19.3±3.7%,与游离HS38(28.7±4.0%)或未治疗组(27.2±3.4%)相比显著降低。这一发现表明,STEER-HS38导致的心肌坏死和凋亡较少。参与炎症的关键基因,包括趋化因子(Ccl2、Ccl5、Ccl7、Ccl12、CXCL1、CXCL5、CXCL10、CXCL12、CXCR2和CXCR4)、促炎细胞因子(IL-1b、IL6、IL11和TNF)、细胞粘附分子(Icam1、Icam2和Vcam1)、纤维化进展(基质金属肽酶,MMPs;MMP9和MMP14)、类收费受体激活(TLR4、TLR7、TLR8、TLR9、Myd88、TRAF3和TRAF6),以及最重要的干扰素刺激基因(Isgs;ISGs;ISG15、Oasl1、Oasl2、Ifit1、Ifit2、Ifit3、Ifit203、Ifit204、Rsad2、IRF3、IRF5和IRF7)在STEER-HS38处理组中被下调,但这一现象在游离HS38处理组中并不明显。此外,STEER-HS38治疗后,损伤心肌中两种关键炎症因子IL-6和IFN-b的蛋白水平显著下降。这些结果表明,STEER-HS38治疗能有效降低急性期先天性免疫反应,其疗效超过了游离HS38。
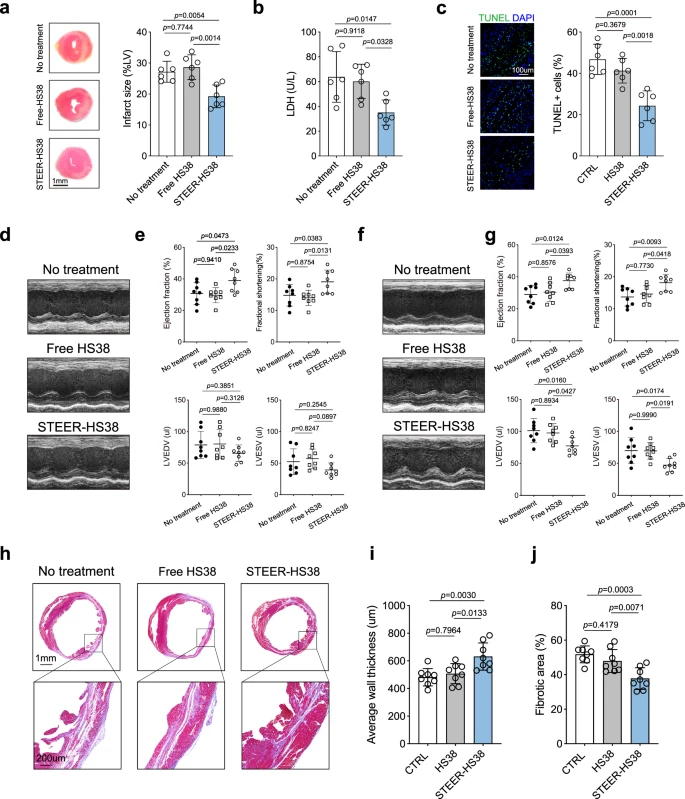
STEER-HS38可改善心肌再灌注效果。
03
总结
1. IRF7作为纳米治疗靶点的发现:
脾脏中特异性表达的IRF7通过动态、多效性的方式调节心肌IR损伤;
仅通过时间依赖性地抑制脾脏IRF7(而非全身性敲除)可以实现对心肌IR的长期保护,使其成为理想的纳米治疗靶点。
2. 纳米平台STEER-HS38的应用:
STEER-HS38通过抑制脾脏IRF7,显著减少了心肌细胞凋亡,并改善了心肌IR损伤的长期预后,包括心脏功能保留、纤维化减少和心脏重塑改善。
3. IRF7在炎症反应中的复杂作用:
IRF7在心肌IR损伤中表现出双峰模式,分别对应于急性炎症期和巨噬细胞表型转换期;
IRF7的抑制可以减少促炎介质的分泌,但也可能影响巨噬细胞从促炎表型(M1)向抗炎表型(M2)的转换,因此需要精确的时间干预以平衡炎症反应和组织修复。
4 纳米医学在心血管疾病中的潜力:
本研究证明了利用脾脏隔离的纳米药物可以重新用于远程调节心肌再灌注损伤,为纳米医学在心血管疾病中的应用开辟了新途径;
研究结果强调了纳米技术在精准靶向治疗中的优势,尤其是在传统靶向策略难以实现的复杂疾病中。
5. 临床转化的前景:
STEER-HS38纳米平台具有巨大的临床转化潜力,其设计简单、生物安全性高,且能实现对IRF7的精准抑制;
该研究为其他难以直接靶向的疾病提供了纳米医学设计的新思路,未来有望推广至更广泛的无菌性炎症疾病。
参考资料:
1.Smith, B. R. & Edelman, E. R. Nanomedicines for cardiovascular disease. Nat. Cardiovasc. Res. 2, 351–367 (2023).
2.Mitchell, M. J. et al. Engineering precision nanoparticles for drug delivery. Nat. Rev. Drug Discov. 20, 101–124 (2021).
 腾讯登录
腾讯登录









还没有人评论,赶快抢个沙发