Cancer Cell | 首个肝细胞癌中TLS的全景发育图谱!Stereo-seq助力肝癌研究再获新突破
| 导读 | Stereo-seq助力科研成果大爆发 |

近年来,精准靶向肿瘤的免疫激活策略成为癌症研究的前沿方向。三级淋巴结构(Tertiary Lymphoid Structures, TLS)作为肿瘤微环境中具有器官样结构的淋巴聚集体,其在肿瘤内的空间定位及功能表型与免疫治疗应答的相关性备受关注。临床研究表明,TLS 的存在与肿瘤患者接受免疫检查点抑制剂治疗后的预后改善显著相关,提示其作为预测性生物标志物的潜在价值。然而,传统组织病理学分类方法难以解析TLS在空间分布模式、细胞组成及分子特征上的复杂异质性,亟需整合空间组学技术揭示其在肿瘤免疫微环境中的功能调控机制。
近日,中山大学附属第一医院肝胆胰外科中心、精准医学研究院,中山大学中山医学院、华大生命科学研究院等团队,联合利用华大自主研发的高分辨率时空组学技术Stereo-seq,首次绘制出肝细胞癌中TLS的全景发育图谱。该研究不仅详细描绘了TLS在调控抗肿瘤免疫及免疫治疗反应中的独特特征,更首次揭示了色氨酸代谢在TLS成熟过程中的关键调控作用,为肝细胞癌及其它癌症的早期诊断和新型免疫治疗方案的开发提供重要参考。相关成果发表于国际学术期刊Cancer Cell。

文章页面截图
研究团队在肝细胞癌患者样本中实现了TLS的全面原位鉴定和精准注释,大幅提升了临床数据采集的效率。借助一套集成自动化鉴定流程,并结合TLS相关基因特征、空间共表达模式及免疫细胞簇的空间聚类方法,团队在肝细胞癌患者队列中共识别出937个TLS,其中成熟TLS的数量达69个。此前研究表明,成熟的TLS与多种实体瘤患者的预后改善及免疫治疗疗效的显著提高密切相关,而未成熟TLS的临床意义则仍存有争议。
基于高分辨率的空间细胞信息与分子信号,团队构建了一个基于发育轨迹的全新分类模型,将未成熟TLS进一步细分为“趋向成熟型”(预示未来有望成熟)和“偏离成熟型”(可能无法成熟)。同时,利用机器学习技术实现了对TLS状态的精准区分。后续分析表明,“趋向成熟型”TLS中T细胞功能通路显著激活,并与B细胞发生更紧密的相互作用,提示其在调控免疫治疗反应中发挥着关键作用,为优化免疫检查点抑制剂的临床应用提供了新思路。
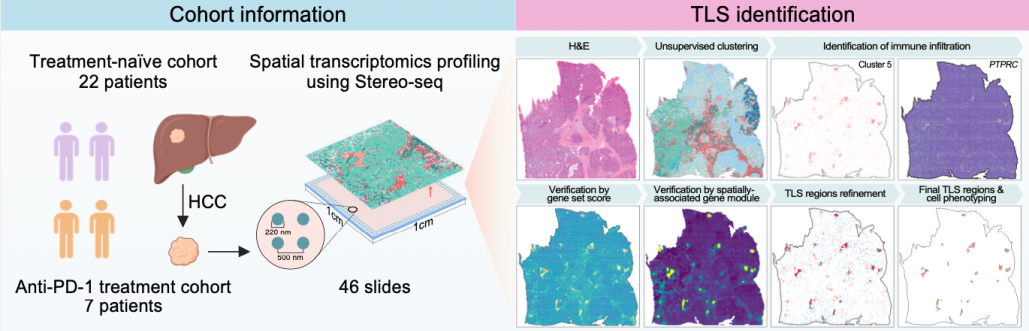
通过深入数据挖掘,研究团队发现肝癌细胞通过调控色氨酸代谢,显著影响TLS的成熟。数据显示,高TDO2(该基因编码的酶负责开启色氨酸的代谢过程)表达区域更易形成“偏离成熟型”TLS;而在不同TLS类型中,B细胞的色氨酸代谢活性存在明显差异,特别是在初始B细胞和生发中心B细胞中,“偏离成熟型”TLS呈现出色氨酸代谢活性显著的空间富集。
研究团队在小鼠肝细胞癌模型中进一步验证了这一发现:低色氨酸饮食不仅显著提升了成熟TLS的密度,还改善了肿瘤内的代谢环境。进一步分析结果显示,低色氨酸饮食或TDO2抑制剂均能够增加成熟TLS数量,并与抗PD-1免疫治疗产生协同效应,有效缩小肿瘤体积。这些发现强调了色氨酸代谢在决定TLS成熟命运及其对免疫治疗反应中的关键作用。

以上研究展现了Stereo-seq在肝癌研究中的巨大潜力。值得一提的是,早在2023年6月,研究人员便基于Stereo-seq,结合单细胞建库平台DNBelab C4,首次解析了肿瘤细胞侵袭正常肝细胞过程中交界线周围区域的细胞组成、分子特征及交互作用,精确定义了以肿瘤边界为中心500 μm宽的区域为肿瘤“侵袭前沿区”,在肿瘤侵袭与进展中发挥关键作用。该研究成果以封面形式发表于国际学术期刊Cell Research,为开发肝癌治疗新策略提供新见解。

除了在肝癌上的应用,Stereo-seq也在结直肠癌、乳腺癌、宫颈癌、糖尿病等高发疾病,以及生命发育、衰老再生、脑科学、植物研究等领域取得关键进展,并助力科研人员在Cell、Science、Nature、Cell Research等期刊上发表了120余篇研究文章,其中,IF大于10的文章占比达到63%。
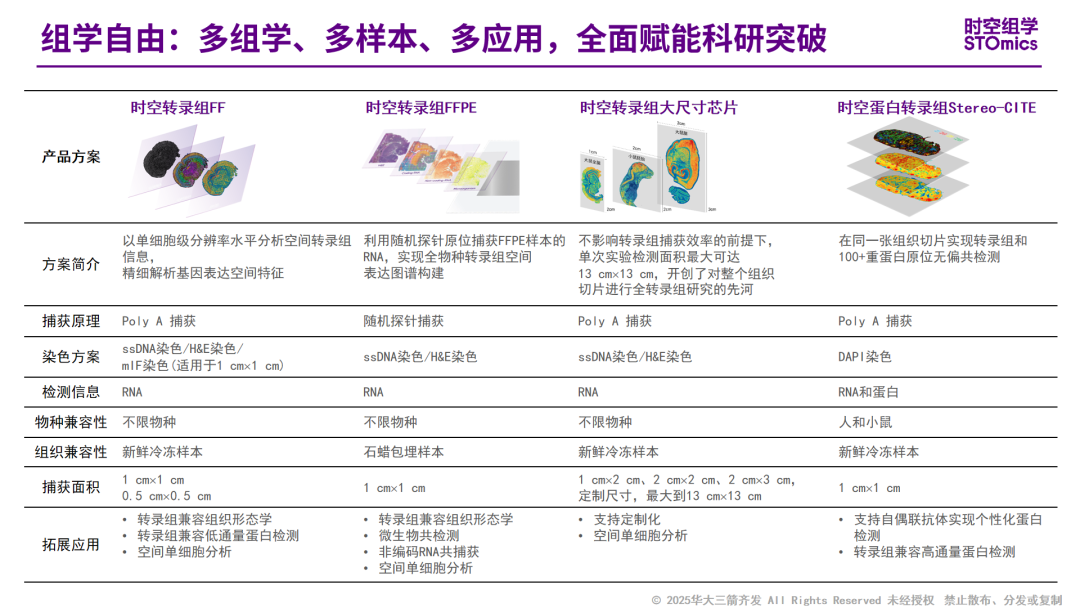
依托Stereo-seq,华大时空组学推出了适用于新鲜冷冻样本的时空转录组FF V1.3、适用于石蜡包埋样本的时空转录组FFPE、适用于大尺寸组织的时空转录组大尺寸芯片,以及时空蛋白转录组Stereo-CITE等产品解决方案,帮助科研人员进一步提升研究的广度与深度。

特别关注

其中,“肿瘤3D图谱创新研究计划”将利用Stereo-CITE/Stereo-FF技术对肿瘤新鲜样本进行肿瘤组织的3D重构,解析真实立体的肿瘤微环境特征,构建大规模肿瘤3D数据库;“肿瘤数字化病理大科学计划”将利用Stereo-FFPE技术对肿瘤的FFPE样本进行大人群队列的回顾性研究,聚焦具体的临床问题和科学研究方向。点击了解计划详情加码赋能!“肿瘤3D图谱创新研究和肿瘤数字化病理大科学计划”启动

对时空组学或细胞组学整体解决方案感兴趣的老师,可选择以下方式和我们联系,我们将及时为您进行详细的介绍:
1. 在公众号留言;
2. 发送信息至邮箱:
services@stomics.tech。
 腾讯登录
腾讯登录






还没有人评论,赶快抢个沙发