苏州大学附属第一医院联合苏州大学首次报道促进胃癌进展的分子机制
| 导读 | 导读:最近的研究表明,NDUFS1在人类癌症中具有重要作用; 然而,NDUFS1在胃癌(GC)中的作用尚不完全清楚。 |
近日,苏州大学附属第一医院联合苏州大学研究人员在学术期刊《British Journal of Cancer》上发表了学术论文,题为“Loss of NDUFS1 promotes gastric cancer progression by activating the mitochondrial ROS-HIF1α-FBLN5 signaling pathway”。该研究中,研究人员通过蛋白质印迹、免疫组织化学和生物信息学分析,证实了NDUFS1在胃癌细胞中表达下调。还通过CCK-8、克隆形成实验、体外Transwell实验和体内裸鼠移植瘤实验研究了NDUFS1对胃癌的影响,并通过共聚焦显微镜观察了NDUFS1的表达、亚细胞定位及线粒体活性氧(mROS)含量。研究结果表明,NDUFS1下调通过激活mROS-HIF1α-FBLN5信号通路促进GC进展。

https://www.nature.com/articles/s41416-023-02409-5#Sec31
研究背景
01
胃癌(GC)是第四大最常见的消化道恶性肿瘤,也是全球癌症相关死亡的第三大原因。2012年,有951,600例胃癌新发病例和723,100例胃癌相关死亡。在中国,胃癌是男性和女性发病率排名第二和第四的肿瘤,也是第二致命的癌症。手术仍被认为是最有效的治疗方法。然而,在诊断时,大多数胃癌患者表现为晚期癌症。胃癌转移,如腹膜转移、淋巴结转移和远处转移,是胃癌患者预后不良的关键因素。因此,揭示促进GC进展的分子机制具有重要意义。
线粒体是细胞的发电厂,产生三磷酸腺苷(ATP),为细胞的生命活动提供能量。它是一种重要的细胞应激传感器,通过产生活性氧(reactive oxygen species, ROS),减少小分子等代谢产物,调节细胞信号转导、细胞代谢等生物行为。线粒体功能障碍与许多疾病密切相关,包括癌症的产生和发展。NDUFS1是线粒体复合体I中最大的亚基,催化线粒体呼吸链内烟酰胺腺嘌呤二核苷酸(NADH)氧化的第一步,对维持线粒体复合体I的稳定性和功能具有核心作用。NDUFS1缺失或突变可降低线粒体复合体I的水平和催化活性,打破NADH的稳态。近期研究表明,NDUFS1在人肺癌和肾细胞癌中表达下调,与肿瘤分期、远处转移、预后不良密切相关。此外,其他研究建议使用NDUFS1作为诊断肾细胞癌的生物标志物。此外,通过CpG岛甲基化NDUFS1的表观遗传失活也被发现参与卵巢子宫内膜异位症的恶性转化。越来越多的证据表明,NDUFS1的改变可能对癌症的进展起关键作用。
研究过程及发现
02
线粒体功能障碍有助于肿瘤的发生和发展。因此,阐明癌细胞中线粒体异常的作用和机制可能有助于开发新的和有效的癌症治疗方法。最近的研究表明,NDUFS1在肺癌和肾癌中表达极低。在本研究中,研究人员进一步证实了之前的无偏见的iTRAQ分析。此外,有研究报道胃癌细胞表现出线粒体复合物I的缺乏和呼吸能力的下降,这在一定程度上支持了研究人员的发现。
生物学实验表明,在体外和裸鼠体内,NDUFS1的降低加速了胃癌细胞的增殖和转移,表明线粒体复合物I亚基NDUFS1是一个新的肿瘤抑制因子。值得注意的是,通过减少核心亚基NDUFS3或NDUFV1以及辅助亚基NUDFB9来抑制线粒体复合体I的活性可增强乳腺癌的侵袭潜能。观察到的现象与研究结论一致,NDUFS1的下调促进胃癌的进展。
研究人员假设NDUFS1的下调会通过激活mROS-HIF1α信号通路促进GC的进展。为了支持该假设,研究人员分析了NDUFS1对GC细胞中mROS水平以及HIF1α表达和转录活性的影响。正如预期的那样,NDUFS1的减少促进了GC细胞中mROS的产生和HIF1α的积累和核易位。因此,NDUFS1的减少增强了HIF1α的转录活性,上调了HIF1α下游基因如GLUT1和VEGFA的表达。这些数据表明,NDUFS1减少通过激活mROS-HIF1α信号通路促进GC进展。
HIF1α是促进血管生成的主要调控因子,在多种肿瘤中异常高表达,与肿瘤转移密切相关。本研究表明,下调GC细胞NDUFS1可激活HIF1α信号通路,从而上调VEGFA的表达。因此,研究NDUFS1表达水平与肿瘤血管生成的临床相关性以及雷莫芦单抗在GC患者中的临床疗效是值得的。也许NDUFS1可以作为GC患者对雷莫芦单抗敏感性的预测性生物标志物。
FBLN5作为细胞外基质蛋白纤维蛋白家族的一员,是一种重要的弹性纤维蛋白,广泛分布于富含弹性纤维的组织中。研究表明,FBLN5是HIF1α的转录靶点,缺氧通过依赖HIF1α的机制刺激FBLN5的表达。此外,缺氧和tgf - β可共同促进FBLN5的表达。NDUFS1下调通过上调mROS激活HIF1α信号通路刺激GC细胞FBLN5的表达。重要的是,FBLN5敲低和功能性过表达实验进一步验证了FBLN5是NDUFS1缺失引发的GC促进作用的关键介质。
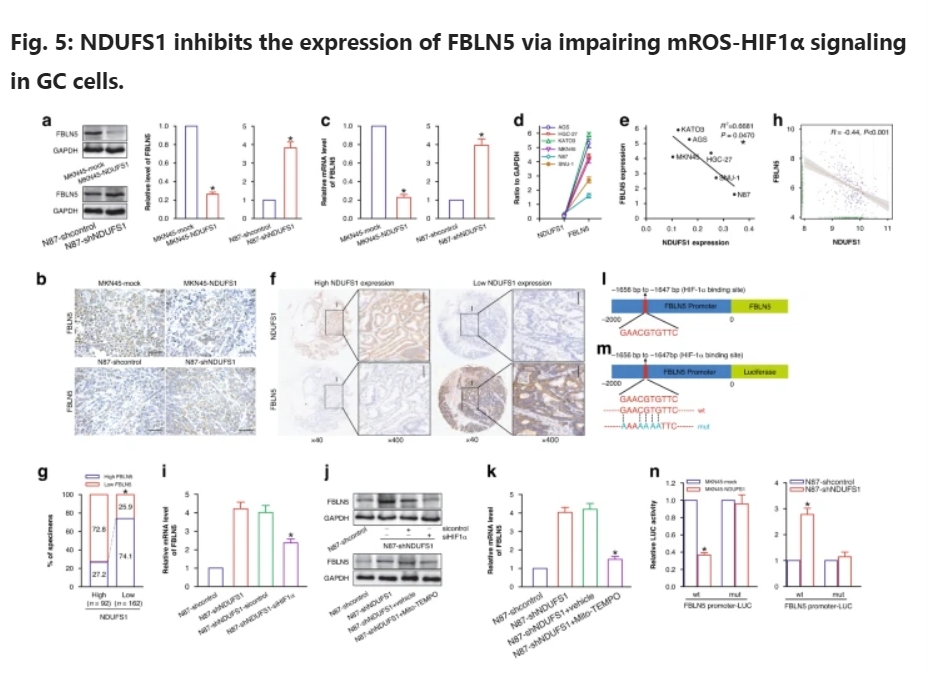
NDUFS1通过破坏GC细胞中mROS-HIF1α信号通路抑制FBLN5的表达
研究结论
03
总之,数据显示,线粒体复合体I亚基NDUFS1的下调通过激活mROS-HIF1α-FBLN5信号通路促进GC进展。FBLN5是NDUFS1还原引起的GC进展的重要介质。NDUFS1可能是一种新的肿瘤抑制因子和潜在的胃癌治疗靶点。(转化医学网360zhyx.com)
参考资料:
https://www.nature.com/articles/s41416-023-02409-5#Sec31
注:本文旨在介绍医学研究进展,不能作为治疗方案参考。如需获得健康指导,请至正规医院就诊。
 腾讯登录
腾讯登录
还没有人评论,赶快抢个沙发