【Cell Discov】上海交大研究团队发现胰腺癌化疗耐药的潜在新机制
| 导读 | 导读:Notch信号通路在胰腺癌细胞中广泛激活,与胰腺癌的发生、化疗耐药和复发密切相关。靶向该通路是一种有前景的胰腺癌治疗策略;然而,目前报道的成功方法很少,目前使用的该通路的分子抑制剂显示出有限的临床获益。 |
9月15日,上海交通大学研究团队在期刊《Cell Discovery》上发表了题为“A microprotein N1DARP encoded by LINC00261 promotes Notch1 intracellular domain (N1ICD) degradation via disrupting USP10-N1ICD interaction to inhibit chemoresistance in Notch1-hyperactivated pancreatic cancer”的研究论文,本研究中,研究人员鉴定了一个之前未被鉴定的微蛋白,Notch1降解相关调节多肽(N1DARP),通过LINC00261编码。为了评估N1DARP的治疗潜力,研究人员设计了一种穿透细胞的钉合肽SAH-mAH2-5,它具有与N1DARP相似的螺旋结构,具有显著的理化稳定性。SAH-mAH2-5与N1ICD相互作用并促进蛋白酶体介导的降解。在notch1激活的胰腺癌模型中,SAH-mAH2-5注射在有限的脱靶和全身不良反应的情况下提供了实质性的治疗益处。综上所述,这些发现证实了N1DARP通过调节USP10-Notch1致癌信号来发挥肿瘤抑制和化学增敏剂的作用,并提出了一个有前景的靶向N1DARP - n1icd相互作用的notch1激活的胰腺癌治疗策略。

https://www.nature.com/articles/s41421-023-00592-6
研究背景
01
胰腺癌是恶性程度最高的消化道肿瘤之一,与其他主要恶性肿瘤相比预后最差,5年生存率< 10%。只有20%的胰腺癌患者适合接受手术治疗,而其他患者必须接受化疗。胰腺导管腺癌(PDAC)因其固有的瘤内异质性和高度促结缔组织增生的肿瘤微环境而对标准化疗产生难治性耐药。最近的证据支持利用在胰腺癌中持续激活的高度保守的信号通路,如Notch、Hedgehog和Wnt信号通路,来识别新的生物标志物和治疗靶点。
Notch是一个短寿命蛋白家族,主要通过泛素-蛋白酶体系统进行快速降解,其各种成分正或负调节Notch1的稳定性。这表明促进泛素介导的Notch家族成员降解可能是靶向Notch激活癌症的一种有希望的策略。USP10是一种序列高度保守的去泛素化酶,是参与肿瘤发生的p53负调控因子。USP10通过去泛素化多种蛋白质,在癌细胞中赋予化学耐药性。N1ICD在usp10介导的生物过程中起着至关重要的作用,如细胞发育、血管生成和心功能障碍。因此,靶向USP10-N1ICD相互作用可能是notch1过度激活癌症的潜在抗肿瘤策略。
长链非编码Rna (lncrna)具有信号、诱饵、导向和支架的功能。在本研究中,研究人员通过RNA测序和核糖体分析鉴定了一个由LINC00261编码的未知多肽N1DARP,它可以通过干扰USP10-N1ICD的相互作用来作为一种新的肿瘤抑制和化疗增敏剂,用于胰腺癌的治疗。该研究还评估了利用N1DARP衍生的修饰钉状肽SAH-mAH2-5靶向N1DARP的治疗潜力,该修饰钉状肽干扰了USP10-N1ICD相互作用并抑制notch1激活的胰腺癌的肿瘤生长,从而为如何靶向N1DARP - n1icd相互作用以开发精确和个性化的胰腺癌治疗提供了见解。
研究过程及发现
02
本研究基于mRNA和核糖体测序结合分析的证据,利用患者来源的类器官模型确定了LINC00261,一个新出现的泛癌症抑制因子,作为一个功能可翻译的lncRNA。在初步筛选中,研究人员将重点放在由LINC00261, N1DARP编码的进化保守肽上,该肽包含41个氨基酸,这与先前的证据一致,即含有30多个氨基酸的多肽被认为具有潜在的功能。与先前报道的主要致癌的多肽不同,N1DARP是一种肿瘤抑制微蛋白,可能为基于蛋白质递送的癌症治疗提供一种新的方法。
在机制上,研究人员发现N1DARP通过与蛋白酶体介导的N1ICD降解相互作用并促进其抑制Notch1信号传导,从而为Notch1信号传导提供了一种新的调节剂。药物抑制Notch信号是治疗胰腺癌的一种很有前途的方法。最近,一项II期研究表明,Notch2/3抑制剂tarextumab与GEM和紫杉醇联合使用可显著降低胰腺癌。同样,本研究为利用非编码RNA编码的多肽靶向特异性Notch1受体提供了一个新的视角。本研究证实,微蛋白N1DARP通过增加K11和k48相关的N1ICD多泛素化来促进N1ICD的降解,提示N1DARP可能是特异性失活Notch1通路的胰腺癌新的治疗靶点。为了在USP10和N1ICD之间的界面上确定一个更可药物化的靶点,研究人员从N1DARP的α-螺旋中衍生了一个钉接肽,SAH-mAH2-5,具有显著的亲和力、渗透性和物理化学稳定性。这些发现为靶向USP10-N1ICD相互作用的治疗潜力提供了强有力的证据,为治疗胰腺癌提供了一个有前途的化学结构和联合策略。
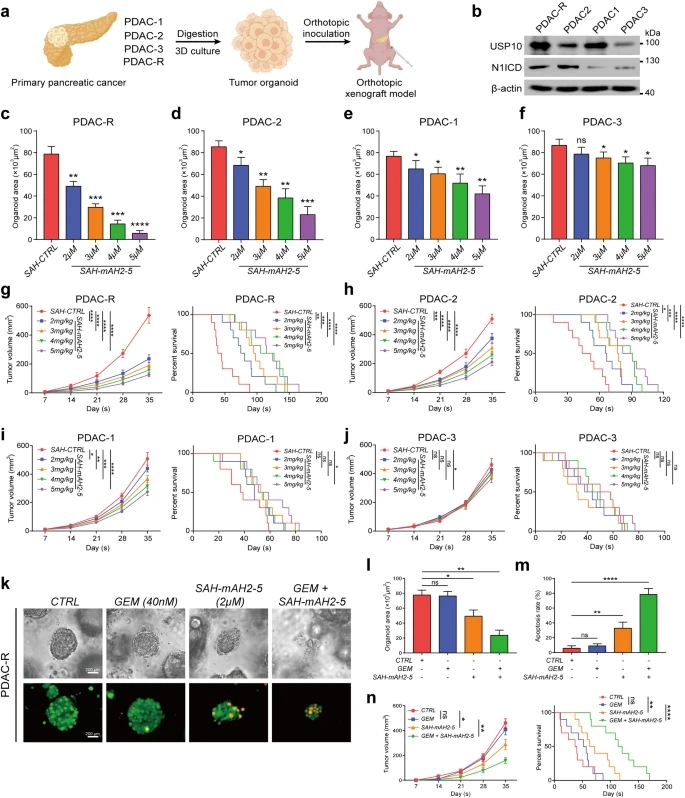
在PDO和PDOX模型中,SAH-mAH2-5抑制胰腺癌细胞的进展并增强化疗敏感性
研究意义
03
总的来说,本研究结果确定了N1DARP是一种新的肿瘤抑制因子和化疗增敏剂,通过控制USP10-Notch1的致癌信号,用于胰腺癌治疗。并提供了一种新的策略,通过设计从微蛋白N1DARP衍生的钉接肽SAH-mAH2-5靶向USP10-Notch1的相互作用。靶向N1DARP-N1ICD相互作用和N1ICD降解可能是治疗notch1激活的胰腺癌的一种有希望的替代策略,并且可能在非肿瘤疾病的治疗中有更广泛的应用。(转化医学网360zhyx.com)
参考资料:
https://www.nature.com/articles/s41421-023-00592-6
注:本文旨在介绍医学研究进展,不能作为治疗方案参考。如需获得健康指导,请至正规医院就诊。
 腾讯登录
腾讯登录
还没有人评论,赶快抢个沙发