《转》访潘柏申教授:医学检验的发展离不开LDT
| 导读 | 《转》访是转化医学网的品牌专访栏目,是业内专家、大佬、知名企业智慧交流碰撞的平台,也是促进行业健康发展的重要力量,《转》访致力于打造转化医学领域最知名的专家访谈栏目。 |

导语:前不久国家卫计委发布了《国家卫生计生委办公厅关于临床检验项目管理有关问题的通知》,似乎是为临床实验室自建项目(LDT)在开闸放水。对此,业内人士有着诸多的期许和猜测。本次我们邀请到复旦大学附属中山医院的潘柏申主任,看看他眼里的LDT发展是怎样的?
1. 精准医学的发展,LDT是必经之路转化医学和个体化医学成为现代医学发展的新动力,实验室新技术的涌现,以及将这些新技术新科技与临床疾病的诊断相结合,让患者可以得到个性化的、可预测的、可预防的以及可参与的一体化医疗服务。临床实验室自建项目(LDT)以分子和蛋白组学技术为基础,为“从实验室到病床旁的快速转化”提供可能。
目前我国对LDT的概念和范围尚没有明确的定义和界定。美国临床病理学会和临床实验室改进咨询委员会对LDT定义为:实验室内部研发、验证和使用,采用生物化学、细胞遗传学、分子生物学试验方法,以诊断为目的,分析DNA、RNA、线粒体、蛋白组和代谢组疾病等生物标志物的体外诊断项目;LDT仅能在研发的实验室使用;可使用购买或自制的试剂,但不能销售给其他实验室、医院或医生;LDT的开展不需要经过食品药物管理局(Food and Drug Administration,FDA)的批准。
基于高新检测技术的LDT的主要特点:检测方法的仪器设备复杂 ,操作技术难度较高 ,操作人员素质和技术能力要求高,结果分析高度依赖高科技分析软件和数据处理系统,结果解释的临床水平要求高。
基于高新检测技术的LDT的临床应用:诊断罕见疾病(如遗传性疾病), 协助选择精准治疗方式(如肿瘤靶向药物选择),预测疾病风险。
2. LDT的监管现状
2.1 美国对LDT有着较为明确的监管措施,并且与医保制度有关
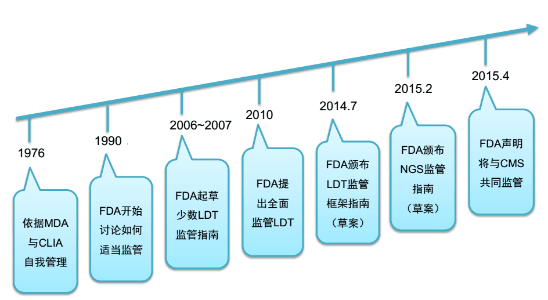
LDT监管过程概要
近年来,LDT问题在美国一直处于舆论的风口浪尖。美国FDA开始希望对LDT进行直接监管,也获得了兄弟政府机构和部分国会成员的“鼎力支持”,但却遭到来自美国临床化学协会(AACC)、美国临床病理学会(ASCP)等权威学术组织强烈的反对。关于FDA监管LDT的争议主要体现在如下几个方面:质疑FDA监管LDT的法定资格:LDT 的监管权应仅限于美国医疗保险和医疗补助服务中
心(The Center for Medicare & Medicaid service,CMS);CMS 依据 CLIA 已对 LDT 进行了很好的监管;FDA 即使可行使监督权,也不是制定监管规则的法定人。
质疑FDA将临床医学检验实验室视为制造商:LDT应该被称为“医学检验实验室自建检测程序”(LDP),这更能准确的描述LDT的本质,LDT是一种医疗服务而并非医疗器械;FDA将已获批准的诊断产品使用中的重大修改也视为LDT,但并没有明确的对于“重大”界定标准。
阻碍具有重大价值的新项目开展,扼杀个体化医疗创新:只有个别资金雄厚的商业化医学检验实验室才有可能达到FDA上市前审批的要求,从而垄断该领域的检测项目,使得临床医生与患者失去了更多的选择机会,长远对于患者而言反而可能是有害的。
FDA监管模式对基因组检测(NGS等技术)适用性:一些罕见病的基因测试可能因为受众太少,难以达到临床性能验证要求而得不到批准;对于基因组检测的LDT临床应用和安全性评估因为耗时太长,无法按照FDA传统的监管模式在上市前完成;FDA没有超越CMS的分析全过程质量保证的监督方案;传统检测项目的结果一致性评价标准(能力验证试验)并不适用于NGS。
FDA与CMS合作成立专项工作组,共同监管LDT
FDA负责LDT上市前审批,包括分析性能评估和临床应用评估;而CMS负责医学检验实验室操作、检测过程和人员能力的监管;专项工作组正在探索可以避免重复监管、提高监管效能的方式,重新定义FDA和CMS存在差异的术语,以便使医学检验实验室更好地理解双方的监管要求。
2.2 欧盟和日本对LDT没有明确的监管措施,与医保关系不大

美国与欧盟、日本对LDT监管情况对比
在欧洲与日本,LDT的监管现状与美国截然不同,既没有明确的针对LDT的监管定义,也没有严格的与此相关联的医保制度。在欧盟地区,IVD上市由各成员国监管部门根据IVD Drecitve(Council Drecitve 98/79/EC)要求审批。然而LDT没有在IVD Drecitve监管范围之内。这也就使得在欧盟LDT不受约束。
2.3 我国LDT的发展需求远重于监管
我国临床医学检验实验室开展的LDT,无论是数量还是种类都与美国等发达国家相距甚远。美国LDT的先进检测方法的代表如新的分子诊断检测技术以及质谱分析技术等,国内仅有少数临床医学检验实验室开展,并且大多仅作为临床研究,无法满足临床诊疗日趋增长的个体化与精准化的需求。我国现有的检验项目注册审批制度和收费管理制度也限制了绝大部分LDT的临床应用和发展。对于我国临床医学检验实验室现状而言,发展的需求远重于监管需求。如果临床医学检验实验室的LDT还没有得到应用和发展,那监管也就事实上缺乏相应主体,成为一句空话。现在就完全参照美国FDA的某些想法对LDT实行进行严格和过度的监管,将可能极大阻碍医学检验实验室新方法新技术的应用及发展。
2007年CFDA颁布了《体外诊断试剂注册管理办法(试行)》,根据产品风险程度的高低,将体外诊断试剂分为第一、二、三类。随着检测技术和临床研究的进展,更多符合临床疾病需求的LDT不断涌现并发展成熟,由于这些 LDT 均未在2013版检测目录中,因此,多数有实力开展 LDT的医疗机构因严格遵从相关规定而并未真正开展大规模的检测工作,而这些项目的检测多由医学独立实验室或第三方检测机构完成。
潘主任表示,对“萌芽”中的LDT试行过于严格、过度的监管,将可能极大的阻碍了医学检验实验室新方法和新技术的应用及发展。全面放开LDT注册审批制度和收费管理制度,虽然可能引发各种乱象,不过,我们建议可以选择一些权威的、有资质的医院来打头阵,慢慢积累经验,从而不断完善现有的LDT管理制度。
3 .“一管就死、一放就乱”的僵局怎么破解?
潘主任表示,“满足临床需求是医学检验的存在基础;医学检验的发展离不开LDT。” 至于“管”与“放”的僵局我们可以从两方面来攻破:一方面,试点单位(如国家临床重点检验专科建设单位;通过 ISO 15189 或 CAP 认可的三甲医院检验部门)的局部放开(在有条件的大型医院医学检验部门逐步放开甚至鼓励适当发展LDT);另一方面,实行适当的质量监管,以取得经验,为LDT在更大范围内的科学合理运用创造条件。“创新发展,并不断促进创新和发展,在发展中进行科学合理的监管”应成为LDT科学监管的新思路、新模式。
4. 国家卫计委关于LDT相关问题通知文件的私家解读
国家卫计委网站截图
潘主任表示,这次卫计委颁布的《国家卫生计生委办公厅关于临床检验项目管理有关问题的通知》文件各界从不同角度理解不一,官方现在也没有权威的解读。我个人觉得卫计委发布的文件只是简单的提及“对于未列入《医疗机构临床检验项目目录(2013版)》,但临床意义明确、特异性和敏感性较好、价格效益合理的临床检验项目,应当及时论证,满足临床需要;医疗机构在引入新的临床检验项目过程中,要合理设置审核程序,优化流程,提高效率,便于符合临床需求的检验项目及时得到应用。”,但是具体怎么论证、怎么审核、审批流程怎么样等并没有具体说明,CFDA并没有明确表态,物价局、医保方面也没什么动静,所以说这次的文件颁布真的是对临床实验室自建项目“开闸放水”?“亮绿灯”?还难以简单解读。5. 关于易感基因检测
易感基因不是发病基因,而是在适宜的环境刺激下能够编码遗传性疾病或获得疾病易感性(有遗传决定的已于患有某种或某类疾病的倾向性)的基因。早期对易感基因进行检测,深入研究,可以有效的防止和控制遗传疾病的发生。
通过易感基因检测我们可以找到与易感基因相关的其他因素,当这些因素了解后可以有助于我们对疾病的控制、筛查、诊断以及治疗。
我们对疾病的认知是一个不断发展、探索的过程,也是一个经验积累的过程。在很多新鲜事物刚出现的时候,很多人都持有怀疑的态度,但是随着我们对疾病了解的不断深入,会伴随发现更多生命的奥秘。同时我认为易感基因在疾病的预防、治疗以及对某种疾病系统性的了解都发挥着重要作用。
潘柏申教授简介:
复旦大学附属中山医院检验科主任,研究员,教授。同时担任《中华检验医学杂志》、《检验医学》、《临床检验杂志》、《国际检验医学杂志》等多本杂志的副主编或编委;中华医学会检验分会第九届委员会主任委员;卫生部全国临床检验标准化委员会副主任委员等。(转化医学网360zhyx.com)本文是转化医学网原创内容,转载请点击获取授权
 腾讯登录
腾讯登录
还没有人评论,赶快抢个沙发