安诺基因助力全球首例亨廷顿猪模型的建立,登顶Cell
| 导读 | 近日暨南大学千人计划特聘教授李晓江等研究团队利用基因编辑和体细胞核转移技术实现了全球首例亨廷顿(HD)舞蹈病猪的培育,并精准地模拟出人类HD舞蹈症的表型,研究成果发表在国际顶级学术期刊Cell上。 |

研究对象:亨廷顿舞蹈症,猪
合作单位:暨南大学粤港澳中枢神经再生研究院、美国Emory大学和中国科学院广州生物医药与健康研究院
发表期刊:Cell
发表时间:2018年3月
影响因子:30.41
研究背景
亨廷顿舞蹈病是由单基因突变导致的神经退行性疾病,是一个理想的疾病模式,是研究多基因突变病的基础。但在以哺乳动物为模式动物模拟这种疾病研究时却处处碰壁。例如以小鼠作为动物模型时由于体型和生理结构等与人类差异显著所以无法模拟病人的病理特征,许多研究结果在临床应用上往往无效;以猴子为模型时由于猴子早夭等问题导致进展困难。因此,建立准确模拟疾病病理的动物模型,成为生命科学领域亟待攻克的难题。
研究思路
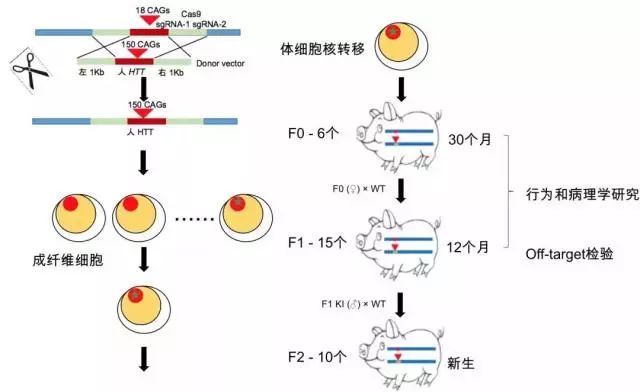
图1 研究路线图
研究结果
基因编辑将猪内源的亨廷顿基因(HTT)替换为人的HTT突变基因
从2013年基因编辑技术(CRISPR/Cas9)开始应用于哺乳动物后,李晓江教授团队就开始利用该技术将猪内源HTT基因的第一个外显子作为靶位点,通过构建两条gRNA,促使猪第一个外显子与人的HTT突变基因(包含150个CAG重复)的第一个外显子同源重组,实现定点替换。将构建好的gRNA、供体质粒(两侧包含1Kb的猪第一外显子两侧同源序列的人HTT突变基因)和Cas9共转化至猪的成纤维细胞,最终实现包含150 CAG重复序列的人HTT第一外显子精确地替换掉猪的HTT内源性基因的第一个外显子。这样就可以在猪的成纤维细胞中表达人突变的HTT基因。
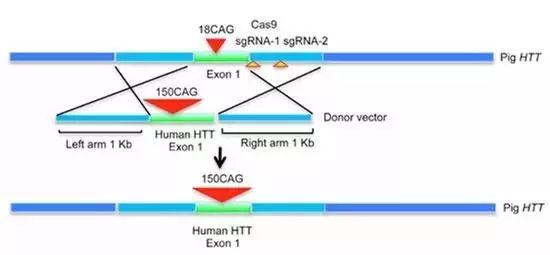
图2 基因编辑实现靶位点定点替换
利用成纤维细胞筛选阳性基因敲入细胞
只有阳性的基因敲入细胞进行体细胞转移才能将人的HTT突变基因导入猪体内,因此首先需筛选阳性基因敲入细胞。为了筛选到成功的基因敲入成纤维细胞,需要对大量的转化细胞进行筛选。PCR鉴定是最直接最快速的鉴定方法。实验团队从2430个成纤维细胞中筛选到9个内源HTT被替换为人HTT突变基因的阳性细胞。
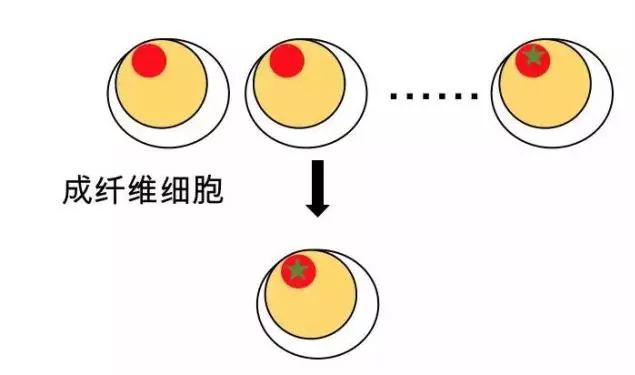
图3 阳性成纤维细胞筛选
体细胞核转移技术培育胚胎并繁殖后代
由于细胞核具有全能性,因此可以将体细胞核转移到去核的卵母细胞中促使其发育成新胚胎,进而获得克隆个体。在筛选到的9个阳性成纤维细胞中选出一个状态最好的并经过PCR证实为替换成功的成纤维细胞用于体细胞核转移,获得2880个胚胎。将这些胚胎移植到16个代孕猪中,10只猪成功受孕。最终获得7个个体,PCR鉴定后确认其中6个个体为基因敲入成功的个体。用这些基因敲入成功个体中的母猪与野生型Bama公猪交配获得F1,然后用F1中基因敲入成功的公猪与Bama母猪交配获得F2。通过两年多的培育结合PCR鉴定,最终共获得15个基因敲入成功的F1和10个基因敲入成功的F2。
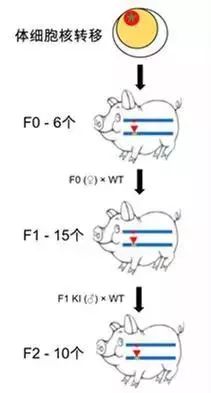
图4 体细胞核转移培育基因敲入猪
阳性个体的脱靶位点检测
基因编辑技术利用RNA引导Cas9核酸酶可在多种细胞的特定的基因组位点上进行切割替换,实现对特定位点的编辑,但是该系统面临严重脱靶危机。以小鼠为例,基因编辑过的小鼠体内有超过1500个单核苷酸发生了突变。一旦基因敲入猪体内出现脱靶位点,那么在后续的研究中很难辨别病理特征是由于基因敲入引起的还是由于脱靶位点变异引起的。
为解决这一难题,实验团队与安诺基因携手,由实验室提供F1的大脑皮层,安诺基因以重测序的方式对两个向导RNA脱靶位点检测,最终结果显示成功的敲入个体中不存在脱靶位点。所以这些基因敲入猪是可进行下一步实验的。
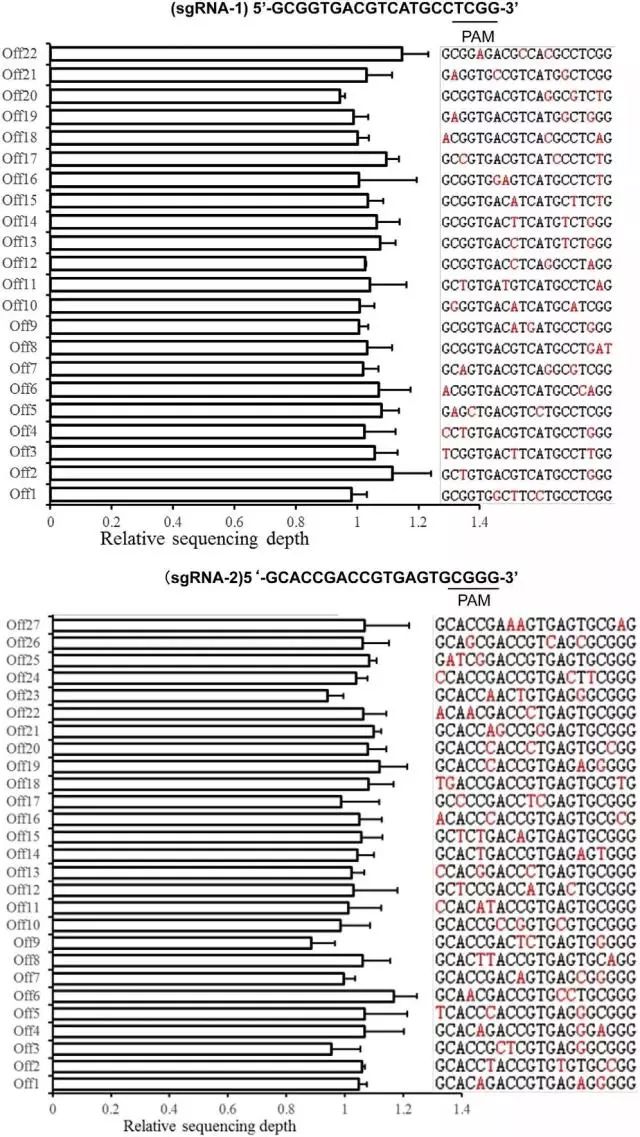
图5 脱靶位点检测
行为和病理学研究
对这些基因敲入个体进行行为学研究发现带有致病基因的个体在出生后前四个月并没有表现出明显症状,这些“亨廷顿猪”们与正常小猪一般可爱,但随着年龄的增大,逐渐就显示了与“舞蹈”症一致的特征:皮肤松弛下垂、体重下降、步态异常、呼吸困难等。此外病理观察发现,亨廷顿猪有着大脑纹状体神经元死亡的典型病理特征。所以亨廷顿猪模型可以精确模拟人类亨廷顿病的行为和病理学特征。

图6 HD基因敲入猪的症状
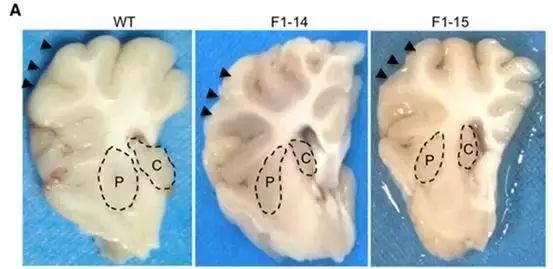
图7 HD基因敲入猪的纹状体特异性退行
本研究成功构建了世界首例可遗传的亨廷顿猪模型,亨廷顿舞蹈病基因敲入猪的建立是神经退行性疾病研究领域中一个里程碑式的发现,使科学家能更深入了解神经细胞死亡的机制及寻找有效的治疗方法。文中基因编辑后对脱靶位点的检测由安诺基因提供。
安诺优势
动植物重测极速体验
安诺基因推出重测序极速周期,最快仅需8个自然日就可以拿到数据。

自动化平台优势
安诺基因拥有高通量的自动化建库,涵盖个体重测序、群体进化、GWAS等各个方向。
全方位脱靶位点检测
体外全基因组检测脱靶位点是利用Cas9和其他类似的核酸酶切割基因组时,打断DNA双链,再用高通量测序的方式进行脱靶位点检测。这种检测方式可以检测到突变频率低于0.1%的脱靶位点。安诺基因通过CRISPR-高深度全基因组测序可以对基因编辑的细胞或个体进行全方位脱靶位点检测,可助力更快速更精准的实现和评估CRISPR基因编辑技术。
(转化医学网360zhyx.com)
 腾讯登录
腾讯登录






顶一下(0) 回复