超热门!进击2018基因编辑CRISPR系统重磅研究盘点!
| 导读 | 基于CRISPR系统的基因编辑技术无疑是当前最热门的领域之一,上顶级期刊头条也是家常便饭 |
基于CRISPR系统的基因编辑技术无疑是当前最热门的领域之一,上顶级期刊头条也是家常便饭,本文将盘点今年这个领域的重磅研究文章,为读者梳理相关的知识要点。


1
新一代基因编辑工具CRISPR/Cpf1
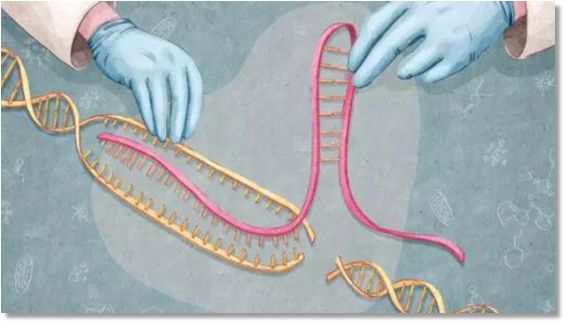
CRISPR/Cpf1基因编辑系统最早出现于2015年,与CRISPR/Cas9基因编辑系统相比,新的CRISPR/Cpf1基因编辑系统具有如下优势,①只需一个协助RNA分子,Cas9需要2个RNA分子协助,Cpf1(也称作Cas12a)只需要一个RNA分子;②Cpf1酶分子量比Cas9小,进入细胞更容易,编辑成功率会提高;③Cpf1系统不同的识别序列令其基因编辑效果更好;④剪切位置与Cas9不同,选择余地更大;⑤产生黏性末端,便于新DNA序列插入。
1月,Cell发表张锋关于第二类CRISPR-Cas系统CRISPR/Cpf1的综述,介绍了新一代CRISPR基因组编辑系统,基于不同的效应蛋白家族,可以分为3种类型和9种亚型,其中譬如Cas9和Cas12a(Cpf1)。指出Cpf1系统更简单一些,它只需要一条RNA。Cpf1酶也比标准SpCas9要小,使得它更易于传送至细胞和组织内;Cpf1以一种不同于Cas9的方式切割DNA(DOI:10.1016/j.cell.2016.12.038)。
5月,Nucleic Acids Res发表上海生科院在Cpf1蛋白切割机理方面的研究,鉴定了Cpf1蛋白的精确切割位点,并基于该切割特性开发新的DNA无缝拼接方法(DOI:10.1093/nar/gkx018)。
6月,Nature发表哥本哈根大学论文,从结构上揭示CRISPR-Cpf1的DNA靶向机制,阐述了Cpf1的分子剪刀让DNA解链并进行切割的分子机制,指出Cpf1的主要优势在于它的高度特异性和DNA切割方式(DOI:10.1038/nature22398)。
8月,Nature Biotechnol发表张锋研究组扩展CRISPR/Cpf1 的靶点选择范围的研究,指出突变AsCpf1和LbCpf1的方法可以扩大了靶点选择范围,由靶点选择仅限于PAM为TTTV 的DNA序列扩大了PAM位点的选择范围(DOI: 10.1038/nbt.3900)。同月,Nat Chem Biol论文提出高效地编辑人类基因组的优化CRISPR-Cpf1技术(DOI:10.1038/nchembio.2410)。
2
提升基因编辑工具效率和准确率
7月,Nature Medicine发表Broad研究院发表关于减少由人体遗传变异导致CRISPR/Cas9基因编辑系统精度削弱的方法,可帮助研究人员设计出有效且安全的CRISPR疗法(Doi:10.1038/nm.4377)。同月,Cell发表基于CHAMP(ChipHybridized Affinity Mapping Platform)基因测序技术平台的CRISPR编辑工具,其能够通过个体的完整基因组来快速检测CRISPR分子(DOI:10.1016/j.cell.2017.05.044)。
9月,Science论文提出改进Cas9的PAM序列,改善Cas9打开DNA双螺旋以搜索基因的位置和频率,使得Cas9更加快速地发现它们的靶序列,而且也会降低副作用产生的风险(DOI:10.1126/science.aah7084)。同月,Nature论文指出操纵Cas9的REC3结构域可大幅降低CRISPR-Cas9的脱靶效应 (DOI:10.1038/nature24268)。
11月,PNAS发表霍普金斯大学关于提高CRISPR/Cas9基因编辑效率的基因组规则,该对于人类基因编辑效率的提升具有重要指导意义。(DOI:10.1073/pnas.1711979114)。同月,Nat Commun提出一种新的方法可以使CRISPR基因编辑准确性高达98%,该方法采用RNA适配子(RNA aptamer)分子胶组装一种完整的CRISPR修复工具包并将这种工具包运送DNA切割位点上(DOI:10.1038/s41467-017-01875-9)。
11月,Nature和Science发表新型DNA/RNA碱基编辑器论文,提出可校正点突变的基因工具,该研究进一步扩大了CRISPR的使用范围,开发出一种更加微妙的被称作碱基编辑(base editing)的方法来修复遗传物质(DOI:10.1038/nature24644;DOI:10.1126/science.aaq0180)。
3
精准多重基因编辑新工具eMAGE的提出
11月,Cell发表耶鲁大学关于更加精确、高效的基因编辑技术,实现真核生物基因组多个位点上进行精确的基因修饰。不同于现有基于DNA双链断裂和重新修复的基因编辑技术,通过对酵母的DNA复制和修复功能进行改造,能够在不发生双链断裂的情形下将新的遗传信息插入到它的基因组多个不同区域中,从而开发出真核生物多重基因组工程工具(DOI:10.1016/j.cell.2017.10.034)。
4
基于CRISPR/Cas9工具的单条染色体敲除技术
8月,MolecularTherapy发表采用澳大利达亚特莱特大学关于CRISPR/Cas9对小鼠完整染色体的清除技术(DOI:10.1016/j.ymthe.2017.05.021)。
11月,Genome Biol发表我国上海生科院采用CRISPR/Cas9工具可选择性消除单条染色体敲除技术,通过证明应用CRISPR/Cas9介导的针对Y染色体的多位点DNA切割可以有效地将小鼠胚胎干细胞的Y染色消除(DOI:10.1186/s13059-017-1354-4)。
5
可靶向RNA编辑的CRISPR/Cas13工具
2月,Mol Cell论文阐述靶向RNA的CRISPR酶系统,研究发现了两个利用Cas13b酶的新型的RNA靶向CRISPR系统,该酶系统具有靶向RNA的能力,可高通量地方式特异性地操纵RNA(DOI:10.1016/j.molcel.2016.12.023)。
6月,Cell发表中科院关于结构上揭示Cas13a切割RNA机制,这种crRNA-靶RNA双链形成促进LbuCas13a的HEPN1结构域移向HEPN2结构域,从而激活LbuCas13a的HEPN催化位点,随后LbuCas13a就以一种非特异性的方式切割单链靶RNA和其他的RNA(DOI:10.1016/j.cell.2017.06.050)。
9月,Nat Struct Mol Biol论文展示RNA靶向CRISPR酶Cas13a的作用机制,描述了Cas13a酶如何产生功能性crRNAs,以及在靶标RNA识别之前,其催化活性如何被封闭,这将有助于解析细菌免疫系统,以及临床诊断治疗(DOI:10.1038/nsmb.3466)。
10月,Nature发表MIT关于CRISPR–Cas13靶向哺乳动物细胞中的RNA的基因编辑工具,证实切割RNA的Cas13a酶(之前称作C2c2)能够特异性地降低哺乳动物细胞中的内源性RNA和报告RNA水平。研究指出Cas13a结合和切割单链RNA,并开发出可在哺乳动物细胞中发挥作用CRISPR-Cas13a的RNA编辑(DOI:10.1038/nature24049)。
7
人类胚胎编辑
8月,Nature发表利用CRISPR/Cas9校正人胚胎中的致病性突变的研究,通过对活的人胚胎进行基因编辑,成功地校正导致心脏病的MYBPC3基因突变(DOI:10.1038/nature23305)。
11月,Protein& Cell发表中山大学利用改进的CRISPR-Cas9校正人胚胎中突变基因的研究,成功地对导致β-地中海贫血的一种单核苷酸错误进行校正,这种技术比之前的方法有潜力实现更高精准的编辑(DOI:10.1007/s13238-017-0475-6)。
8
基因编辑技术用于干细胞
7月,Cell Res发表中科院关于单碱基基因编辑干细胞进行可遗传功能增强研究,利用基因编辑技术改写了人类基因组遗传密码中NRF2编码基因第2号外显子上的单个碱基,首次在实验室中获得了遗传增强的“超级”干细胞(DOI:10.1038/cr.2017.86)。
9
基因编辑技术用于T细胞
3月,Nature发表斯隆凯特林癌症纪念中心利用CRISPR/Cas9构建强效CAR-T细胞的研究论文,证实CRISPR/Cas9技术能够运送CAR基因到T细胞基因组中的特定位点上(DOI:10.1038/nature21405)。
(转化医学网360zhyx.com)
 腾讯登录
腾讯登录






还没有人评论,赶快抢个沙发