Nature一天连发两文!肠道菌群不仅攸关神经退行性疾病,还可能导致白血病!
| 导读 | 点击上方“转化医学网”订阅我们!干货|靠谱|实用 导 读我们在出生时就会从母体上“捎带”一些肠道菌群,出生后,周围环境的细菌也会成为肠道菌群的一部分。每个人的肠道中都有500-1000个不同种类的肠道菌群,总数大约有10万亿。近年来,肠道菌群的相关研究如火如荼,人们惊奇地发现,这些存在于肠道的微生物与睡眠、免疫、肥胖、心血管疾病甚至癌症等生理病理过程息息相关。5月16日,著名国际期刊 |
我们在出生时就会从母体上“捎带”一些肠道菌群,出生后,周围环境的细菌也会成为肠道菌群的一部分。每个人的肠道中都有500-1000个不同种类的肠道菌群,总数大约有10万亿。近年来,肠道菌群的相关研究如火如荼,人们惊奇地发现,这些存在于肠道的微生物与睡眠、免疫、肥胖、心血管疾病甚至癌症等生理病理过程息息相关。5月16日,著名国际期刊《Nature》连发两文,指出肠道菌群不仅可以影响神经退行性疾病,在某些特定情况下还可能导致白血病!
1. 肠道菌群在神经系统搞的事——与大脑“深入交流”
小胶质细胞(microglia)是神经胶质细胞的一种,相当于脑和脊髓中的巨噬细胞,是中枢神经系统(CNS)中的第一道也是最主要的一道免疫防线。无数临床上和神经病理学研究表明激活的小胶质细胞在如帕金森病,多发性硬化和阿尔兹海默症等的神经退行性疾病的发病机理中起到十分重要的作用。在《Microglial control of astrocytes in response to microbial metabolites》一文中,美国哈佛医学院等机构的研究人员指出神经退行性疾病可能受肠道内共生微生物与大脑细胞作用的影响。他们确定了介导小胶质细胞和星形胶质细胞交流的关键分子,明确了肠道微生物代谢物影响小胶质细胞和星形胶质细胞的致病活性和抑制CNS炎症的途径。

研究人员对部分多发性硬化症(MS)小鼠喂食了一种不含色氨酸的食物,结果显示这些小鼠的小胶质细胞产生了VEGF-B,而VEGF-B激活了星形胶质细胞,导致小鼠表现出了更多的MS症状。当食物中添加色氨酸后,小胶质细胞则释放了TGFα,抑制了星形胶质细胞的活性并改善了动物的健康。这就表明由共生菌群产生的色氨酸微生物代谢物可控制小胶质细胞的活化和TGFα和VEGF-B的产生。
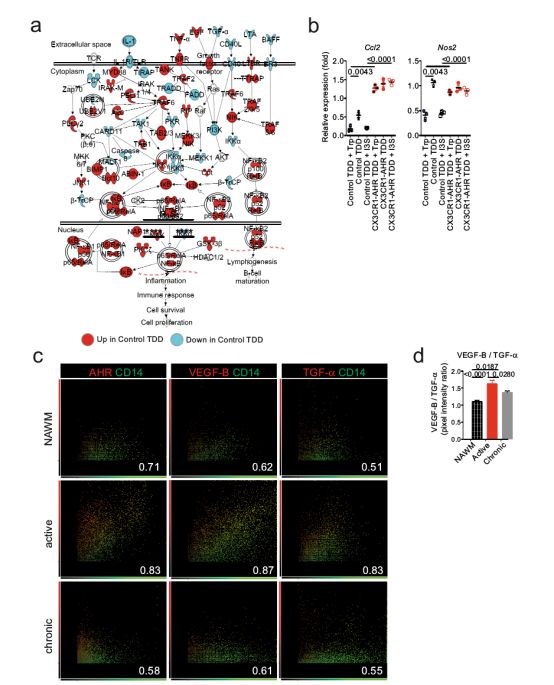
色氨酸微生物代谢物对TGFα和VEGF-B的影响
接着研究人员对MS小鼠模型产生的TGFα和VEGF-B进行研究。TGFα和VEGF-B由小胶质细胞分泌,他们发现TGFα可与星形胶质细胞中的ErbB1受体发生作用,从而限制其致病活性和MS的发展。相反,VEGF-B则能触发星形胶质细胞中的FLT-1信号传导,导致MS恶化。同时VEGF-B和TGFα也参与人小胶质细胞对星形细胞的作用。此外,他们发现CD14+细胞中TGFα和VEGF-B的表达也与多发性硬化病变的发展相关。
另一方面,过往的研究表明,色氨酸微生物代谢物可与芳基烃受体(AHR)相互作用,而小胶质细胞中也存在AHR,因此AHR或许是动物肠道微生物释放的代谢产物作用于小胶质细胞的关键受体。研究人员通过小鼠AHR缺失的对照实验确认小胶质细胞可通过AHR接受肠道微生物传递的信号,而且AHR可调节TGFα和VEGF-B的产生,进而影响炎症水平。
就此,肠道菌群对神经退行性疾病的调节机制已趋明了。最终研究人员还在实验室培养的人类小胶质细胞、星形细胞以及MS组织样本中证明了色氨酸代谢物、AHR、TGFα和VEGF-B的作用,从而指出肠道微生物和与之信号对接的细胞或可成为疾病治疗的靶点。
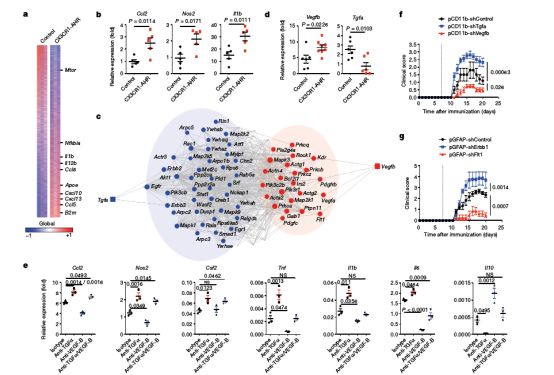
AHR调节小胶质细胞TGFα和VEGF-B
2. 肠道菌群与白血病——“帮凶”当得不亦乐乎

白血病是一类造血干细胞恶性克隆性疾病。近期有研究发现TET2基因突变在DNA去甲基化修饰、表观遗传调控及骨髓造血中扮演着重要角色,这一突变会给造血干细胞带来额外的生存优势,且容易恶化,与部分白血病的发病有关。但是,芝加哥大学医学院的研究人员却在研究TET2突变影响白血病发病机制时发现只有50%-75%的TET2突变小鼠出现白血病症状,说明TET2突变仅仅是白血病的诱因之一,而不是唯一的因素,并发现肠道菌群在白血病的发病中扮演了某种关键角色。
研究人员通过定量分析,在TET2突变小鼠的外周血液、肠系膜淋巴结以及脾脏中找到了细菌16S rRNA的存在,而进一步的细菌培养证实了这些细菌包括乳酸杆菌(Lactobacillus)等肠道菌群。进一步的验证实验中,研究人员对实验小鼠使用了抗生素和IL-6抑制剂,成功逆转了小鼠在白血病发作前的骨髓增生,另一方面,无菌环境下出生的小鼠即使存在TET2突变,也没有发生骨髓增生。这就明确地证明了肠道菌群在白血病发病过程中具有举足轻重的作用,也就是说,肠道菌群可以成为TET2突变的帮凶,导致白血病发病。因此,肠道菌群水平和IL-6水平或许可以成为白血病治疗的契机,成为所有白血病患者的福音。
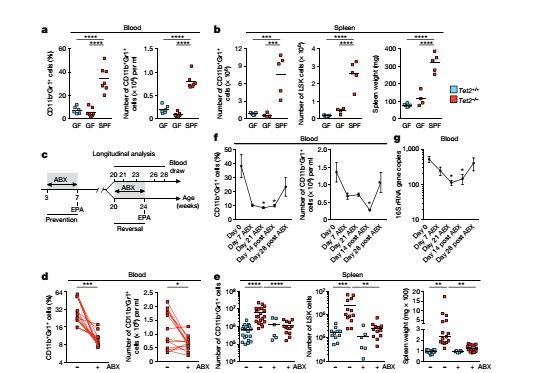
肠道菌群对TET2突变白血病的影响
随着研究的深入,肠道菌群相关研究快速成为热门头条,吸引了生物医学界的大量目光。肠道菌群在长期的进化过程中,通过个体的适应和自然选择,实现了菌群中不同种类之间,菌群与宿主之间,菌群、宿主与环境之间的动态平衡,形成了一个互相依存,相互制约的系统。这个系统可影响体重和消化能力、抵御感染和自体免疫疾病的患病风险,还能控制人体对癌症治疗药物的反应。相信随着肠道菌群系统进一步深入研究,会有更多惊喜等着我们。
参考文献:
1.Microglial control of astrocytes in response to microbial metabolites
2.Microbial signals drive pre-leukaemic myeloproliferation in a Tet2-deficient host
 腾讯登录
腾讯登录







还没有人评论,赶快抢个沙发