【Nature子刊】癌症免疫治疗反应预测:复旦大学附属肿瘤医院带来“精准医疗”新突破
| 导读 | 这项研究确认了胃癌中apCAFs的存在及其在抗肿瘤免疫中的重要作用,揭示了apCAFs在免疫治疗反应中的潜在预测价值,为未来免疫治疗策略的优化提供了新方向。 |
2025年3月4日,复旦大学附属肿瘤医院的研究团队在期刊《Nature Communications》上合作发表了题为“Antigen-presenting cancer associated fibroblasts enhance antitumor immunity and predict immunotherapy response”的研究论文。

https://www.nature.com/articles/s41467-025-57465-7
这项研究确认了胃癌中apCAFs的存在及其在抗肿瘤免疫中的重要作用,揭示了apCAFs在免疫治疗反应中的潜在预测价值,为未来免疫治疗策略的优化提供了新方向。
01
研究背景
癌症相关成纤维细胞(CAF)是肿瘤组织、器官和组织中数量最多的细胞,对肿瘤的生长、侵袭和耐药性有重大影响。CAF对肿瘤免疫的影响也受到了极大关注。CAFs不仅通过PD-L1/PD1协调受体轴直接阻碍T细胞的抗肿瘤功能,还能上调肿瘤细胞中PD-L1的表达,促进免疫逃避。然而,在胰腺癌小鼠模型中靶向清除α-SMA CAFs后,肿瘤生长不仅没有被抑制,反而加速了,TME内的免疫抑制细胞浸润也增加了,这表明CAFs在维持抗肿瘤免疫反应中也起着至关重要的作用。
02
肿瘤内apCAFs基线可预测免疫疗法的临床疗效
在免疫治疗前后,应答者的成纤维细胞中apCAFs特征表达均高于非应答者。此外,免疫治疗后,应答者在成纤维细胞中的apCAFs特征表达量进一步增加,而非应答者中没有观察到这种情况。这些发现表明,apCAFs参与了肿瘤对免疫疗法的反应,可作为TNBC免疫疗法反应的潜在生物标志物。此外,在接受抗PD1或抗PD1联合抗CTLA4治疗的黑色素瘤患者中,应答者的apCAFs特征明显高于非应答者,而且apCAFs特征可以预测免疫治疗应答。在接受抗PD1治疗的非小细胞肺癌(NSCLC)患者中,也观察到了类似的结果。这些发现支持了apCAFs作为泛癌症免疫疗法生物标志物的价值。
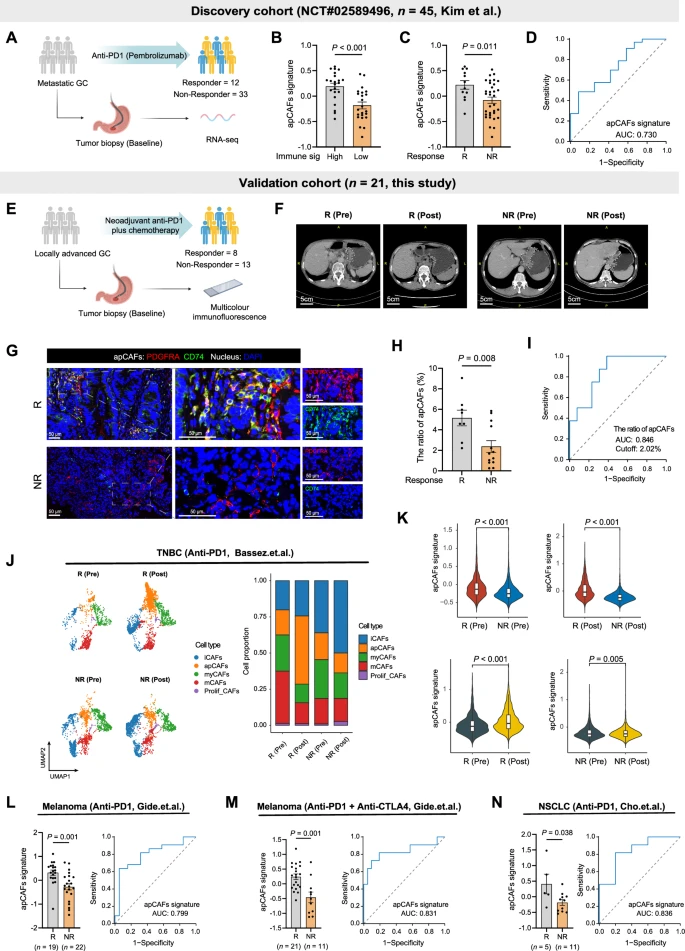
肿瘤内apCAFs基线可预测免疫疗法的临床疗效。
03
总结
1. apCAFs(抗原呈递癌症相关成纤维细胞)的发现:
研究首次确认胃癌(GC)中存在apCAFs,其特征为MHC II分子高表达和抗原呈递途径上调,与良好预后相关,并能激活抗肿瘤免疫反应,抑制肿瘤生长。
2. apCAFs在不同癌症中的作用:
在肺癌中,apCAFs通过与CD4 T细胞的TCR相互作用并产生C1q,保护T细胞免于凋亡;
在乳腺癌中,apCAFs的浸润与良好预后相关,但可能促进调节性T细胞(Treg)的产生,破坏抗肿瘤免疫;
在胃癌中,apCAFs的存在与Treg数量增加相关,可能因缺乏共刺激分子导致。
3. apCAFs与免疫治疗反应的关联:
ICB(免疫检查点阻断)治疗前,反应者中apCAFs的浸润高于无反应者;
ICB治疗后,反应者中apCAFs显著增加,而无反应者无此变化;
apCAFs可能作为免疫治疗反应的预测因子,其浸润水平与泛癌免疫治疗反应率相关。
参考资料:
1.Sung, H. et al. Global cancer statistics 2020: GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries. CA Cancer J. Clin. 71, 209–249 (2021).
2.Smyth, E. C. et al. Gastric cancer. Lancet 396, 635–648 (2020).
 腾讯登录
腾讯登录








还没有人评论,赶快抢个沙发