靶向治疗肺癌,参与DNA甲基化,从表观遗传学水平抑制肿瘤基因表达
| 导读 | 非小细胞肺癌是世界范围内导致癌症致死的主要杀手,应用拓扑异构酶II抑制剂依托泊苷只对一小部分患有非小细胞肺癌的病人具有良好疗效,因此,改变药物作用靶点愈来愈成为药物治疗该疾病的重中之重。 |
非小细胞肺癌是世界范围内导致癌症致死的主要杀手,应用拓扑异构酶II抑制剂依托泊苷只对一小部分患有非小细胞肺癌的病人具有良好疗效,因此,改变药物作用靶点愈来愈成为药物治疗该疾病的重中之重。之前有研究表明,EZH2能与PRC2共同作用对H3K27进行三甲基化,从而起到基因沉默的作用,因此甲基转移酶EZH2成为一个非常具有应用前景的潜在作用靶点。[1]
昨日,马克斯德尔布卢克分子医学中心(Max Delbrück Center for Molecular Medicine)分子肿瘤研究小组领导的一项研究发现:Ezh2抑制剂与抗炎药联合应用可显著抑制肺癌发展,该研究结果发表在《JEM》杂志。[2]

EZH2基因编码的是一种组蛋白赖氨酸N-甲基转移酶,参与DNA甲基化从而抑制其他基因转录,EZH2通过参与组蛋白甲基化过程可以从表观遗传学水平抑制肿瘤抑制基因的表达。抑制EZH2活性可以激发肿瘤抑制基因的表达,从而抑制肿瘤细胞生长。
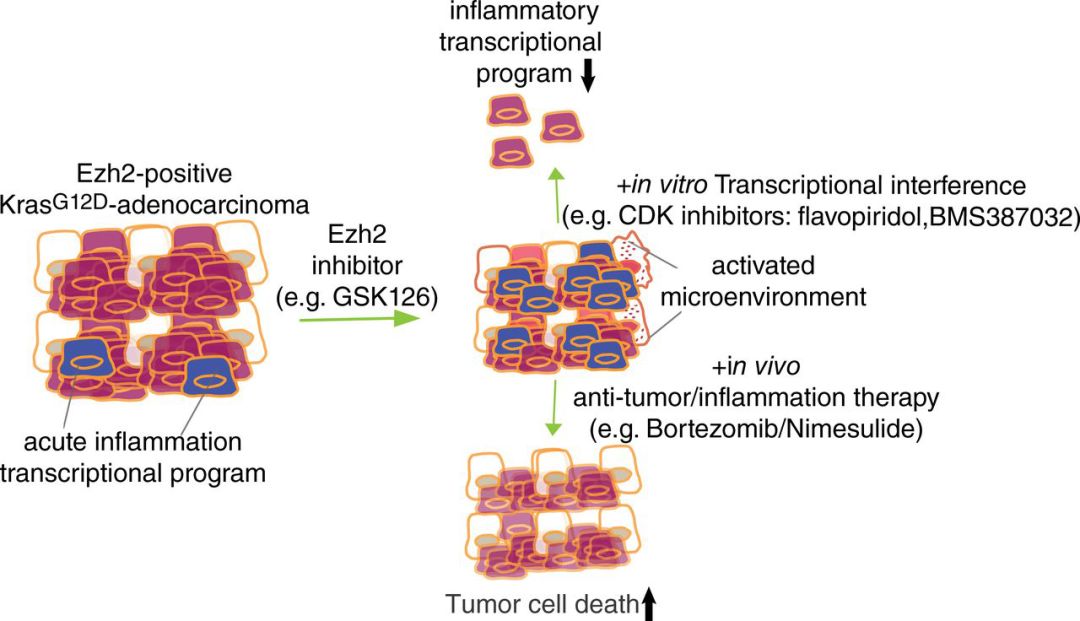
实验最初,实验组小鼠在注射Ezh2抑制剂后确实表现出与预期一样的作用效果,抑制了肿瘤细胞的增殖,从而使癌症得到控制。
但研究人员发现随着时间的推移Ezh2抑制剂的作用愈来愈弱,不仅如此,实验组小鼠还表现出炎症反应,雪上加霜的是,这些反应貌似支持着肿瘤的生长。这一系列的反应带来的后果便是:剩下的癌细胞变得更加具有侵略性。
基于以上发现,研究人员随后在上述基础上给老鼠注射了一种消炎物质——肺癌小鼠竟真地停止了发展。
表观遗传异常是肿瘤发生发展的重要根源,其中组蛋白甲基转移酶EZH2是表观遗传领域备受关注的抗肿瘤治疗靶点,已有多个抑制剂处于临床研究。但之前的研究证据均表明,EZH2抑制剂仅对个别血液系统肿瘤具有一定的治疗效果,对实体瘤治疗基本无效,从而极大地限制了这类抑制剂的临床研究与应用空间。
而MDC的研究给相关科研人员以踌躇满志,要使患者从这些新的治疗策略中获益,未来还有很长的路要走。有必要寻找生物标记物,使临床科学家能够清楚地预测这种策略在哪些患者身上会真正有效。
近年来,对非小细胞肺癌的研究可谓是愈来愈热,上个周,加州大学旧金山分校的Khyati Shah和 Sourav Bandyopadhyay等发现,极光激酶参与了非小细胞肺癌对EGFR抑制剂的耐药过程,联合使用EGFR抑制剂和极光激酶抑制剂,在小鼠中可以增强疗效,推迟耐药。这项研究发表在《自然医学》上。[3]
以上研究的发现突破现有认识局限,有望将EZH2抑制剂的应用推广到EZH2高表达的实体肿瘤,极大地拓展了这类抑制剂的临床应用空间。
重要的是,该项研究首次提出Ezh2抑制剂与抗药药物的联合应用,有望实现较广范围覆盖EZH2高表达肿瘤群体的精准治疗方案,同时为其他类型表观遗传抑制剂的个性化治疗提供了成功范例,具有普遍的指导意义。
参考文献
[1]Fillmore CM, Xu C, Desai PT, et al. EZH2 inhibition sensitizes BRG1 and EGFR mutant lung tumours to TopoII inhibitors. Nature. 2015 Jan 28.
[2] Michela Serresi, View ORCID ProfileBjorn Siteur, zh2 inhibition in Kras-driven lung cancer amplifies inflammation and associated vulnerabilities.Journal of Experimental Medicine,2018
[3]SHAH K N, BHATT R, ROTOW J, et al. Aurora kinase A drives the evolution of resistance to third-generation EGFR inhibitors in lung cancer[J]. Nature Medicine, 2018.
(转化医学网360zhyx.com)
 腾讯登录
腾讯登录









还没有人评论,赶快抢个沙发