2018鼻咽癌年终盘点 | 免疫治疗初露锋芒
| 导读 | 主要包括基因分子标签的提出、对第八版分期预后的再探讨、综合治疗中化疗方案的优化以及免疫治疗等.其中,以PD-1单抗为代表... |
回首2018年,鼻咽癌治疗在多方面均取得了不菲的成绩,主要包括基因分子标签的提出、对第八版分期预后的再探讨、综合治疗中化疗方案的优化以及免疫治疗等。其中,以PD-1单抗为代表的免疫治疗最为引人注目,其在复发转移鼻咽癌的治疗中初露锋芒,或将成为新一年发展的大势。

马骏教授
基因分子标签有望指导临床治疗
TNM临床分期是判断预后、指导治疗的金标准,然而单纯基于解剖学信息的TNM分期不能反映肿瘤个体间的生物学异质性,因此加入分子指标有望补充临床分期的不足。2018年2月,中山大学肿瘤防治中心马骏教授团队在《柳叶刀·肿瘤学》(Lancet Oncol)上发表的研究显示,由13个基因组成的分子标签可以预测鼻咽癌患者的无远处转移生存期,同时还可以筛选同期化疗获益人群。研究结果表明,低转移风险组患者可以从同期化疗中获益,5年远处转移率从16%降至5%;而高风险组患者5年远处转移率则无显著改善,提示此类患者可能需要进一步强化治疗。纳入基因表达谱和N分期等构建的列线图预后模型能够精准预测鼻咽癌个体的转移风险,将预测准确性由57%升至75%(图1)。
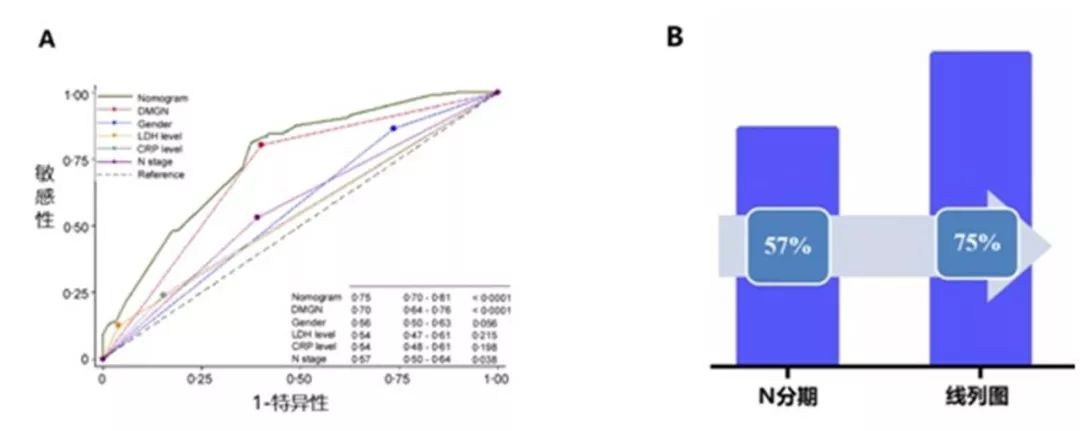 图1. 13个基因分子标签和临床指标构建的列线图可提高鼻咽癌患者远处转移风险预测的准确性
图1. 13个基因分子标签和临床指标构建的列线图可提高鼻咽癌患者远处转移风险预测的准确性
EBV DNA或将纳入临床分期系统
近期研究显示,EBV DNA与鼻咽癌患者的肿瘤负荷、肿瘤分期和生存率有关,治疗前中后EBV DNA检测已广泛应用于临床初步诊断及预后判断。马骏教授团队利用979例初诊无转移鼻咽癌患者构建的RPA模型,获得了2000copy这一预后截点,并建立了基于EBV DNA及解剖学信息的新分期模型。在550例患者中前瞻性抽样验证发现,新分期系统在风险一致性、区分性、预后预测能力以及样本量均衡性等方面均优于第八版TNM分期(图2)。来自香港的Lee AW 教授团队也证实,在现有分期中加入EBV DNA能优化对预后的预测。
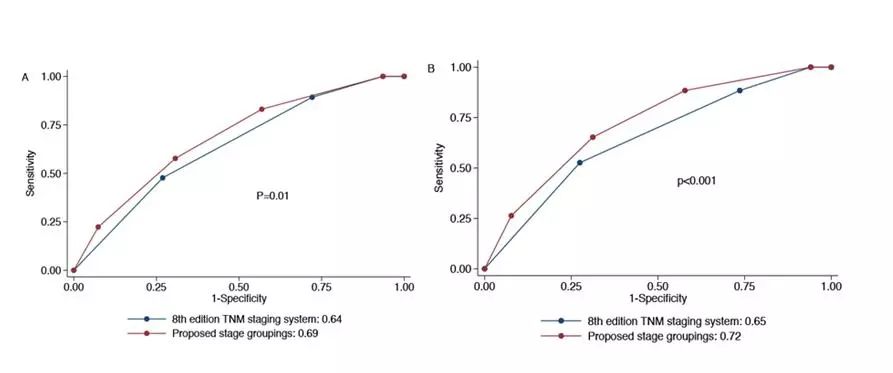 图2. 采用EBV 2000copy联合解剖分期构建模型对比UICC第八版分期在550例鼻咽癌患者中进行前瞻性验证的ROC曲线。A. 无进展生存(PFS);B. 总生存(OS)
图2. 采用EBV 2000copy联合解剖分期构建模型对比UICC第八版分期在550例鼻咽癌患者中进行前瞻性验证的ROC曲线。A. 无进展生存(PFS);B. 总生存(OS)
高危患者辅助化疗惹争议
1. NPC-9901/9902:支持在放疗基础上加用“同期-辅助化疗”治疗Ⅲ-Ⅳb期鼻咽癌
2018年8月Lee AW 教授团队在《国际放射肿瘤学·生物学·物理学杂志》(Int J Radiat Oncol Biol Phys)上发表了NPC-9901和NPC-9902联合分析的十年长期随访结果。这两项临床试验基于INT-0099实验设计,共纳入441名Ⅲ-Ⅳb期(基于第五版AJCC/UICC分期)非角化鼻咽癌患者。对照组接受单纯放疗,试验组接受同期放化疗联合辅助化疗。同期化疗为顺铂100mg/m2,每三周一程,共3程;辅助化疗为顺铂80mg/m2,氟尿嘧啶1000mg/m2连用4天,每四周一程,共3程。经过中位13.9年的随访,研究结果证实了放化疗组的治疗获益,10年无病生存(DFS)率(62% 对比52%,P=0.016),10年OS率(60% 对比50%,P=0.044)。生存获益主要得益于局部区域控制的改善,而在远处转移控制上未见统计学差异,10年无远处转移生存率(69% 对比66%,P=0.25)。在远期毒性反应(3级及以上)方面,两组未见明显差异(图3)。与3程同期化疗相比,2程同期化疗在生存上无统计学差异,但耳毒性的发生率明显降低;除此之外,同期及辅助期间的化疗药物(顺铂或氟尿嘧啶)的累积剂量是肿瘤控制的独立预后因素。这项研究进一步证实同期联合辅助化疗可以使局部区域晚期的鼻咽癌患者获得长期生存获益,且不会增加晚期毒副反应。但该研究中绝大部分患者采用的是二维或三维放疗技术(99.3%),在调强放疗时代,以上研究结论的推广需谨慎求证。
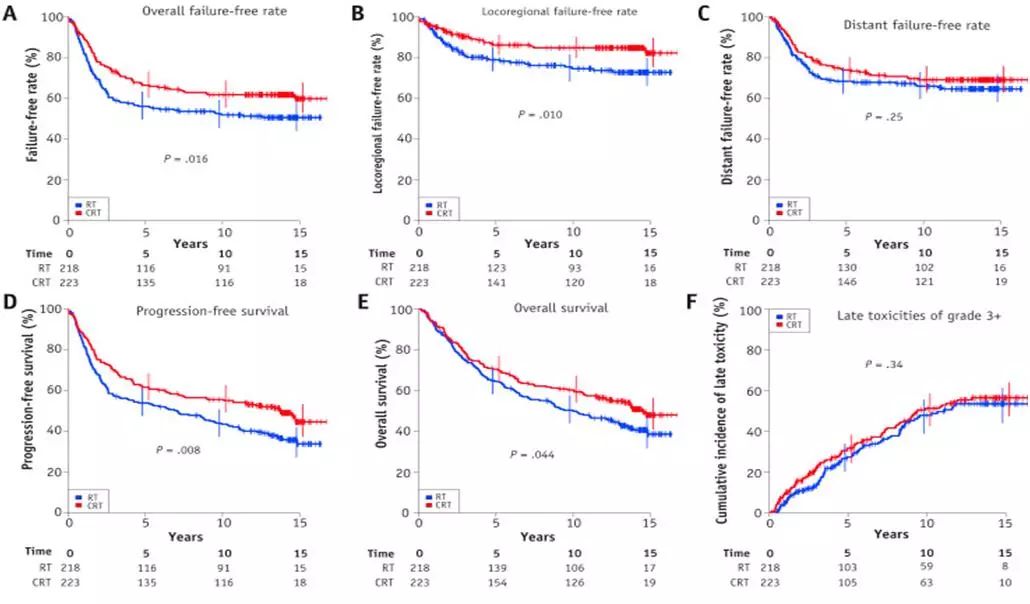
图3. NPC-9901/9902研究结果。A-E. 生存曲线;F. 晚期毒性反应
2. 0502试验:放疗后血浆EBV-DNA阳性的Ⅱb-Ⅳb期鼻咽癌患者不能从辅助化疗中获益
2018年7月,Chan ATC教授团队在临床肿瘤学杂志(J Clin Oncol)上发表了香港鼻咽癌研究组0502试验的研究结果。这项随机对照试验首先对789名完成了根治性放疗或放化疗的Ⅱb-Ⅳb期(基于第六版AJCC/UICC分期)鼻咽癌患者进行筛选,共入选104名放疗后血浆EBV-DNA为阳性的患者。将其随机分配至临床观察组和辅助化疗组。辅助化疗方案是顺铂40 mg/m2+吉西他滨1000 mg/m2,d1,d8,每三周一程,共6程。经过中位6.6年的随访,辅助化疗组与观察组的生存之间未发现统计学差异,5年DFS率(49.3% 对比54.7%,P=0.75),5年OS率(64.0% 对比67.8%,P=0.79;图4),提示辅助化疗不能使此类高危患者在生存方面获益。研究者认为,顺铂同期化疗后,潜在亚临床病灶对铂类药物的耐药性或许是导致阴性结果的原因之一。该随机对照研究以分子指标血浆EBV-DNA做分层因素指导鼻咽癌患者的治疗决策,是第一个公开发表的此类研究,也是鼻咽癌迈向个体化治疗的重要一步,尽管是阴性结果,依然具有重要科学意义。
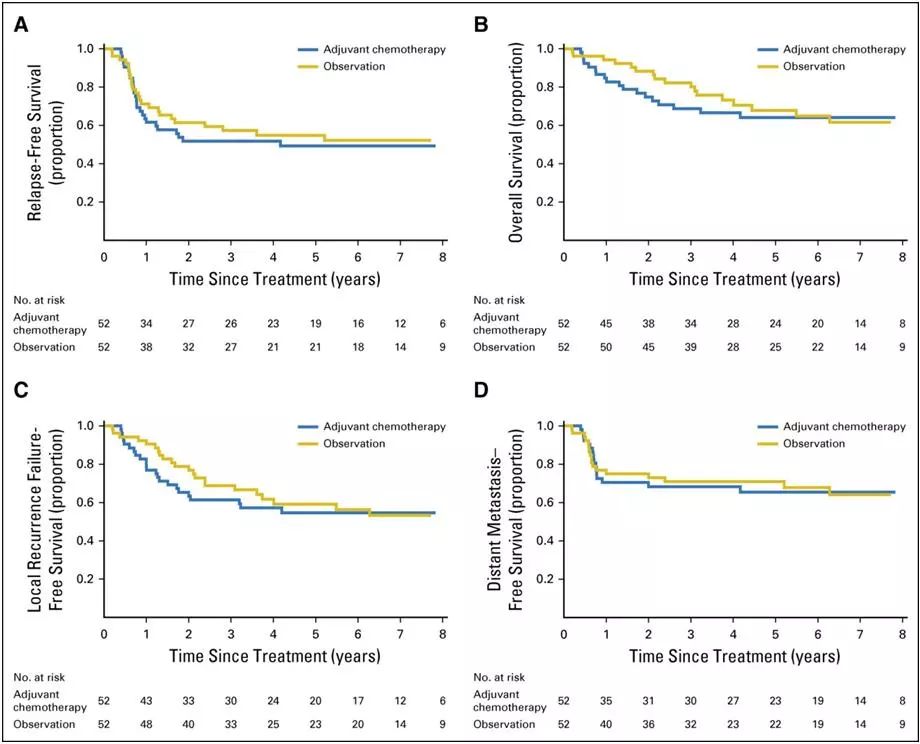
图4.香港鼻咽癌研究组0502试验生存曲线。
化疗方案的优化
顺铂方案的同期放化疗一直是局部晚期鼻咽癌患者的标准治疗方案,但是顺铂化疗会引起频繁的恶心、呕吐、肾毒性等副作用,严重影响患者的生活质量。2018年3月,中山大学肿瘤防治中心麦海强教授团队在《柳叶刀·肿瘤学》(Lancet Oncology)上发表了一项“奈达铂对比顺铂同期放化疗治疗局部晚期鼻咽癌”的非劣效、开放随机对照Ⅲ期临床试验(研究号NCT01540136)。该研究入组402例Ⅱ-Ⅳb期的鼻咽癌患者,顺铂和奈达铂同期放化疗组各201例。研究结果显示,顺铂同期放化疗组与奈达铂同期放化疗组的两年PFS率无统计学差异(89.9% 对比 88.0%);除此以外,两组OS率、无远处转移生存率及无局部区域复发生存率也无统计学差异。然而应用奈达铂所引起的恶心、呕吐、食欲减退等化疗相关的急性毒副反应发生率均比顺铂减少约20%,严重呕吐(3~4级)的发生率从18%降至6%。该研究证实奈达铂放化疗方案毒副反应更低,患者生活质量更好。
此外,2018年中国临床肿瘤学会(CSCO)年会上中山大学肿瘤防治中心郭翔教授团队汇报了一项“IMRT联合洛铂+5-FU对比顺铂+5-FU治疗局部中晚期鼻咽癌” 的Ⅲ期多中心、开放、随机对照临床试验。研究入组Ⅲ-Ⅳb期初诊鼻咽癌患者,试验组采用洛铂+5-FU诱导化疗序贯洛铂30 mg/m2每三周方案同期化疗,对照组采用顺铂+5-FU诱导化疗序贯顺铂100 mg/m2每三周方案同期化疗,初步结果显示,两组生存方面无显著差异,而试验组在化疗毒性方面显著优于对照组。
再程放疗患者危险分层
针对鼻咽癌复发患者,再程放疗能获得较好的肿瘤控制,但严重毒性不容忽视。2018年临床肿瘤学杂志(J Clin Oncol)上发表了一项关于局部复发鼻咽癌再程放疗的预后评分模型的研究,探讨如何根据该模型选择合适的患者接受再程放疗。该项研究由中山大学肿瘤防治中心的韩非教授团队和新加坡国家癌症中心Melvin L. K. Chua教授团队合作完成。该研究发现患者年龄、复发肿瘤体积、复发T分期(T3-4 对比T0-2)、首程放疗毒性(是否有≥3级的毒性)、再程放疗剂量(≥68 Gy 对比<68 Gy)是再程放疗疗效的独立预后因素。利用这些因素建立的预后评分模型将患者分为低危组和高危组。对于低危组,再程放疗可使肿瘤得到较好控制,且放疗副作用低,建议行再程放疗;而对于高危组,再程放疗疗效不理想,且副作用较严重,治疗方案的选择仍面临挑战。该模型为个体化治疗策略的选择及社会医疗资源的优化配置奠定了基础。
免疫治疗方兴未艾
以PD-1/PD-L1免疫检查点抑制剂为主的免疫治疗引领了鼻咽癌治疗领域的重大突破,革新了鼻咽癌的治疗体系。今年共有两项研究PD-1单抗的重要研究正式发表,为免疫治疗在鼻咽癌中的应用提供了更多证据。
来自香港中文大学的Brigette Ma教授报告了纳武利尤单抗(nivolumab)在一线治疗后复发或转移鼻咽癌中安全性与疗效的一项Ⅱ期试验,该研究发现nivolumab的客观反应率(ORR)为21%,1年OS率及PFS率分别为59%和19%,同时具有较好的安全性。而来自中山大学肿瘤防治中心的张力教授在《柳叶刀·肿瘤学》(Lancet Oncol)上报告了两项具有重要意义的Ⅰ期试验,分别探索了国产PD-1单抗SHR-1210单药治疗一线化疗失败后的晚期鼻咽癌的Ⅰ期临床研究和PD-1单抗联合化疗一线治疗晚期鼻咽癌的Ⅰ期临床研究,并评价了其安全性及有效性。该研究显示,单药治疗组患者最佳总体有效率为34%,疾病控制率为59%;PD-1单抗单药治疗引起的3度及以上严重不良反应发生率均较低。联合治疗组的总体有效率达到可观的91%,疾病控制率甚至高达100%,而毒性以化疗毒性为主,基本可控。另外今年有两项研究,PD-1单抗在局部晚期鼻咽癌中辅助化疗或联合诱导+同期化疗的试验正式启动(NCT03427827和NCT03700476),其结果可为免疫治疗在鼻咽癌中的应用提供更多证据。
然而我们也应注意到,免疫治疗在鼻咽癌临床应用中仍存在有效率偏低的问题,目前晚期鼻咽癌中的有效率仅约20%~30%,大多数患者并未从中获益。我们亟需寻找有效的免疫治疗疗效标志物,筛选出获益人群。目前鼻咽癌免疫治疗临床试验在PD-L1表达、HLA-A/B、肿瘤突变负荷、治疗前后EBV DNA拷贝数、EBV DNA清除率等指标中均未发现有效指标。由于鼻咽癌的突变数较少,且为EBV感染相关肿瘤,PD-L1表达与肿瘤浸润淋巴细胞水平均较高,基于免疫分子标签的基因表达进行分型,从而筛选获益患者,或可为鼻咽癌的精准免疫治疗提供新思路。马骏教授团队基于全基因组表达谱建立了针对头颈部肿瘤的免疫分子分型(免疫激活型、免疫耗竭型和非免疫型),并证实了免疫激活型患者预后最好且从免疫治疗中获益最大。该研究为未来头颈部肿瘤免疫治疗标志物及新型靶点的发展指明了方向。我们期待未来预测效果更优的免疫分子分型体系的建立能够进一步指导鼻咽癌的临床免疫治疗。(转化医学网360zhyx.com)
 腾讯登录
腾讯登录






还没有人评论,赶快抢个沙发