《Nature》子刊:肠道微生物与免疫检查点抑制剂双剑合璧,抑制黑色素瘤发展,科学大发现!
| 导读 | 近日,《Nature》杂志再次将肠道微生物推上热点。坐实人体肠道共生微生物对癌症免疫治疗的重大影响,肠道微生物与免疫系统双剑合璧为肿瘤免疫治疗谱写了新蓝图。 |
近日,《Nature》杂志再次将肠道微生物推上热点。坐实人体肠道共生微生物对癌症免疫治疗的重大影响,肠道微生物与免疫系统双剑合璧为肿瘤免疫治疗谱写了新蓝图。

由桑福德·伯纳姆·普雷比斯医院的研究人员领导的40多名科学家和三所医院组成的研究团队在著名期刊《Nature Communications》上详细阐述了肠道菌和癌症免疫治疗之间的关系。
研究人员发现了11种细菌的混合物,这种细菌混合物可以激活小鼠的免疫系统并减缓黑色素瘤的生长速度。
免疫系统是控制肿瘤的主导力量,免疫监视功能低下可导致肿瘤发生、发展。近年来,肿瘤免疫治疗开辟了肿瘤治疗的新方向,然而除了微卫星高度不稳定患者外,获益人群仍不明确。目前报道的程序性细胞死亡蛋白配体1(programmed cell death protein 1 ligand 1, PD-L1)的免疫组化表达和肿瘤突变负荷均无法明确预测免疫检查点抑制剂(immune checkpoint inhibitors, ICIs)的疗效。有研究指出,肠道微生态参与了肿瘤的发生、发展,并影响肿瘤免疫治疗效果。肠道菌群被认为是一个潜在的可预测肿瘤免疫治疗效果的生物标志物,因此,调控肠道微生态也成为了免疫治疗的一个部分。
癌症免疫疗法尤其依赖于正确细菌的存在,曾有研究显示,服用过抗生素的患者在接受PD-1抑制剂治疗后,癌症很快出现复发,生存时间显著缩短,人体的肠道菌群紊乱也将大大降低PD-1抑制剂的药效。如果将对免疫治疗反应良好患者的粪便移植到无菌小鼠体内,无菌小鼠的治疗效果将会得到提高。
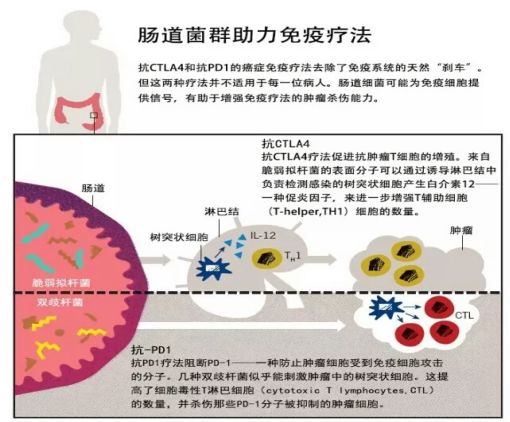
如今,“免疫疗法”和“肠道微生物”迎头相撞,擦出了一道令科学家们兴奋的火花。科学家研究发现肠道微生物(至少在老鼠体内)显著影响免疫系统对付癌症的能力:这些微生物影响个体对癌症的自然免疫能力以及个体对免疫治疗药物的应答;某些种类的细菌能有效地驾驭个体的抗肿瘤免疫力。
而在种种迹象的背后,研究人员发现了这其中的关键物质--UPR(未折叠蛋白反应),这是一种维持蛋白质健康(动态平衡)的细胞信号通路。在该研究中,对免疫检查点治疗有反应的黑色素瘤患者中UPR水平显著减少。这表明,UPR在肠道微生物群与抗肿瘤免疫之间具有重要相关性。宿主微生物群在检查点阻断免疫治疗功效中具有因果作用,这一发现有助于选择对治疗有反应的患者,指导个体化免疫治疗。
基于以上发现,Ronai和他的团队进一步研究了缺乏RING指蛋白5(RNF5)基因的遗传小鼠模型,RNF5是一种泛素连接酶,有助于去除不适当折叠或受损的蛋白质。结果发现,在具有完整的免疫系统和肠道微生物组的前提下,缺乏RNF5的小鼠能够抑制黑色素瘤的生长。通过对实验组小鼠肠道微生物的提取,发现了11种细菌菌株,有趣的是,将这11种细菌菌株转移到缺乏肠道细菌(无菌)的小鼠中,竟也能诱导抗肿瘤免疫应答并减缓肿瘤生长。

当然,仅限于动物模型的科学发现终归是残缺的,为了探索该机制在人类中的有效性,科学家们从三组患有转移性黑色素瘤的人群中获得了组织样本,这些人随后接受了检查点抑制剂治疗,长期追踪随访发现,对免疫检查点抑制剂反应较好的患者生存期明显长于对免疫检查点抑制剂反应较差的患者。实际上,UPR组分(sXBP1,ATF4和BiP)的表达降低与对治疗的反应性相关,这表明,对于应该接受免疫检查点治疗的患者的来说,存在潜在的预测性生物标志物。
接下来,科学家们计划研究细菌的产生速度,从而有目的性地减缓肿瘤生长。来评估它们增强抗肿瘤免疫力的能力。
然而,不可避免的是,缺乏RNF5的小鼠也容易发生肠道炎症 - 这是某些免疫检查点疗法的副作用 - 我们可以利用这一模型来研究如何在自身免疫和抗肿瘤免疫之间取得平衡,这可能有助于更多患者从中受益。
参考文献:
Yan Li, Roberto Tinoco,Gut microbiota dependent anti-tumor immunity restricts melanoma growth in Rnf5−/− mice(转化医学网360zhyx.com)
 腾讯登录
腾讯登录









还没有人评论,赶快抢个沙发