寻根溯源——蛋白基因组研究全面剖析结直肠癌
| 导读 | 近日,贝勒医学院的研究人员利用基因组蛋白组学相结合的分析技术首次对结肠癌的蛋白基因组进行了详尽的分析,全面剖析了结直肠癌相关生物标志物、药物靶点和肿瘤抗原,有助于系统地确定该肿瘤的新型治疗机会。 |
作者:Ruthy 编辑:Carrie
近日,贝勒医学院的研究人员利用基因组蛋白组学相结合的分析技术首次对结肠癌的蛋白基因组进行了详尽的分析,全面剖析了结直肠癌相关生物标志物、药物靶点和肿瘤抗原,有助于系统地确定该肿瘤的新型治疗机会。
随着我国迈入老龄化社会的脚步加剧,加之人们生活方式的改变,结直肠癌发病率和死亡率正在逐年上升,为患者、家庭和社会带来了巨大的身心及经济负担。
随着基因组学、蛋白质组学技术的发展,在基因与蛋白层面上阐述结直肠癌的发病机制,进而提高早期诊断和治疗能力并非天方夜谭。然而,快速积累的组学数据尚未将新的生物标志物和药物靶标带入临床。
近日,贝勒医学院的研究人员利用基因组蛋白组学相结合的分析技术首次对结肠癌的蛋白基因组进行了详尽的分析,全面剖析了结直肠癌相关生物标志物、药物靶点和肿瘤抗原,有助于系统地确定该肿瘤的新型治疗机会。

SOX9——于结直肠癌中的过表达并非意外
研究人员比较了结肠癌肿瘤组织与临近的健康组织,并进行了蛋白组学和磷酸化蛋白质组学的队列分析。SOX9是一个在许多实体肿瘤中发生异常表达的转录因子,大量数据显示SOX9在结直肠癌中显著过表达,与结直肠癌低生存率、不良预后及对某些化疗药物的敏感性降低有关,有望成为有价值的诊断、评估标志和治疗靶点。我们知道,SOX9表达量的高低在不同类型的肿瘤中有不同的体现,在结直肠癌中,SOX9是作为癌性基因存在。这是为什么呢?
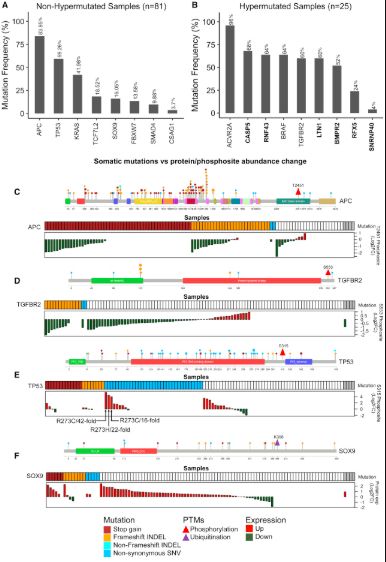
结直肠癌细胞突变及其蛋白质组学分析结果
研究人员发现,结直肠癌中SOX9不仅过表达,还有多种突变同时存在,包括六个停止增益突变,八个移码突变和五个非同义SNV,且多为截短突变。大多数截短突变发生在HMG-box结构域的下游和进化上保守的遍在蛋白靶点K398的上游,这就导致SOX9的26S蛋白酶体依赖性降解。这些截短突变可以去除K398遍在蛋白化位点,从而稳定SOX9蛋白并增加蛋白质丰度,最终导致结直肠癌中SOX9显著过表达,进而影响肿瘤大小、远处转移预后。也就是说,SOX9于结直肠癌中过表达并非意外,而是有迹可循,如何控制这些截短突变的作用将是结直肠癌治疗的新课题。
Rb磷酸化——结肠癌的重要驱动和治疗靶点
Rb是一种肿瘤抑制基因,是最早发现的抑癌基因,其在大多数肿瘤组织中多呈缺失和频繁突变状态,但其在结直肠癌中却是明显的过表达!而其过表达并未发挥应有的抑癌作用,反而很大程度上促进了结直肠癌的发生发展。这又是为何呢?
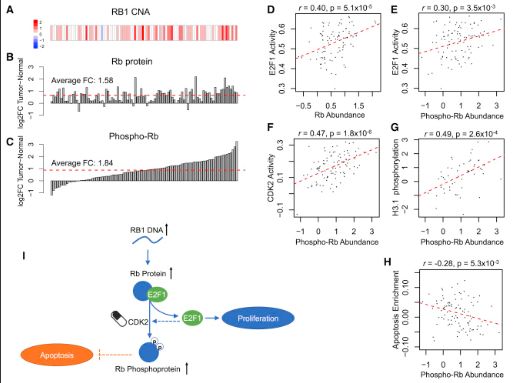
Rb磷酸化作为结肠癌的重要驱动和治疗靶点
正常情况下,Rb是通过抑制E2F转录因子来阻止细胞增殖,而在结直肠癌细胞中,Rb发生了特殊的修饰——磷酸化。研究人员在结直肠癌样品中发现了6个Rb磷酸化位点,而样品中E2F转录因子明显增强,因此,样品中Rb总量增加应归因于磷酸-Rb,而且E2F1活性与磷酸化Rb之间存在正相关的正反馈通路。E2F1转录增加可上调细胞周期蛋白E,激活CDK2,从而磷酸化Rb,而Rb被磷酸化后又进一步解除了其对E2F1的抑制。
进一步分析显示,结直肠癌中Rb磷酸化的变化与凋亡标志基因组呈负相关,也就是说,磷酸-Rb具有抗细胞凋亡作用,可以阻止细胞凋亡,使细胞获得“不死之身”。目前已有多种CDK2抑制剂在研,这些成果证明了Rb磷酸化可作为结肠癌的重要驱动和治疗靶点,开辟了利用CDK2抑制剂阻断Rb磷酸化,进而治疗结直肠癌的新型抗癌道路。
此外,研究人员还指出MSI亚型的结直肠癌中糖酵解增加与免疫抑制相关,提出免疫检查点抑制剂和糖酵解抑制剂的组合疗法有望成为存在单一阻断剂抗性的MSI肿瘤患者的有效治疗策略。虽然这些治疗假设尚未应用于临床,但其有望在结肠癌的分子引导精确治疗方面取得实质性进展,这是相关治疗的新希望,对结直肠癌患者而言无疑是巨大福音。
参考文献:
Suhas Vasaikar,et al.Proteogenomic Analysis of Human Colon Cancer Reveals New Therapeutic Opportunities.Cell.
推荐内容

(转化医学网360zhyx.com)
 腾讯登录
腾讯登录









还没有人评论,赶快抢个沙发