“癌中之王”胰腺癌近期研究进展一览
| 导读 | 被称为“癌症之王”的胰腺癌是一种恶性程度很高,诊断和治疗都很困难的消化道恶性肿瘤,约90%为起源于腺管上皮的导管腺癌。其发病率和死亡率近年来明显上升。5年生存率极低,是预后最差的恶性肿瘤之一。胰腺癌早期的确诊率不高,手术死亡率较高,而治愈率很低。我们所熟知的乔布斯、帕瓦罗蒂、沈殿霞都是因为这一疾病去世的。 |
被称为“癌症之王”的胰腺癌是一种恶性程度很高,诊断和治疗都很困难的消化道恶性肿瘤,约90%为起源于腺管上皮的导管腺癌。其发病率和死亡率近年来明显上升。5年生存率极低,是预后最差的恶性肿瘤之一。胰腺癌早期的确诊率不高,手术死亡率较高,而治愈率很低。我们所熟知的乔布斯、帕瓦罗蒂、沈殿霞都是因为这一疾病去世的。对它,医学工作者们一直在寻找对抗之法,这篇文章就为大家介绍今年胰腺癌研究及治疗进展。
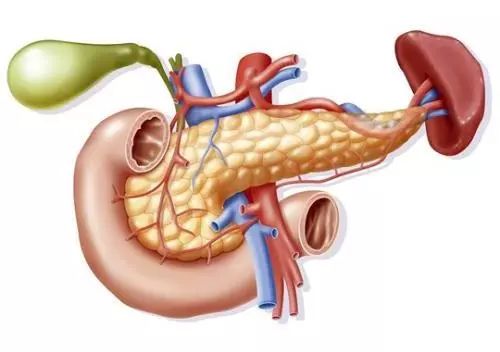
——检 测 类——
舌苔菌群或将助力早期胰腺癌检测
Shusen Zheng, Lanjuan Li. Tongue coating microbiome data distinguish patients with pancreatic head cancer from healthy controls
发现人体肿瘤常见的方法包括医生的体格检查、肿瘤标记物筛查以及CT等影像学检查,当然还包括近几年发展较为迅速的“滴血验癌”。今年年初,来自浙江大学第一附属医院的研究团队给出了一种全新的验癌方式,只要查看受试者舌头中的菌群构成就能从正常人中区分出早期胰腺癌患者,这项研究的进展发表于《Journal of Oral Microbiology》杂志。
此研究共入组了30名早期胰腺癌患者(被诊断为胰头癌)和25名健康个体,年龄在45岁至65岁之间,没有其他疾病或口腔健康问题,在研究开始前三个月没有服用任何抗生素或其他药物。科研团队应用DNA测序技术分析入组人群的舌苔微生物组。
研究结果表明,健康对照人群的舌苔中,卟啉单胞菌和嗜血杆菌的相对丰富度显著高于早期胰腺癌患者,而纤毛菌和梭杆菌丰富度显著低于早期胰腺癌患者。
虽然已经在胰腺癌患者中发现了对身体其他部位微生物组的破坏,但这是首次发现胰腺癌会改变舌苔中细菌的变化。如果在更大规模的研究中得到证实,这可能为这种高度侵袭性疾病开发新的早期发现或预防治疗措施。
切除的Ⅰ~Ⅱ期胰腺癌中检及淋巴结数量新标准
https://mp.weixin.qq.com/s/GumyAoKpYUvjuR_T9xm2Aw
2019年ASCO年会上,来自海德堡大学海德堡医学院德国癌症研究中心的Dr. Lei Huang口头汇报了一项基于人群的大规模国际队列研究,该研究指出了在切除的Ⅰ~Ⅱ期胰腺癌中检及淋巴结数量(ELN)和准确分期及远期生存的关系,并进一步提出了ELN的最低和最优新标准。
该研究分析了来自于美国和荷兰于2003~2015年接受手术的共约2万例TNM I~II期原发侵袭性外分泌胰腺癌患者,运用稳健的统计学模型分析了这些真实世界队列,并进行了国际性内部和外部验证,是关于切除的I~II期PaC中ELN临床意义与界值点的最大研究,结果有很好的代表性和可推广性,为PaC治疗提供了重要的基于人群的质量标准数据参考。
对于身体条件允许可切除的PaC患者,切除原发肿瘤和局部淋巴结是根治性治疗的基础。淋巴结检测将可能有助于提高分期精确性和治疗效果。之前关于ELN和PaC远期生存的研究结果之间分歧巨大,且大多数有重要的局限性,如没有矫正混杂因素,缺乏分层分析及样本量有限等,而导致结果不稳定。ELN为癌症处理中重要的质量评估标准之一。
——治 疗 类——
PARP抑制剂有望一线治疗胰腺癌
https://www.astrazeneca.com/content/astraz/media-centre/press-releases/2019/lynparza-significantly-delayed-disease-progression-as-1st-line-maintenance-treatment-in-germline-brca-mutated-metastatic-pancreatic-cancer-26022019.html
今年2月,阿斯利康和默沙东联合开发的Olaparib (Lynparza,奥拉帕利)作为治疗携带种系BRCA基因突变(gBRCAm)的转移性胰腺癌患者的一线维持疗法,在3期临床试验中达到试验主要终点。这是第一款在3期试验中证明让gBRCAm转移性胰腺癌患者获益的PARP抑制剂。
参加此次试验的154名转移性胰腺癌患者都携带gBRCAm,且在此前的一线铂基化疗期间没有发生疾病进展。这些试验对象按3:2比例被随机分配,分别接受每日两次300 mg的Lynparza或安慰剂,作为一线维持疗法直至疾病进展。试验的主要终点是无进展生存期(PFS),关键的次要终点包括总生存期(OR),总体缓解率(ORR),疾病控制率,以及和与健康相关的生活质量。实验结果显示,与安慰剂相比,患者的PFS得到了统计学意义上显著的临床改善。
奥拉帕利是首个口服多聚二磷酸腺苷核糖聚合酶(PARP)抑制剂药物,作用机理是基于DNA修复损伤机制(DNA damage response,DDR)。奥拉帕利由阿斯利康开发,2017年7月27日,阿斯利康和默沙东公司达成一项肿瘤领域战略合作:共同推广全球首个领先的PARP抑制剂奥拉帕利。2018年10月,奥拉帕利被FDA授予“胰腺癌患者的孤儿药”称号。
——研 究 类——
胰腺癌原来是这样“找饭吃”的
Samir Hanash,Ronald A. DePinho, Giulio F. Draetta. Syndecan 1 is a critical mediator of macropinocytosis in pancreatic cancer
今年三月, 《Nature》杂志上发表的一篇文章中介绍,来自德州大学的Giulio Draetta教授及其同事发现了胰腺癌细胞表面的一种名为syndecan-1(SDC1)的蛋白质可以响应胞内KRAS的信号,并促进巨噬细胞的破坏作用。
“癌症之王”胰腺癌令人不寒而栗,而90%胰腺导管癌中存在KRAS突变。KRAS突变会通过尚不明确的机制激活肿瘤微环境的巨噬细胞,并促进巨噬细胞的胞吞作用。KRAS在胰腺导管腺癌中的高突变率导致患者的五年内生存率只有8%。为了研究KRAS与细胞膜的联系,研究人员设计了一种研究胰腺癌中KRAS分别处于开放和关闭状态下,细胞表面变化情况的模型。
研究人员发现,细胞表面的蛋白质对KRAS的表达产生了巨大的响应变化,而SDC1在KRAS通路开放时变化最为活跃。这提示KRAS可指导SDC1整合到细胞膜表面并发挥其功能。研究人员使用不同的方法来阻止SDC1整合到细胞膜中,其结果发现只有当SDC1表达于细胞表面才能激活巨噬细胞。研究人员有望利用这一通路开发出靶向SDC1的治疗方案。
目前,针对SDC1的单克隆抗体正在多发性骨髓瘤中进行测试,这一药物可能会开启胰腺癌类似疗法的临床研究”。了解胰腺癌细胞是如何“找饭吃”,再利用这一机制切断其能量供应,这可能是未来治疗胰腺癌的关键方案。
外泌体靶向ADAM9抑制胰腺癌的发展
Bone Marrow Mesenchymal Stem Cell-Derived Exosomal MicroRNA-126-3p Inhibits Pancreatic Cancer Development by Targeting ADAM9. Mol Ther Nucleic Acids.
前不久,在Molecular Therapy-Nucleic Acids杂志上发表的文章揭示了由骨髓间充质干细胞衍生的外泌体传递的miR-126-3p在胰腺癌进展中的作用,确定miR-126-3p可作为胰腺癌治疗的分子靶点。
基于资料,研究人员认为来自骨髓间充质干细胞(BMSC)外泌体中的miR-126-3p(miRNA的一种亚型)可通过下调去整合素金属蛋白酶9(ADAM9)来抑制胰腺癌的进展。首先,研究者筛选了一系列候选miRNA以及与胰腺癌相关的基因靶点,并用miR-126-3p转染PANC-1细胞或者沉默ADAM9,检测了miR-126-3p和ADAM9在胰腺癌细胞中的调节作用。进一步分离源自BMSC的外泌体并与胰腺癌细胞共培养后,阐明了外泌体在胰腺癌中的作用。此外,研究者通过慢病毒包装miR-126-3p的方式,在体内分析了BMSCs外泌体的过表达miR-126-3p对胰腺癌细胞的增殖、迁移、侵袭、凋亡、肿瘤生长和转移的影响。结果发现,来自于BMSCs的外泌体中,过量miR-126-3p抑制了胰腺癌细胞的增殖、侵袭和转移,并在体外和体内促进胰腺癌细胞的凋亡。这项研究表明,miR-126-3p具有作为胰腺癌治疗新型生物标志物的潜力。
胰腺癌疾病进展模式新机制被发现
TGFB1-induced autophagy affects the pattern of pancreatic cancer progression in distinct ways depending on SMAD4 status
近日,复旦大学研究团队在《自噬》上发表了一项关于胰腺癌疾病进展模式的研究新成果,即在胰腺癌驱动基因SMAD4不同状态下,细胞转化生长因子TGFB1所诱导的自噬作用不同,进而影响胰腺癌的增殖及转移能力。
SMAD4是胰腺癌最为主要的驱动基因之一,约有60%的胰腺癌患者存在SMAD4突变。相关研究表明,细胞转化生长因子TGFB1作为SMAD4信号通路中重要的信号分子,参与介导肿瘤的多种恶性生物学行为。
研究团队从TGFB1入手,发现在SMAD4阳性的胰腺癌细胞中,TGFB1诱导的自噬可以通过阻碍SMAD4入核,进而表现出促进肿瘤细胞增殖,抑制侵袭能力。与之相反,在SMAD4缺失的胰腺癌细胞中,TGFB1诱导的自噬通过调控MAPK/ERK通路的激活,发挥抑制增殖而促进侵袭的能力。后续,研究者在胰腺癌临床组织样本中发现并验证TGFB1的表达与自噬指标LC3B呈正相关。而在SMAD4缺失的胰腺癌患者中,LC3B高表达人群往往有着较差的预后,进一步也证实了TGFB1诱导的自噬参与影响了胰腺癌的疾病进展模式。
CA19-9:胰腺癌的“幕后黑手”
The glycan CA19-9 promotes pancreatitis and pancreatic cancer in mice
美国冷泉港实验室(CSHL)的研究人员发现CA19-9是导致胰腺炎和胰腺癌的罪魁祸首,靶向CA19-9有望成为防止胰腺炎和胰腺癌的新手段。
研究者利用转基因技术对小鼠进行改造,使其表达人CA19-9。结果发现CA19-9在小鼠体内的表达导致了表皮生长因子受体(EGFR)信号的过度激活,进而导致快速和严重的胰腺炎。EGFR信号通路异常与多种癌症的发生发展密切相关。因此,这种炎症加速了胰腺癌的进展。
研究人员表示,预防性干预胰腺炎可能预防高危患者发展成胰腺癌。因为胰腺炎是发展为胰腺癌所必需的,通过在动物模型中使用抗体靶向CA19-9,可以降低胰腺炎的严重程度,甚至可以防止胰腺炎的发生。据悉,德国生物技术公司BioNTech已经取得CA19-9抗体治疗和预防胰腺炎的专利许可。
叶茂/谭蔚泓团队阐明胰腺癌特异性核酸适体XQ-2d识别靶标的机制
https://pubs.acs.org/doi/10.1021/jacs.9b03720
近日,湖南大学叶茂/谭蔚泓团队在JACS发表了文章,系统地阐明了胰腺癌特异性核酸适体XQ-2d识别靶标的机制。(核酸适体(Aptamer)是从人工合成的DNA/RNA文库中筛选得到的能够高度特异性、高亲和性结合靶标分子的单链寡核苷酸。)
研究发现,转铁蛋白受体1(transferrinreceptor1,TfR1, CD71)是核酸适体XQ-2d识别胰腺癌细胞的分子靶标。通过计算生物学分析CD71和XQ-2d的结构,并进行模拟分子对接,发现CD71上有16个关键氨基酸残基介导了与XQ-2d的结合,而这些氨基酸残基也是CD71天然配体转铁蛋白(Transferrin,Tf)的结合位点,空间结构上的位阻解释了XQ-2d与转铁蛋白竞争性结合的分子基础。
CD71是II型的跨膜糖蛋白,能与含有铁离子的转铁蛋白结合,经网格蛋白内吞途径进入细胞,介导细胞对铁的吸收。研究表明,CD71不仅在胰腺癌中,而且在多种肿瘤中高表达,主要满足肿瘤细胞增殖对铁的需要。基于核酸适体XQ-2d与CD71的特异性结合,该研究进一步通过构建富含GC的XQ-2d嵌合体,装载传统化疗药物DOX,从而实现了化疗药物的靶向递送和胰腺癌的靶向治疗。
本研究是核酸适体识别靶标机制的系统性研究,为基于核酸适体的肿瘤标志物的发现以及肿瘤的诊疗提供了新的分子工具和新的策略。
谭蔚泓院士将出席今年的第二届上海国际癌症大会,届时将为我们分享他的观点,希望大家能积极报名参加大会呀~
(转化医学网360zhyx.com)
第二届上海国际癌症大会今年10月11~13日要召开。在大会上,研究者们将对免疫治疗、肿瘤微环境、代谢重编程、肿瘤标志物等主题进行热烈讨论,欢迎大家一起来聆听、分享自己的研究进展和见解~
(识别二维码报名,优惠即将结束,手快半价参会 )
)

 腾讯登录
腾讯登录









还没有人评论,赶快抢个沙发