B细胞带来危机与转机,黑素瘤免疫疗法将何去何从?
| 导读 | 黑色素瘤来源于黑色素细胞,高度恶性,已经成为严重危害人类健康的疾病之一。以免疫检查点阻断剂(ICBs)为代表的免疫疗法在人晚期黑色素瘤患者中疗效明显,但仍有约50%的患者对该类药物不敏感,而且部分患者在后续的治疗中产生耐药现象。 |
导 读:黑色素瘤来源于黑色素细胞,高度恶性,已经成为严重危害人类健康的疾病之一。以免疫检查点阻断剂(ICBs)为代表的免疫疗法在人晚期黑色素瘤患者中疗效明显,但仍有约50%的患者对该类药物不敏感,而且部分患者在后续的治疗中产生耐药现象。因此,破解疗效和耐药难题是当前黑色素瘤免疫治疗的重中之重,但相关研究多局限于T细胞。
近日,EMBL欧洲生物信息学研究所和维也纳医科大学的研究人员发现在黑色素瘤的免疫反应中,另一种重要免疫细胞B细胞同样扮演了重要角色。他们指出B细胞展示了显著的“左右互搏”的功能——既促炎又抗炎。而这正是黑色素瘤免疫治疗的危机与转机!

危机——肿瘤微环境(TME)炎症的维护者
机体的免疫功能与肿瘤的发生发展密切相关,免疫系统对肿瘤细胞有免疫监视和清除作用,而肿瘤细胞也会影响免疫系统的免疫应答。
在肿瘤的发生发展过程中,机体可通过固有免疫和获得性免疫识别和清除肿瘤细胞,而肿瘤细胞会通过多种途径逃避机体的免疫监视。其中,促进免疫抑制性细胞趋化到TME中是肿瘤免疫逃逸发生的主要原因。
TME包含肿瘤组织中各种细胞如肿瘤细胞、免疫细胞、成纤维细胞等,还包含这些细胞分泌的各种可溶性因子,以及代谢底物和代谢产物等等。TME的炎症反应和免疫抑制作用已被证实是免疫逃逸的主要影响因素,而追根溯源后发现,肿瘤相关B细胞(TAB)正是导致TME炎症的罪魁祸首之一!
小鼠癌症模型显示,部分TAB亚型可促进肿瘤TME炎症,而且可以抵抗肿瘤T细胞依赖的治疗反应。体内黑素瘤移植模型揭示了同基因小鼠中一些TAB缺乏或消耗可引起原发性抗肿瘤作用。更重要的是,B细胞免疫系统受损的小鼠模型TME中的炎症反应无法存在,所以无法形成完整的TME。研究人员发现,人黑素瘤细胞可释放FGF-2,诱导一些TAB分泌IGF-1,这是黑素瘤细胞对丝裂原活化蛋白激酶(MAPK)抑制剂获得性耐药的来源。MAPK抑制剂耐药性经常与TME中炎症和免疫细胞的浸润与极化共同演变。
同时,一系列临床数据表明,黑色素瘤终末期通过抗CD20抗体的使用或B细胞耗竭可产生意想不到的临床益处。这就意味着TAB是黑色素瘤免疫逃逸的重要帮手,也是免疫治疗的危机。
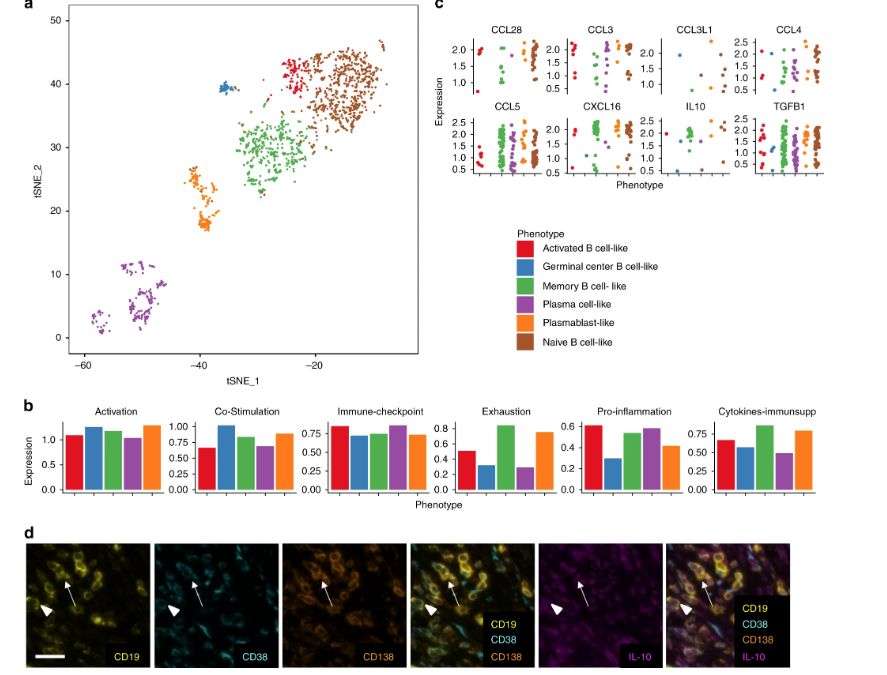
TAB的不同功能表型
转机——效应T细胞的“指明灯”
那是否只要破坏B细胞免疫系统就可以有效治疗黑色素瘤呢?当然不是。
研究人员指出黑色素瘤中TAB是T细胞的重要“引路人”。这是什么意思呢?他们发现,TAB是个“精分”,其不仅表达促炎物质,还同时表达抗炎因子。这些抗炎因子正是效应T细胞募集至关重要的趋化因子。
TAB的大量消耗的不仅仅是TME中的炎症因子,还有效应T细胞和其他免疫细胞。进一步的研究指出,一些TAB的特殊亚型可以将效应T细胞吸引入肿瘤阻止并加以保护,而且可以帮助激活T细胞的免疫作用。研究人员指出,治疗中这类B细胞亚型浓度越高,患者对免疫疗法的反应就越好。也就是说,TAB亦是黑色素瘤免疫治疗的重要转机!
TAB带来了危机,也带来了转机,该如何合理处置,最大限度发挥黑色素瘤免疫治疗的作用,让更多患者受益,是目前必须解决的问题。黑色素瘤细胞如何修饰B细胞、B细胞支持T细胞活化的机制都是需要深入了解的课题。
参考文献:
Johannes Griss,et al.B cells sustain inflammation and predict response to immune checkpoint blockade in human melanoma.Nature Communicationsvolume 10, Article number: 4186 (2019).

(转化医学网360zhyx.com)
 腾讯登录
腾讯登录









还没有人评论,赶快抢个沙发