Nature:非小细胞肺癌新药——靶向药AMG 510的庐山真面目!
| 导读 | 近日,美国、澳大利亚等多个医疗机构的研究人员报道提出了一种针对基因组突变蛋白的新型药物,并且在针对鼠的动物试验和前期临床首批给药组中已经被证明可有效抑制肿瘤的生长。 |
近日,美国、澳大利亚等多个医疗机构的研究人员报道提出了一种针对基因组突变蛋白的新型药物,并且在针对鼠的动物试验和前期临床首批给药组中已经被证明可有效抑制肿瘤的生长。相关研究发表于近日的《Nature》杂志中,该研究为缺乏有效治疗方法的癌症患者带来了新的希望。

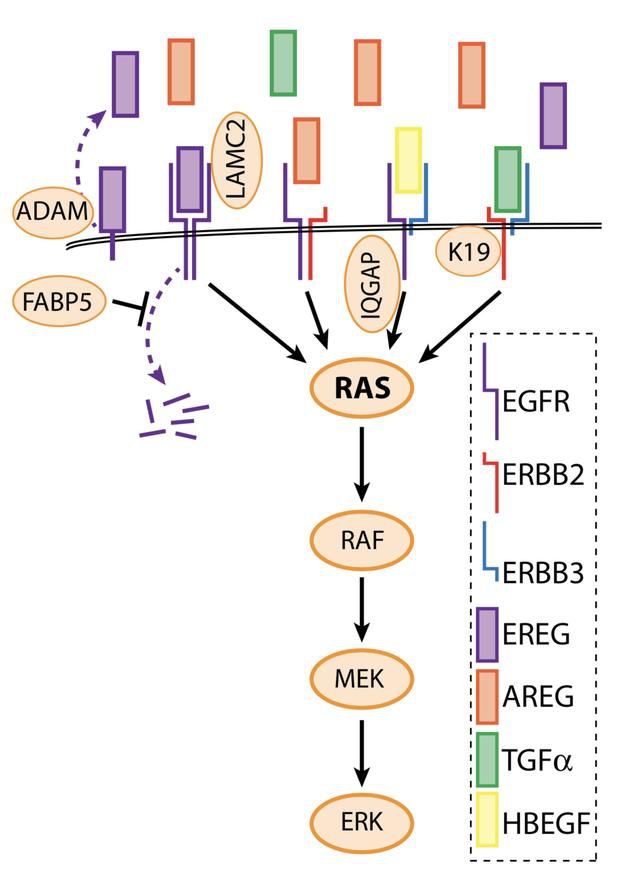
在人类癌症中,KRAS是癌症中最常见的致癌基因,正常的KRAS基因可抑制肿瘤细胞生长,而一旦发生突变,它就会在肿瘤细胞中编码关键的信号蛋白,促使细胞生长过程出现持续刺激,在打乱生长规律的同时,还有抑制细胞正常凋亡的作用,从而直接导致了肿瘤的发生。KRAS基因突变出现在接近九成的胰腺癌、三到四成的结肠癌和近五分之一的肺癌中(大多为非小细胞型肺癌)。其余会在胆管癌、宫颈癌、膀胱癌、肝癌和乳腺癌等实体癌中出现。KRAS基因就像体内一个“开关”,在肿瘤细胞生长以及血管生成等的信号传导通路里起着重要调控作用,但值得注意的是,该基因位点突变厚会形成一个具有特征性的半胱氨酸残基KRAS(G12C)。以此为基础,围绕该残基设计多种蛋白结合位点进行靶向治疗的研发思路,在目前的研究中均被报以良好的预期,如共价抑制剂等,但长期以来并没有可用于前期临床试验的产品问世。
另外文章中指出,在临床数据方面,接受AGM510治疗的四名肺癌患者中,六周后有两名患者的癌肿出现萎缩,一个减少了34%,另一个减少了67%。另两名患者癌肿大小的未见有明显改变。
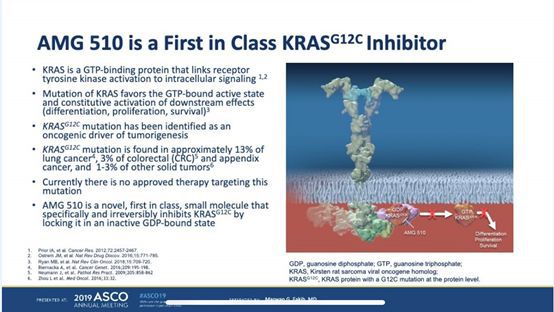
实际上关于AGM510作为KRAS(G12C)抑制剂首例药物对于癌症突出的治疗效果,早在今年6月初的美国临床肿瘤学会(ASCO)上,安进公司就已经公布了该药的Ⅰ期临床结果,Ⅰ期临床研究(NCT03600883),29例KRAS(G12C)突变实体瘤可供评估,其中10例为非小细胞型肺癌,19例肠癌等实体瘤。10例非小细胞型肺癌中有5例癌肿缩小,4例无明显进展,仅有1例患者出现癌肿持续恶化。癌肿缩小的患者至学会发言时止仍在继续服药中(7.3-27.4周)。在其余实体瘤中反应一般,所有患者未表现有癌肿减小,仅有74%的患者表现为未进一步恶化。
另一方面AMG 510耐受性表现较好,主要不良反应为食欲下降、腹泻、乏力、头痛、咳嗽、潮热和恶心,没有发现剂量限制毒性和与药物有关的4级以上不良反应。(转化医学网360zhyx.com)
参考文献:
Jude Canon. et al. The clinical KRAS(G12C) inhibitor AMG 510 drives anti-tumour immunity, Nature (2019).
DOI: 10.1038/s41586-019- 1694-1
推荐阅读:
-
日程更新:108位重量级嘉宾等你来!第三届现代临床分子诊断论坛&第四届精准医学高峰论坛
-
强强联手!新组合用药有望“创造”靶点,实现对癌症“围追堵截”
-
这些被忽视的免疫细胞,竟是乳腺癌细胞治疗的“潜力股”!
-
Science子刊:深挖“双面蛋白”沦为肿瘤免疫逃逸帮凶的真相
-
Cancer Cell:基于多蛋白复合物的癌症精准治疗范式,有望攻克一半以上的肿瘤
 腾讯登录
腾讯登录









还没有人评论,赶快抢个沙发