结构生物学+Octet®=高分文章
| 导读 | 直播预告|跟清华学姐学习高分论文发表秘决 |

结构生物学研究是通过解析蛋白质的精细结构,深入理解蛋白质如何在生命活动中进行工作,进而为探寻疾病根源、设计新药提供新路径,迄今为止,已有十余个诺贝尔奖颁给了结构生物学领域的相关科学家。
科研界流传了一句话,“想发高分文章,结构少不了”。生命科学领域中结构学相关的分子水平研究已成为一种趋势,这其中需要对蛋白进行结构解析,还需要对蛋白的功能进行验证。今天我们就来分享几个结构生物学与分子互作的经典案例!
1 西湖大学陶亮团队解密超毒力艰难梭菌毒素受体
超毒力艰难梭菌感染会导致腹泻、结肠炎和脓毒症等严重的症状,是最常见的病原菌感染之一。TcdB是艰难梭菌的主要毒力因子,在先前的研究中,陶亮及其研究团队表明FZD蛋白是TcdB1/3/5的致病受体[1]。今年3月,陶亮团队进一步揭示了TFPI是超毒力艰难梭菌特异性表达的两种TcdB亚型(TcdB2和TcdB4)的病例相关受体[2],文章中使用大量的BLI结合动力学分析数据进行验证分析。
TFPI在哺乳动物中存在α和β两种主要的同源异构体,都可以作为TcdB4的受体(图1)。为了进一步在分子水平鉴定TcdB的特异性结合区域,作者使用Octet®测试TFPIK1+K2-Fc与TcdB4的结合动力学,结果显示Kd为13 nM。为了进一步阐明K1和K2与TcdB4的作用关系,作者将TFPIK1和TFPIK2分别固定在Octet® AHC传感器上检测其与TcdB4的结合状况,结果显示,TcdB4与TFPIK2-FC的结合亲和力为6 nM,而未与TFPIK1-FC结合(图2),说明TcdB4特异性结合TFPI K2结构域。
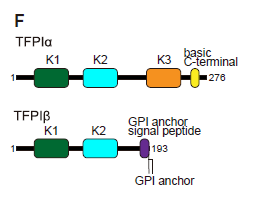
图1. TFP1α和TFP1β结构示意图。两者在蛋白N端共有两个被称为Kunitz的保守结构域K1和K2。
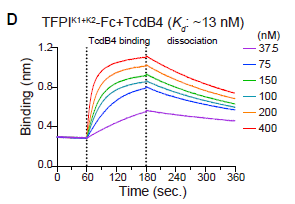

图2. Octet® Red 96分别检测TcdB4与TFPIK1+K2-FC,TFPIK1-FC和TFPIK2-FC的结合亲和力。
之后作者通过冷冻电镜,确定了TFPI-TcdB4复合物的三维结构。TFPIK2可通过与胰蛋白酶类底物(如FXa)相同的环路和TcdB4相互作用。为了比对FXa和TcdB4与TFPIK2的结合,作者将TFPIK2固定在AHC传感器上,首先将其暴露在300 nM的TcdB41285-1834或对照缓冲液中,随后再浸入100 nM FXa中进行检测。结果显示,预先结合TcdB的TFP1阻碍了FXa的后续结合。反之亦然(图4)。进一步确认了TcdB4的特异性结合域为TFPIK2。
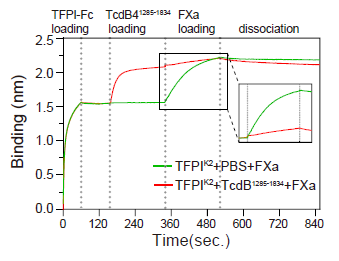
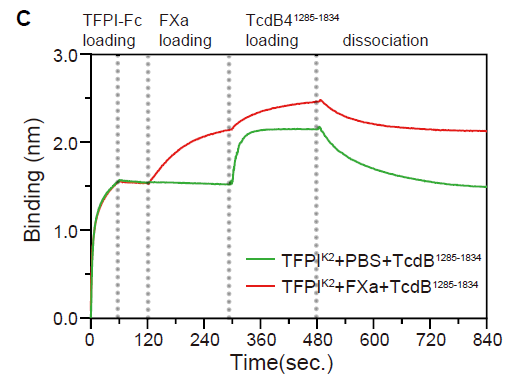
图4. FXa和TcdB4与TFPIK2的结合对比。
作者同样使用Octet®测定TcdB2与人TFPIK2的结合亲和力为0.4 μM。同时阻断TcdB2/4与TFPI以及CSPG4(TcdB2的结合受体)的结合,能够有效中和其毒性并阻止其对结肠上皮的损伤。这些发现确定了TFPI是超毒力艰难梭菌毒素TcdB2/4的结肠隐窝受体,为利用TFPI衍生物作为中和蛋白预防和治疗超毒力艰难梭菌感染提供基础。
2 最早的SARS-CoV-2 S蛋白结构解析
最先发表新冠S蛋白结构解析文章的是华盛顿大学的Veesler团队[3]和美国国立卫生研究院的McLellan团队[4]。两者都用到了Octet®检测S蛋白和ACE2的亲和力。Veesler团队首先对SARS-CoV-2 和SARS-CoV分离株的S蛋白的结构域B与人ACE2结合的亲和力进行了比较,SARS-CoV-2 SB与ACE2具有较高的结合亲和力(KD:1.2 nM vs 5 nM),并且解离速度稍慢一些(koff:1.6 x 10-4/s vs 7.1x 104/s)。一定程度上解释了SARS-CoV-2比SARS-CoV具有更强的感染和传播能力。

SARS-CoV-2 SB与hACE2

SARS-CoV SB与hACE2
用HIS1K传感器固化SARS-CoV-2 SB /SARS-CoV SB结合ACE2(Octet RED96)
3 核酸-蛋白结构生物学大牛施一公组的剪切体结构解析[5]
施一公课题组表达了酿酒酵母中所有的七个Lsm蛋白,将这一Lsm1-7复合物进行了纯化,并对这种复合物结晶进行解析,获得了分辨率为3.0埃米的结构模型。结构分析发现Lsm1-7复合物具有同源七聚体Lsm2-8。
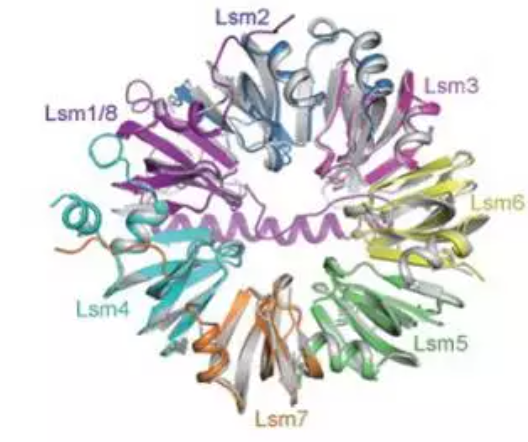

使用清华大学结构生物学高精尖创新中心蛋白平台的Octet® RED96,通过SA传感器固化biotin-RNA,直接检测蛋白,得到准确KD值
Lsm1-7与8A和8U的亲和力分别为6 μM和2 μM,没有明显差别。Lsm2-8与8U的结合比8A强100倍(20 nM与2 μM)。这就说明Lsm1-7对RNA末端8A的识别水平与Lsm2-8类似的,但是Lsm2-8对8U的结合识别能力更强。

将Lsm1-7当中的一些亚基的某些氨基酸位点进行了突变,然后再与8A和8U的RNA序列进行亲和力检测
Lsm2与Lsm3亚基上的Arg(精氨酸)位点突变之后,Lsm1-7与8U的结合变得更弱了,而Lsm1-7与8A的结合则没有明显变化。说明这些Arg是Lsm1-7与8U的结合的重要的氨基酸残基位点。
4 中国药科大学天然药物活性组分与药效国家重点实验室[6]
研究人员首先对Hsp90-Cdc37的复合物晶体结构进行分析,寻找二者的相互作用界面,确定关键的作用残基。随后对一个含有超过150万个分子的化合物库进行虚拟筛选,最终发现化合物11具有进行深入优化的潜力。对化合物11的结构进行构效关系研究后,研究人员得到了化合物DDO-5936。将这个化合物的一些潜在的参与HSP90结合的R46,E47,Q133等氨基酸位点突变后,用Octet®检测发现这些HSP90突变与这个小分子亲和力不同程度的下降,证明了结构解析的结果。

用SSA传感器固化HSP90与不同浓度的DDO-5936结合解离(Octet® RED96)
5 辉瑞基于三元复合物的结构解析设计PROTAC分子[7]
文章报道了一种独特的BTK降解器cIAP1三元复合物晶体结构,并利用相关构象解析数据设计了一种新的PROTAC分子,采用了更刚性的linker,改变了其与蛋白的结合动力学和降解能力,与计算模型和第二三元复杂晶体结构的预测一致。这些数据为E3连接酶的IAP家族靶向蛋白降解机制提供了新的见解。
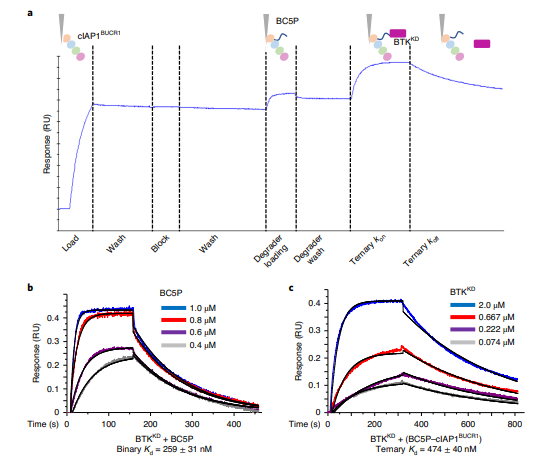
作者利用Octet®开发了一种三元复合物形成实验(下图 a)。将带有biotin-cIAP1偶联到SA传感器上,浸入含BC5P的溶液中。经过简短的清洗后,将二元络合物浸入含有对BTK激酶结构域的溶液中,分析其结合速率常数(kon)和解离速率常数(koff)。可以看到Binary Kd = 259 ± 31 nM < Ternary kd = 474 ± 40 nm,说明了三元复合物系统是非协同的(下图 b和c)。
11月3日(周四)下午14:00-15:30,赛多利斯联合清华大学医学院博士后/助理研究员马丙婷博士,聚焦结构生物学领域,共同解读结构解析与结合动力学赋能病毒研究经典案例,一键Get高分文章秘诀。
扫描二维码预约

会议日程

-参考文献-
[1] Tao, L. et al. Frizzled proteins are colonic epithelial receptors for C. difficile toxin B. Nature 538, 350-355, (2016).
[2] Luo et al., TFPI is a colonic crypt receptor for TcdB from hypervirulent clade 2 C. difficile. Cell 185, 980–994 March 17, 2022
[3] A. C. Walls, et al., Structure, function, and antigenicity of the SARS-CoV-2 spike glycoprotein. Cell , 2020, 181(2)..
[4] D. Wrapp, et al., Cryo-EM structure of the 2019-nCoV spike in the prefusion conformation. Science , 2020, 367, 1260-1263.
[5] Zhou, L., et al., Crystal structure and biochemical analysis of the heptameric Lsm1-7 complex. Cell research, 2014, 24(4):497-500.
[6] Small-molecule inhibitor targeting the Hsp90-Cdc37 protein-protein interaction in colorectal cancer. Sci. Adv. 2019, 5, eaax2277.
[7] J. Schiemer, et al., Snapshots and ensembles of BTK and cIAP1 protein degrader ternary complexes. Nature Chemical Biology. 2020.
 腾讯登录
腾讯登录






还没有人评论,赶快抢个沙发