癌症治疗的根源?加州大学最新研究确定了对抗癌症治疗耐药性的新方法
| 导读 | 阻断癌症基因组的不稳定性可以防止肿瘤的多样化并逃避治疗。 |
1月26日,加州大学洛杉矶分校琼森综合癌症中心(UCLA Jonsson Comprehensive Cancer Center)发表在《Cancer Discovery》上的一项研究“Blocking Genomic Instability Prevents Acquired Resistance to MAPK Inhibitor Therapy in Melanoma”,确定了靶向癌症治疗耐药性的DNA根源,为解决癌症治疗中的棘手问题提供了一种潜在策略。
https://doi.org/10.1158/2159-8290.CD-22-0787
研究背景
Roger Lo博士说:“我们正在采取一种新的方法来对抗‘获得性治疗耐药性’,即癌症通过分子进化逃避靶向治疗的能力。密集的研究主要集中在治疗复发的癌症上,试图在肿瘤细胞变得更加复杂和强大后进行干预。我们认为,预防,而不是在癌症变得更加具有侵略性后试图逆转耐药性,这可能会提高患者的生存几率。”
为了了解癌症基因组在靶向治疗开始后是如何立即发生变化的——可能产生能够逃避治疗的新遗传变异,研究人员专注于转移性皮肤黑色素瘤。这种侵袭性皮肤癌没有有效的治疗方法,直到最近开发出一种针对癌症携带BRAF基因突变的患者的靶向疗法,在大约一半的转移性黑色素瘤患者和许多其他类型的常见和高致命癌症患者中发现。研究人员希望通过阻断黑色素瘤产生遗传多样性的手段,可以提供防止癌症逃避靶向治疗的无数方式。
研究结果
研究表明,在患者和患者来源的异种移植物(PDX)中进行MAPK抑制剂(MAPKi)治疗后,转移性皮肤黑色素瘤的获得性耐药基因组通过复杂的基因组重排(CGRs)和染色体外DNA(ecDNA)特异性地扩增耐药驱动因子,非同源末端连接(NHEJ)和同源重组修复(HRR)基因。几乎所有敏感和获得性耐药基因组都拥有普遍的染色体藓门区域,具有不成比例的高突变负荷,并且与ecDNA和CGRs跨度显著重叠。
目前,ecDNA和CGRs扩增子内的体细胞突变丰富了HRR信号,特别是在获得性耐药肿瘤中。无论灵敏度或耐药性如何,断点序列分析表明NHEJ对于CGR和ecDNA形成的双链DNA断裂修复至关重要。在人类黑色素瘤细胞系和PDXs中,通过DNA-PKCS抑制剂靶向NHEJ,通过在联合治疗早期减少ecDNA和CGRs的大小来预防/延迟获得的MAPKi耐药性。因此,针对基因组不稳定的原因可以防止获得性耐药性。
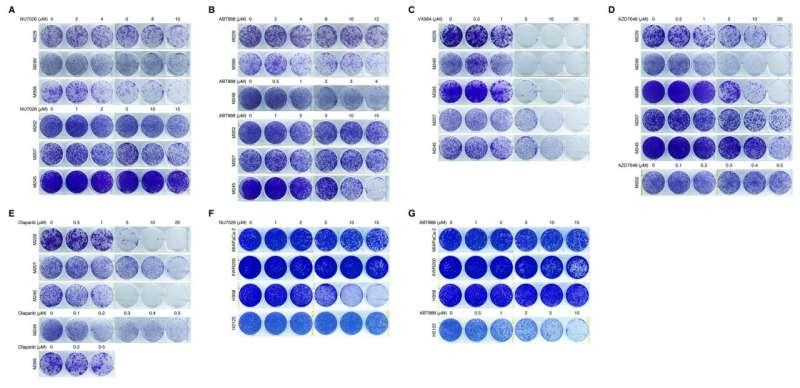
人体黑色素瘤、PDAC 和 NSCLC 克隆生成生长测定中的单药抑制效力。
研究意义
总而言之,研究分析了破碎基因组DNA的重新缝合是如何在耐药性黑色素瘤中发生的,并发现了一种可能特别重要的称为DNA-PK的蛋白质。Gatien Moriceau说:“我们测试了一种新的组合方法来阻止基因组不稳定性并防止模型细胞系和植入小鼠的患者肿瘤细胞的获得性耐药性,并且相信这种方法有可能将应用于多种黑色素瘤亚型和几种其他类型的侵袭性癌症,如胰腺癌和肺癌。”(转化医学网360zhyx.com)
参考资料:
https://medicalxpress.com/news/2023-01-approach-cancer-evolving-resist-treatment.html
https://doi.org/10.1158/2159-8290.CD-22-0787
注:本文旨在介绍医学研究进展,不能作为治疗方案参考。如需获得健康指导,请至正规医院就诊。
 腾讯登录
腾讯登录






还没有人评论,赶快抢个沙发