【Nature】 重磅!颠覆性蛋白设计技术助力靶向不可成药靶点
| 导读 | 导读:近年来,人工智能(AI)技术飞速发展。借助人工智能,医务人员不但可以为患者提供咨询服务,而且还可以设计全新蛋白分子。已有多篇论文揭示了利用机器学习,更精准、更快速地按需设计蛋白质分子的能力。 |
近日,华盛顿大学David Baker教授带领的团队在顶级学术期刊《Nature》上发表了一篇题为De novo design of modular peptide-binding proteins by superhelical matching的研究论文。
该研究描述了一种设计蛋白的颠覆性技术,通过借鉴大自然中天然重复蛋白与包含重复多肽序列的蛋白相结合的机制,他们研发了一种针对重复多肽序列,设计全新结合蛋白的通用策略。通过这一策略,可以生成高度稳定,具有高度特异性和亲和力的结合蛋白。这一策略不但可以用于靶向包含重复多肽序列的蛋白靶点,还可以扩展到靶向包含无序结构的不可成药靶点。

https://www.nature.com/articles/s41586-023-05909-9
设计背景
01
无论对于基础科学研究还是新药开发,能够生成与靶点蛋白或者多肽结合的蛋白质非常关键。由于在大自然中,很多蛋白或者多肽在游离状态下并没有确定的三维结构,这给设计与它们结合的蛋白带来很大挑战。在本研究中,Baker教授领衔的团队借鉴了自然界中重复蛋白的作用机制。比如犰狳重复蛋白(armadillo-repeat proteins)包含着重复出现的结合模块,每个模块可以与特定的重复多肽序列结合,多个模块组合在一起,可以与包含多个重复多肽序列的蛋白产生高亲和力、高特异性的相互作用。
设计方法
02
设计人员通过模块化重复蛋白支架将肽识别推广到任意重复肽骨架几何结构。这需要解决两大挑战:首先,构建重复间隔和方向与目标肽构象相匹配的蛋白质结构。其次,确保将未结合状态的肽-水氢键替换为结合状态的肽-蛋白质氢键。
为了解决第一个挑战,他们推断设计蛋白质上的重复单元与肽上的重复单元之间的同相几何匹配的必要(但不充分)标准是两者追踪出的超螺旋之间的对应关系。生成了大量的重复蛋白主链,这些主链对范围广泛的超螺旋几何结构进行了采样。然后,通过随机采样二肽和三肽构象(避免肽内空间冲突)生成相应的重复肽主链集,再重复这些 4-6 次以生成 8-18 残基肽。最后,在搜索匹配的重复蛋白质和重复肽骨架对,要求上升在 0.2 Å 以内,扭曲在 5° 以内,半径相差至少 4 Å。
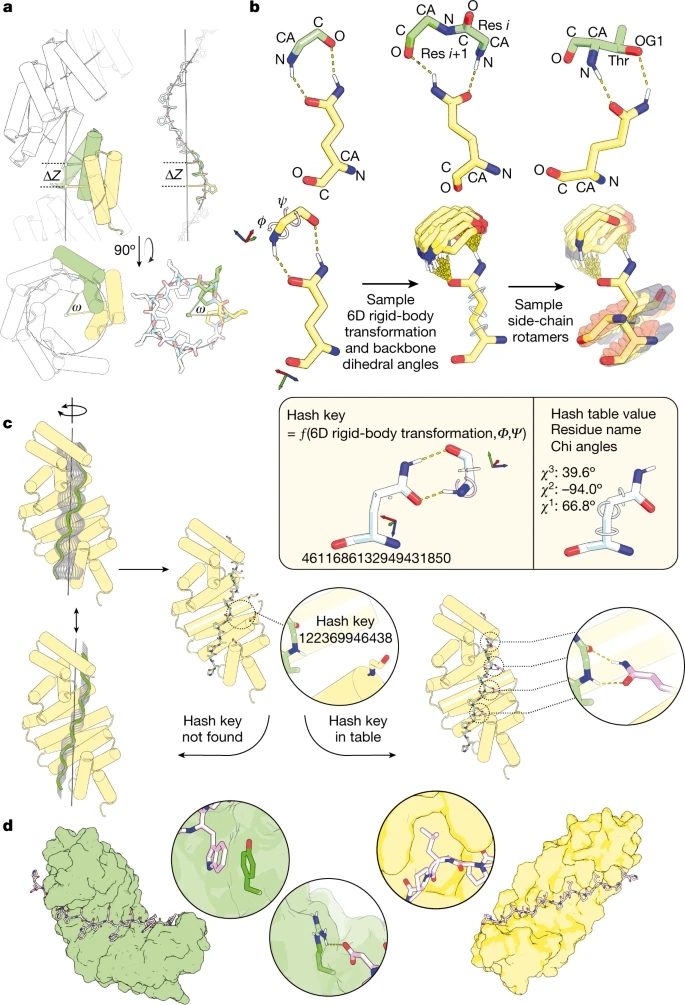
模块化肽结合物设计流程概述
为解决第二个挑战,他们推断蛋白质上的侧链和肽上的成对主链基团或主链和侧链基团之间的双齿氢键可以允许在蛋白质上掩埋足够的肽表面积,以实现高亲和力结合而不会导致大量去溶剂化。他们开发了一种几何哈希方法,能够快速识别蛋白质上肽的刚体对接,这些对接与双齿相互作用的阶梯相容。
设计意义
03
综上,该设计揭示了计算蛋白质设计的能力,可以靶向肽和不具有刚性三维结构的本质上无序的区域。由于设计的蛋白质以相当高的水平表达并且非常稳定,这些设计和针对更广泛目标的进一步设计将在蛋白质组学和其它需要特定肽识别的应用中有许多用途。本论文进一步扩展了人工智能设计蛋白质的策略,让靶向更多不可成药靶点即将成为现实。(转化医学网360zhyx.com)
参考资料:
https://www.nature.com/articles/s41586-023-05909-9
注:本文旨在介绍医学研究进展,不能作为治疗方案参考。如需获得健康指导,请至正规医院就诊。
 腾讯登录
腾讯登录









还没有人评论,赶快抢个沙发