【Nature子刊】最新!斯坦福大学研究人员在肿瘤联合治疗方面取得突破!
| 导读 | 癌症免疫疗法已经彻底改变了治疗方法,但作为单药疗法,其成功程度有限。研究人员使用单细胞和基于成像的空间分析来阐明异质性基底细胞癌肿瘤上皮周围的三个微环境邻域。 |
5月10日,斯坦福大学研究人员联合发文,在《Nature:Communications》上发表了“Skin basal cell carcinomas assemble a pro-tumorigenic spatially organized and self-propagating Trem2+ myeloid niche”的文章,研究人员称这项工作为独立于免疫抑制的直接肿瘤免疫生态位动力学提供了机制见解,也为潜在的肿瘤联合治疗方法提供了基础。

https://www.nature.com/articles/s41467-023-37993-w
研究背景
01
虽然免疫检查点阻断(ICB)疗法的出现已经彻底改变了癌症治疗的方法,但这些治疗的疗效仍各不相同。此外,单细胞基因组技术已经揭示了对ICB的耐药性。皮肤基底细胞癌(bcc)是研究靶向治疗与上皮异质性和可塑性之间相互作用的理想选择,因为它的发病率高,并且能够在治疗过程中从确切位置连续活检。研究人员做了大量的工作集中在肿瘤上皮中心对靶向Hedgehog (HH)治疗的耐药机制上,包括诱导和选择介导复发的离散肿瘤上皮群体。
研究方法
02
最近研究人员发现了由表面标记物LY6D标记的持久性BCC群体,具有BCC和鳞状细胞癌样特征。虽然BCC上皮状态已被确定,但驱动和稳定每种肿瘤状态的TME仍缺乏具体特征。与其他上皮肿瘤一样,通过aPD1和 aPDL抗体进行的免疫检查点阻断疗法已被批准作为靶向治疗失败的BCC患者的二线治疗。aPD1治疗的有效率约为30%,这表明需要进一步了解耐药机制。异质性和动态免疫抑制TME成分的反卷积表明,骨髓细胞和癌症相关成纤维细胞等基质群体是免疫抑制和ICB失败的驱动因素。
肿瘤相关巨噬细胞(tam)在ICB中有重大意义,因为它们能够通过抑制肿瘤浸润淋巴细胞(TILs)来增强免疫抑制,例如通过PDL1的上调与PD1直接相互作用,或分泌免疫抑制代谢物或配体促进T调节性细胞(Tregs)的募集。TAMs的亚群最近被认为与促进免疫抑制性TME有关,同时靶向这些细胞与aPD1 ICB结合可增强肿瘤清除。此外,在aPD1治疗失败的患者中发现TREM2+ tam增加。除了确定tam的特定靶标亚群之外,最近的研究还关注tam的起源和维持,因为去除tam将消除一个重要的肿瘤刺激,并且仍然是治疗障碍。大多数TAM维持模型依赖于持续的TAM前体招募和随后的分化作为主要来源。然而,阻断迁移信号(如CCL2/CCR2)的抗趋化因子临床试验进展不理想,这表明多个冗余信号可能参与了肿瘤的募集,或者随着肿瘤的生长,还有其他机制促进TAM群体的扩张。
研究人员使用单细胞和空间表达方法鉴定了一个独特的TREM2+ VCAM1+巨噬细胞群体,我们称之为皮肤癌相关巨噬细胞(SCAMs)。SCAMs通过分泌配体OSM促进LY6D-肿瘤上皮细胞增殖,这一作用独立于免疫抑制。研究人员还发现SCAMs在TME内增殖,并能在连续传代的肿瘤中保持。肿瘤在几天内从骨髓来源的单核细胞(bmdm)中招募和极化SCAMs,为肿瘤免疫生态位的组装动力学提供了深入见解,这将有助于合理的靶向联合治疗。
https://www.nature.com/articles/s41467-023-37993-w
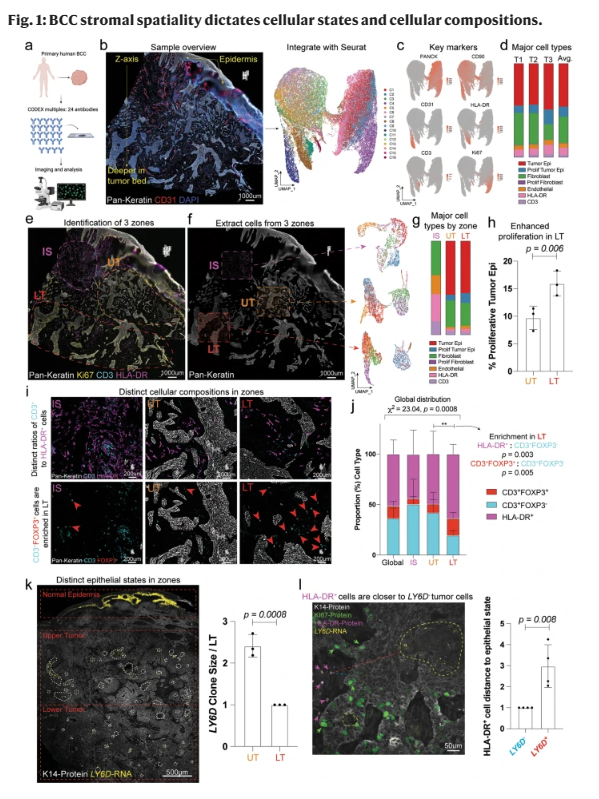
为了解肿瘤上皮和间质之间的空间和调控关系,研究人员使用了CODEX多重系统对24种抗体进行染色,以询问肿瘤细胞组成并定义全局邻域(图1a)。与其他上皮性肿瘤不同,这些BCC肿瘤包含患者的正常表皮,这是研究的关键里程碑(图1b)。对肿瘤相关区域的单个细胞进行分割,不包括正常表皮,提取荧光强度,然后与Seurat的scRNA-Seq分析工具整合(图1b)。在一个有代表性的样本中,研究人员根据24种抗体不同的荧光强度发现了16个不同的簇(图1b),确定了关键的细胞类型,包括肿瘤上皮细胞(PANCK+)、成纤维细胞(CD90+)、内皮细胞(CD31+)、免疫细胞亚群(HLA-DR+抗原呈递细胞或CD3+ T细胞),以及它们的增殖指数(KI67+),在三个患者肿瘤中,原代细胞类型的比例相似(图1c, d)。
沿着z轴,研究人员注意到KI67标记的下肿瘤(LT)区域增殖增强(图1e)。相反,与靠近患者表皮界面的LT相比,肿瘤上皮增殖减少,研究人员称之为上肿瘤(UT)(图1e)。对肿瘤含上皮腔室的定量分析证实了视觉观察,即LT具有更高比例的增殖肿瘤细胞(图1)。最后,与肿瘤含上皮区相反,散布着大量缺乏肿瘤上皮的区域由大量CD3+和HLA-DR+细胞主导,称之为免疫群(IS)(图1b、e)。
研究意义
03
虽然ICB疗法已经彻底改变了癌症治疗,但在确定防止肿瘤生长的额外免疫靶点,但是仍然存在概念上的障碍。利用多路成像工具和单细胞多组学技术,研究人员在bcc高增殖的LT区域内描述了空间组织的免疫景观,定义了增殖性肿瘤免疫生态位,也为潜在的肿瘤联合治疗方法提供了基础。(转化医学网360zhyx.com)
参考资料:
https://www.nature.com/articles/s41467-023-37993-w
注:本文旨在介绍医学研究进展,不能作为治疗方案参考。如需获得健康指导,请至正规医院就诊。
 腾讯登录
腾讯登录









还没有人评论,赶快抢个沙发