【Adv. Sci.】同济大学首次确认食管鳞癌进展和耐药性的新机制并揭示新的治疗策略
| 导读 | 导读:食管鳞状细胞癌(ESCC)因强大的侵袭性表型和化疗耐药,是最致命的癌症之一。TAO激酶属于丝裂原活化蛋白激酶,介导多种癌症的耐药性。然而,TAO激酶在ESCC进展和化疗耐药中的作用尚未被探讨。 |
9月13日,同济大学研究人员在学术期刊《Science Advance》上发表了题为“TAOK3 Facilitates Esophageal Squamous Cell Carcinoma Progression and Cisplatin Resistance Through Augmenting Autophagy Mediated by IRGM”的研究论文。本研究报道了TAOK3通过增强细胞自噬进而促进食管鳞癌的进展和化疗耐药。机制上,TAOK3磷酸化KMT2C在S4588并加强KMT2C和ETV5之间的相互作用。因此,KMT2C核易位增加,自噬相关基因IRGM的转录进一步上调。此外,抑制剂SBI-581在体外和体内均能显著抑制TAOK3介导的细胞自噬,并与顺铂协同治疗ESCC。

https://onlinelibrary.wiley.com/doi/full/10.1002/advs.202300864
研究背景
01
食管癌在人类癌症死亡率中排名第六,其中(ESCC)约占90%。ESCC与广泛的淋巴扩散有关,通常在晚期诊断出来。化疗对ESCC患者至关重要,在术后辅助治疗和一线治疗中发挥着不可替代的作用。顺铂仍是治疗ESCC的首选药物,但耐药限制了其实际疗效,恶化了ESCC患者的预后。因此,研究ESCC的发生机制及顺铂耐药机制,发现ESCC新的治疗靶点及预后指标具有重要意义。
1001 (TAOK)激酶是丝氨酸/苏氨酸激酶,属于SET20激酶家族。作为MAP3K的一种,TAO激酶对刺激有反应,如紫外线照射、细胞因子、热、营养缺乏和渗透性休克。据报道,在电离和紫外线辐射模拟下,TAO激酶被ATM(共济失调毛细血管扩张突变)磷酸化和激活,并进一步调节p38介导的DNA损伤反应。此外,除了p38 MAPK级联中的MKK3/6外,TAO激酶被发现可磷酸化MKK4/7并激活JNK信号级联。Hippo信号通路,也称为SWH通路,调节细胞增殖和凋亡。除了参与MAPK级联反应外,TAO激酶也被发现调节Hippo信号通路。除了调节各种信号通路,TAO激酶被证实与其他细胞蛋白相互作用,既有依赖的,也有不依赖的。TAO激酶通过与一些靶蛋白相互作用,调节DNA损伤应答、细胞骨架稳定性、凋亡等生理和病理生理应答。值得注意的是,据报道TAO激酶可介导多种癌症的化疗耐药。然而,TAO激酶在ESCC中的作用尚未被探讨。
研究过程及发现
02
ESCC患者预后较差,主要是症状不明显,早期易发生转移。迄今为止,顺铂是治疗ESCC的首选药物,但耐药仍然是一个巨大的问题。因此,弄清ESCC进展和顺铂耐药背后的生物学过程,寻找新的治疗靶点势在必行。自噬是一种重要的稳态细胞循环机制,在耐药性中起着至关重要的作用。
本研究中,研究人员首次发现在ESCC细胞系和组织中,TAOK3而不是TAOK1和TAOK2显著过表达。此外,只有TAOK3能够增强ESCC的自噬。在功能上,TAOK3可以促进ESCC细胞的增殖、迁移、侵袭和顺铂耐药,但抑制细胞凋亡。这些结果表明,TAOK3通过诱导自噬促进ESCC的进展和顺铂耐药。从机制上讲,TAOK3可以使组蛋白甲基转移酶KMT2C在S4588位点磷酸化,并加强KMT2C与转录因子ETV5之间的相互作用。研究结果表明,TAOK3可以被视为ESCC的癌基因和预后生物标志物,类似于其他癌症。相关分析显示IRGM蛋白表达水平与TAOK3蛋白表达水平呈正相关,表明IRGM蛋白表达在ESCC组织中受TAOK3调控。
鉴于本研究中TAOK3依赖于其激酶活性促进ESCC的进展,研究人员期待寻找特异性的TAOK3抑制剂,以改善其对肿瘤进展的影响。最近,研究人员对5600种化合物进行扫描后,发现了一种针对TAOK3的特异性抑制剂SBI-581 (IC50 = 42nm)[28]。然而,其肿瘤抑制作用,特别是与化疗的协同作用尚未被研究。研究还发现,SBI-581可以将TAOK3的磷酸化明显迁移到KMT2C,并且KMT2C与ETV5的结合被稳健释放。使用SBI-581后,ESCC细胞的自噬水平降低,IRGM过表达可有效恢复这种作用。体外和体内实验证实了SBI-581与顺铂的协同作用。这些结果表明,SBI-581能够显著抑制TAOK3对ESCC的作用,并与顺铂在ESCC治疗方面具有良好的协同作用。因此,SBI-581在未来临床应用于ESCC治疗的可能性很大。
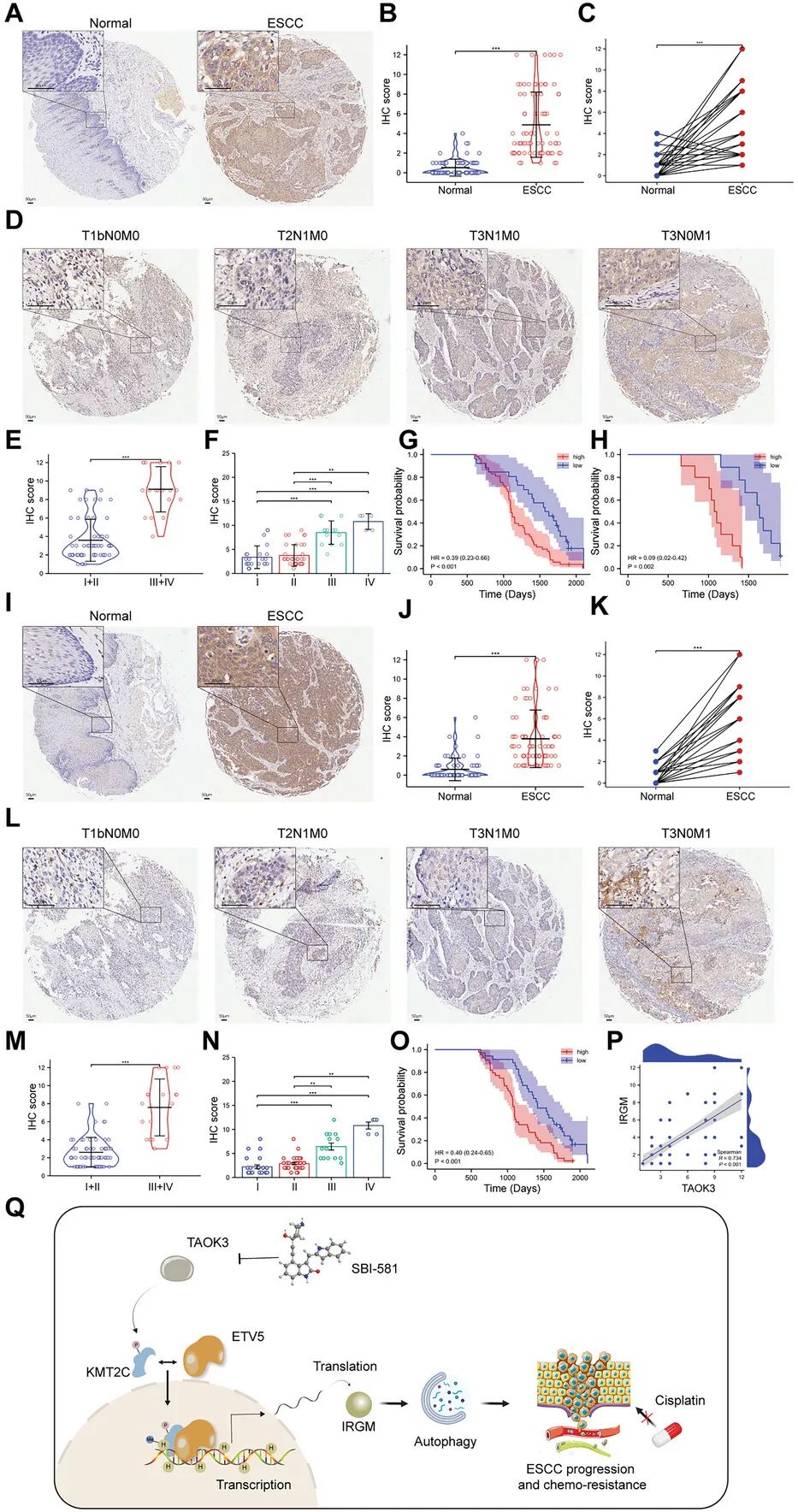
TAOK3和IRGM在ESCC组织中过表达,在临床上与肿瘤分期和不良预后相关
研究结论
03
综上,研究人员首次确定了TAOK3在ESCC的进展和化疗耐药中的潜在作用。TAOK3在ESCC中的过表达可上调自噬相关蛋白IRGM的表达,进一步增强ESCC的自噬。从机制上讲,TAOK3磷酸化KMT2C的S4588位点,并促进KMT2C和ETV5之间的相互作用。在KMT2C和ETV5的帮助下,KMT2C的核易位增加,IRGM的转录上调。TAOK3可以作为ESCC的癌基因和重要的预后生物标志物。抑制剂SBI-581可与顺铂联合作为一种新的治疗策略。(转化医学网360zhyx.com)
参考资料:
https://onlinelibrary.wiley.com/doi/full/10.1002/advs.202300864
注:本文旨在介绍医学研究进展,不能作为治疗方案参考。如需获得健康指导,请至正规医院就诊。
 腾讯登录
腾讯登录









还没有人评论,赶快抢个沙发