新治疗选择!哈尔滨医科大学乔国芬团队发现“癌中之王”胰腺癌最新生物标志物
| 导读 | 现有研究表明,不同表达的circRNA(DECs)可以作为癌基因或抑癌基因,调控胰腺癌细胞的增殖、迁移、侵袭、转移、凋亡和细胞周期等。 |
12月11日,哈尔滨医科大学乔国芬团队在期刊《Cell Death Discovery》上在线发表题为“Circular RNA hsa_circ_0001846 facilitates the malignant behaviors of pancreatic cancer by sponging miR-204-3p and upregulating KRAS expression”的研究论文,研究证实了hsa_circ_0001846作为胰腺癌特异性临床生物标志物的潜力,为探索胰腺癌的诊断和治疗靶点提供了更多选择和理论基础。

https://www.nature.com/articles/s41420-023-01733-2
研究背景
01
胰腺癌可能由内分泌或外分泌细胞引起,是迄今为止最致命的胰腺疾病,其病因通常与其他胰腺疾病相关。尽管近年来其5年生存率已增加到10%,但胰腺癌仍然是最致命的人类癌症之一。
环状RNA(CircRNA)是一类具有封闭环结构的非编码RNA,在研究过程中,研究人员发现与线性RNA相比,虽然circRNA的表达水平较低,但它们仍具有更高的丰度、多样性和特异性,一些circRNA甚至在同一组织或细胞中与它们同源的线性RNA表达水平相反。这表明circRNA可能具有自己的功能。
环状RNA(circRNA)主要在细胞中作为调控分子发挥作用。现有研究表明,不同表达的circRNA(DECs)可以作为癌基因或抑癌基因,调控胰腺癌细胞的增殖、迁移、侵袭、转移、凋亡和细胞周期等。这些功能涉及多种机制,包括miRNA的海绵活性、癌相关信号通路的调节以及蛋白质相互作用。
hsa_circ_0001846通过miR-204-3p
间接调节KRAS表达水平发挥其致癌效应
02

研究人员使用miRDB、miRDIP、miRWALK和TargetScan等生物信息学网站分析了miR-204-3p和KRAS的序列,并发现它们之间存在结合关系。研究人员突变了miR-204-3p和KRAS的结合位点,构建了Mut-KRAS/WT-KRAS质粒,并进行了双荧光素酶实验。结果显示,共转染WT-KRAS和miR-204-3p模拟物的HEK293T细胞明显降低了荧光素酶活性,而Mut-KRAS和miR-204-3p模拟物在细胞中未显著改变荧光素酶活性。虽然发现miR-204-3p抑制剂并没有显著增加KRAS的mRNA水平,但Western blot结果显示它能够增加KRAS的蛋白表达水平,表明miR-204-3p可能主要影响KRAS的转录后水平。沉默hsa_circ_0001846可以抑制KRAS的表达,而miR-204-3p抑制剂则对抗了这种效应。
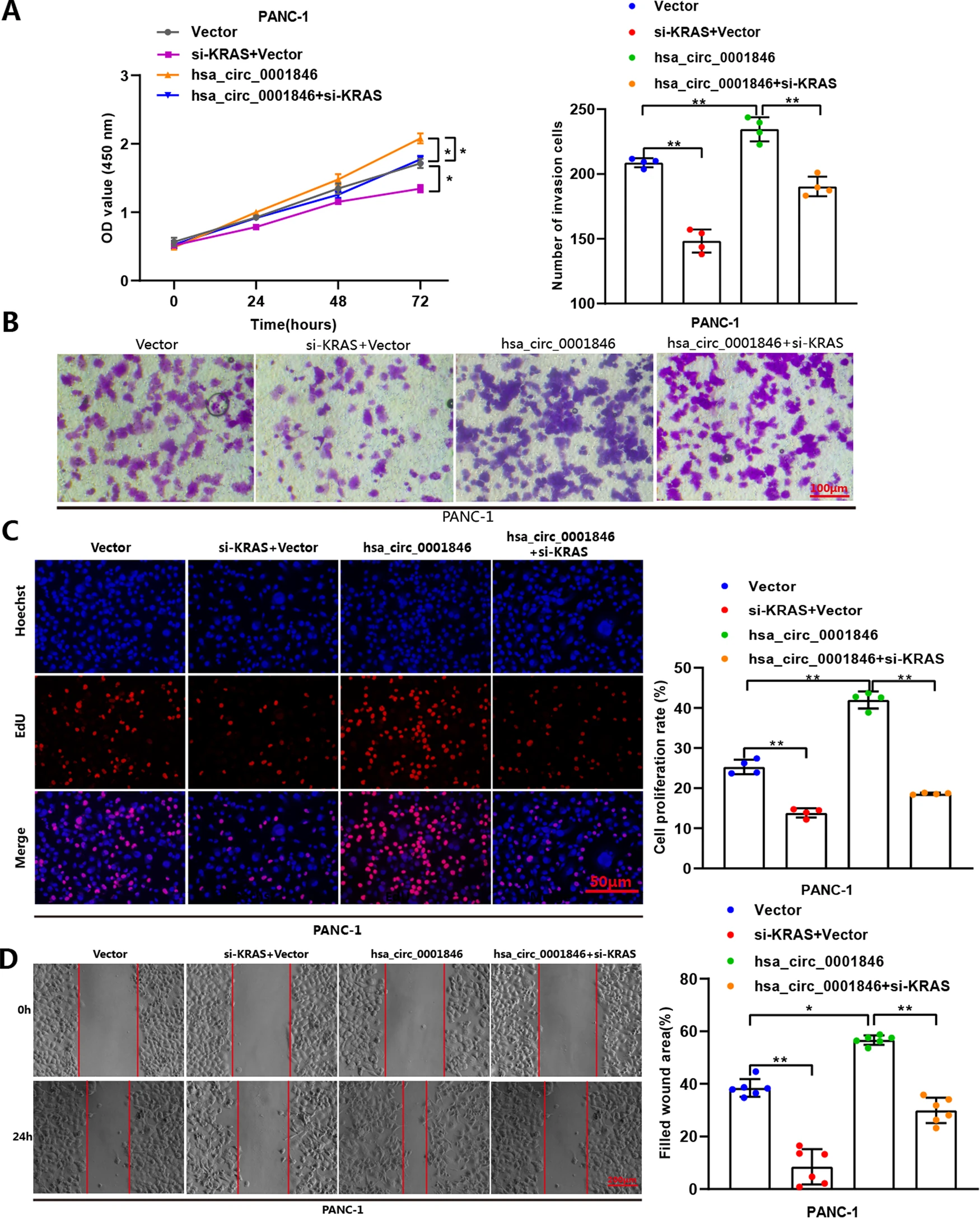
功能性实验还显示,沉默KRAS可以逆转hsa_circ_0001846过表达引起的致癌效应。 上述结果表明,KRAS是miR-204-3p的下游靶标,而hsa_circ_0001846通过吸附miR-204-3p间接调节KRAS的表达,从而发挥其致癌作用。
研究结果
03
综上所述,研究证实了hsa_circ_0001846作为胰腺癌特异性临床生物标志物的潜力,为探索胰腺癌的诊断和治疗靶点提供了更多选择和理论基础。(转化医学网360zhyx.com)
参考资料:
https://www.nature.com/articles/s41420-023-01733-2
注:本文旨在介绍医学研究进展,不能作为治疗方案参考。如需获得健康指导,请至正规医院就诊。
 腾讯登录
腾讯登录








还没有人评论,赶快抢个沙发