新进展!复旦大学发文:揭示胰腺癌联合免疫治疗新思路
| 导读 | 多种内源性和外源性机制导致的免疫抑制微环境给胰腺癌的免疫治疗带来了巨大挑战。 |
近日,复旦大学研究团队在期刊《Cell Death&Disease》上发表了题为“The GFPT2-O-GlcNAcylation-YBX1 axis promotes IL-18 secretion to regulate the tumor immune microenvironment in pancreatic cancer”的研究论文,本研究中,研究人员阐明了胰腺癌细胞中己糖胺生物合成途径(HBP)的代谢途径与免疫微环境的关系,为HBP易感性与胰腺癌免疫治疗的联合治疗提供了新的思路。
https://www.nature.com/articles/s41419-024-06589-7
研究背景
01
到2040年,胰腺导管腺癌(PDAC)将成为癌症相关死亡的第二大原因。大约15-20%的患者在诊断时有切除的机会,但这些患者中只有大约20%存活到5年。对于局部晚期,不可切除和转移性疾病,治疗是姑息性的。目前晚期PDAC患者的标准治疗是基于吉西他滨的化疗方案。然而,这种治疗方案只带来了适度的益处:仅增加了5周的生存期。迫切需要找到更有效的治疗方案。
免疫治疗在实体器官肿瘤中显示出显著的益处,免疫检查点阻断改善了各种癌症的治疗选择,如转移性黑色素瘤、肾细胞癌、微卫星不稳定性结直肠癌、非小细胞肺癌和霍奇金淋巴瘤。然而,免疫疗法治疗PDAC的疗效令人失望。幸运的是,针对PDAC中多种内源性和外源性机制形成的免疫抑制肿瘤微环境的联合免疫治疗策略已经成为一种有价值的治疗选择。
研究发现
02
为了鉴定PDAC中与免疫相关的预后基因,研究人员对22例来自FUSCC诊断为PDAC的患者的肿瘤样本进行了转录组测序。通过比较两组患者的转录组测序,研究人员鉴定出1491个差异表达基因。研究人员进一步对来自癌症基因体图谱 (TCGA)的177个PDAC转录组数据集进行单样本基因集富集分析,并将患者分为免疫细胞浸润高水平和低水平两组。为了进一步验证这些与免疫相关的预后基因,研究人员对TCGA和国际癌症基因组联盟(ICGC)数据中的327个基因进行了单变量Cox风险分析,并使用森林图显示这些基因的P值< 0.05。研究人员发现GFPT2在肿瘤组织中普遍较高表达,且GFPT2高表达与较差的预后相关。此外,研究人员分析了GFPT2的表达与免疫细胞(B细胞、CD4 + T细胞、CD8 + T细胞、中性粒细胞、巨噬细胞和树突状细胞)浸润的相关性,发现巨噬细胞与GFPT2的相关性最好。因此,研究人员确定GFPT2是免疫相关的预后基因,并进一步探讨了GFPT2对巨噬细胞的影响。
为了进一步探讨GFPT2对巨噬细胞极化的影响,研究人员构建了与巨噬细胞共培养的GFPT2稳定敲低或过表达的胰腺癌细胞体外模型。研究结果表明胰腺癌细胞中GFPT2过度表达促进巨噬细胞M2极化。研究结果还表明GFPT2作为癌基因发挥作用,促进胰腺癌细胞的增殖和迁移。胰腺癌细胞中GFPT2过表达通过促进O-GlcNAc糖基化促进巨噬细胞M2极化和PDAC的恶性表型。另外,研究结果表明GFPT2通过促进PDAC中IL-18的合成和分泌来促进巨噬细胞M2极化和恶性表型。GFPT2促进PDAC中YBX1的O-GlcNA酰化和核转位。
最后,研究结果提示GFPT2-YBX-1-IL-18信号通路的存在,并为PDAC的联合治疗提供了一些见解。
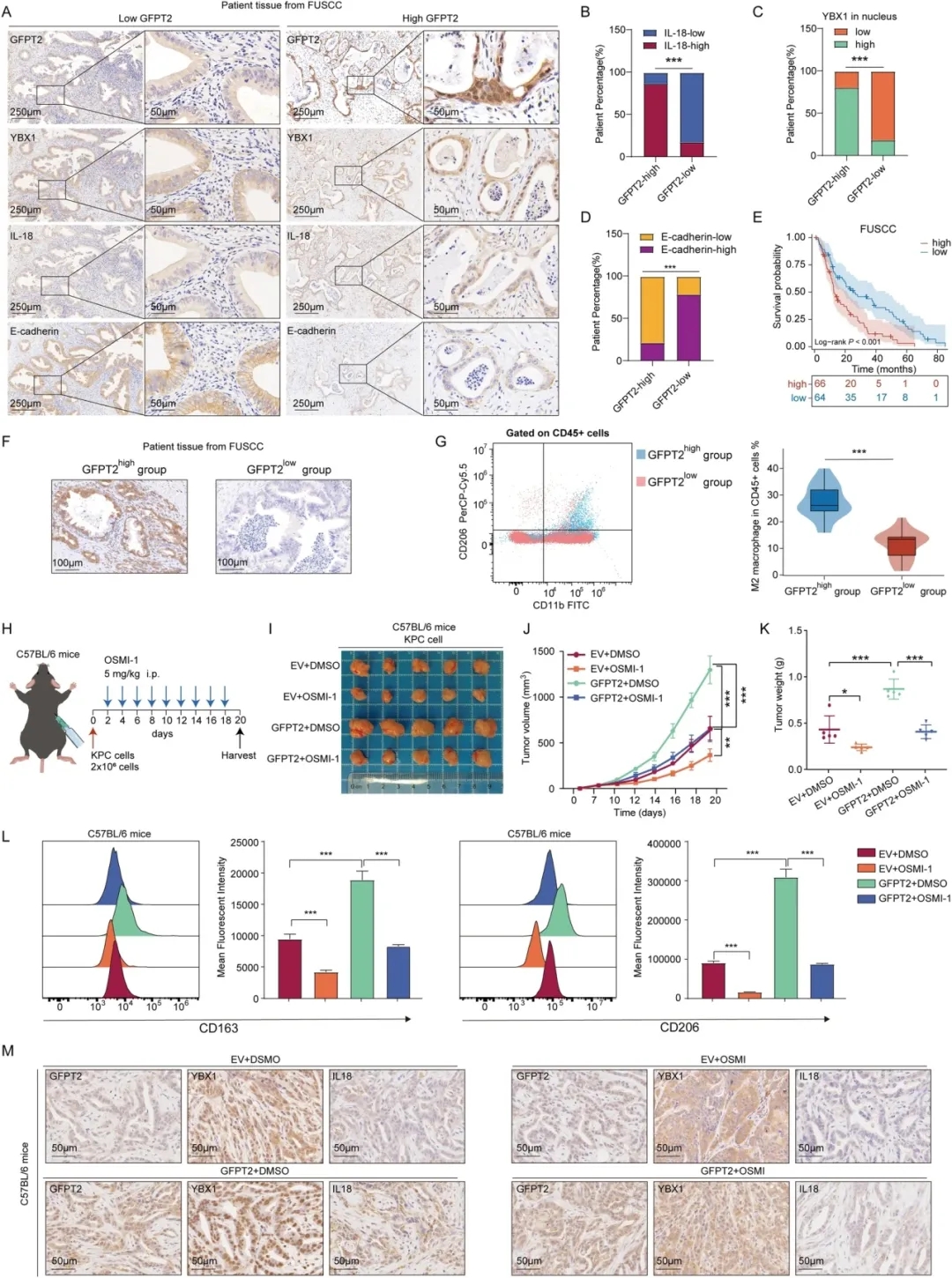
GFPT2-YBX1-IL-18信号通路在临床试样和体内实验中得到进一步证实
研究结论
03
综上所述,研究人员确定了GFPT2在PDAC中是一个免疫相关的预后基因,并且GFPT2介导的o - glcnac基化促进了YBX1的o - glcnac基化和核转位。核内定位的YBX1作为转录因子促进IL-18的转录和分泌。最终,IL-18促进了巨噬细胞M2型极化和PDAC的恶性表型。因此,本研究可能为联合治疗PDAC的HBP易感性和免疫治疗提供一些见解。(转化医学网360zhyx.com)
参考资料:
https://www.nature.com/articles/s41419-024-06589-7
注:本文旨在介绍医学研究进展,不能作为治疗方案参考。如需获得健康指导,请至正规医院就诊。
 腾讯登录
腾讯登录








还没有人评论,赶快抢个沙发