医校联动!湖南省肿瘤医院联合中南大学:揭示癌症治疗新策略
| 导读 | 放疗是治疗恶性肿瘤的主要方法之一。鼻咽癌是一种主要通过放疗治疗的恶性肿瘤,为研究癌症对放疗抵抗的机制提供了宝贵的模型。尽管一些研究报告称环状RNA参与了调节对放疗的抵抗,但其基本机制尚不清楚。 |
近日,湖南省肿瘤医院联合中南大学在期刊《Journal of Experimental & Clinical Cancer Research》发表了研究论文,题为“CircCDYL2 bolsters radiotherapy resistance in nasopharyngeal carcinoma by promoting RAD51 translation initiation for enhanced homologous recombination repair。本研究揭示了环CDYL2/EIF3D/RAD51轴在鼻咽癌放疗抵抗中的新作用。本研究不仅阐明了其潜在的分子机制,还强调了环CDYL2作为鼻咽癌治疗敏感化靶点和有潜力的预后分子标志物的潜力。

https://jeccr.biomedcentral.com/articles/10.1186/s13046-024-03049-0#Sec26
研究背景
01
鼻咽癌是一种起源于鼻咽黏膜的恶性肿瘤。其发病率具有明显的地域差异,东南亚、中国南方和非洲北部是高危地区。遗传易感性和环境因素,如EB病毒感染,共同促成了鼻咽癌的发生。由于相对对电离辐射敏感,放疗成为鼻咽癌的主要临床治疗手段。然而,尽管放疗在实现局部控制方面有效,但一些癌细胞对放疗具有抵抗力。这导致癌细胞持续存在、局部复发、远处转移,最终导致治疗失败和患者死亡。
环状RNA(circRNA)是一种近年来备受关注的新型非编码RNA。circRNA在鼻咽癌的进展中起着重要作用,既可作为致癌基因,也可作为肿瘤抑制基因发挥作用。本研究团队之前已经鉴定出许多与鼻咽癌发生和发展相关的circRNA,对肿瘤的侵袭、迁移、免疫逃避和放疗抵抗产生影响。此外,circRNA在调节肿瘤对放疗的抵抗方面发挥着关键作用,使其成为增强放疗敏感性的潜在分子靶点,并可作为临床诊断和预后指标。到目前为止,鼻咽癌放疗抵抗的分子机制尚未得到充分理解。值得注意的是,circRNAs在放疗抵抗中的作用日益受到重视,值得深入研究。
研究进展
02
环状RNA在多个层面上对基因表达产生显著影响,已成为生物医学研究的前沿和高度关注领域。环状RNA广泛存在于各种组织和细胞中,通过多种机制对基因表达进行调控。这些机制主要包括作为miRNA海绵或与蛋白质结合,从而调节下游基因转录或剪接过程。此外,环状RNA还参与表观遗传调控,某些情况下直接编码具有生物学功能的小肽。然而,关于环状RNA在辐射抵抗方面的研究,尤其是在鼻咽癌的DNA损伤修复方面的研究仍然有限。在这项研究中,研究人员发现鼻咽癌中环CDYL2的表达升高,且这种上调与患者不良预后相关。通过使用DR-GFP和EJ5-GFP报告系统,研究人员阐明了环CDYL2的过表达和敲低对HR修复而非NHEJ产生显著影响。免疫荧光染色实验表明,在鼻咽癌细胞经辐射治疗后,环状CDYL2促进了RAD51焦点的形成,RAD51是HR途径中的关键蛋白质。蛋白质印迹分析进一步证实,环状CDYL2提高了RAD51的表达。随后的研究揭示,环状CDYL2可有效促进RAD51的翻译,从而促进HR修复,并导致鼻咽癌对放疗产生抵抗。尤其是,RAD51是HR修复的关键组成部分,在多种实体肿瘤中表达较高,因此,它可能成为一种潜在的癌症治疗新靶点。
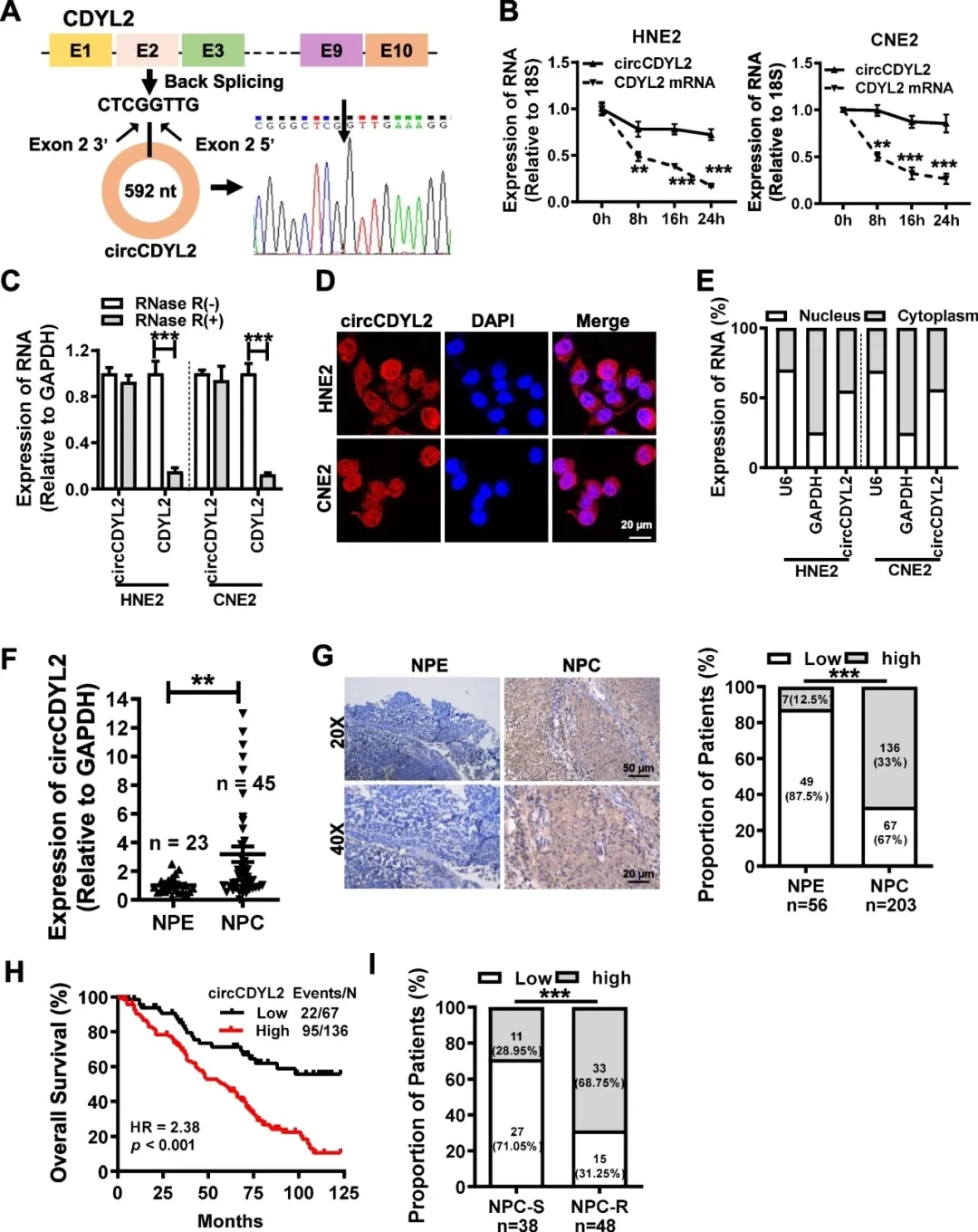
环CDYL2在鼻咽癌中高度表达,与不良预后相关
研究结论
03
总之,circCDYL2 是一个尚未充分研究的分子,其在肿瘤中的功能尚未阐明。本研究首次发现 circCDYL2 在鼻咽癌中具有明显的表达,与不良预后相关。在体内和体外实验中,研究人员证明 circCDYL2 能促进鼻咽癌细胞对放疗的抵抗。这些发现强调了 circCDYL2/EIF3D/RAD51 轴在调节鼻咽癌放疗抵抗方面的关键作用。此外,circCDYL2 有可能成为预测鼻咽癌不良预后的标志物。靶向 circCDYL2 和 RAD51 或是使鼻咽癌对放疗更敏感的有前景的治疗策略。(转化医学网360zhyx.com)
参考资料:
https://jeccr.biomedcentral.com/articles/10.1186/s13046-024-03049-0#Sec26
注:本文旨在介绍医学研究进展,不能作为治疗方案参考。如需获得健康指导,请至正规医院就诊。
 腾讯登录
腾讯登录








还没有人评论,赶快抢个沙发