将“冷肿瘤”转化为“热肿瘤”!上海交通大学等合作发现最新抗肿瘤免疫刺激策略
| 导读 | 肿瘤微环境(TME)在肿瘤进展中起着重要作用。在TME成分中,癌症相关成纤维细胞(CAFs)具有多种促癌作用,可诱导肿瘤免疫逃避和耐药性。调节CAF可能是增强全身抗肿瘤免疫力的潜在策略。 |
5月17日,上海交通大学和上海大学研究人员共同通讯在期刊《ADVANCED SCIENCE》上在线发表题为“Hydrogen Therapy Reverses Cancer-Associated Fibroblasts Phenotypes and Remodels Stromal Microenvironment to Stimulate Systematic Anti-Tumor Immunity”的研究论文,研究结果表明,这种氢疗法系统逆转了CAFs的免疫抑制表型,从而通过重塑肿瘤基质微环境提供了系统的抗肿瘤免疫刺激策略。

https://onlinelibrary.wiley.com/doi/10.1002/advs.202401269
研究背景
01
气疗是一种新兴且有前景的治疗方法,在抗肿瘤治疗方面引起了越来越多的关注。作为内源性气体递质,气体分子如一氧化氮(NO)、一氧化碳(CO)、硫化氢(H2S)和氢(H2)可以调节肿瘤细胞的生物学过程,包括血管舒张、神经传递、增殖和转移。其抗肿瘤作用的普遍接受机制是这些气体递质与各种蛋白质中的血红素铁中心结合,尤其是线粒体中的血红蛋白,诱导肿瘤细胞中的生物能量紊乱。在众多治疗气体中,H2即使在高浓度下也没有血液中毒风险,并显示出显著的安全益处。近年来,氢疗法被广泛应用于新型纳米药物抗肿瘤策略的开发中。然而,这些治疗策略主要集中在癌细胞本身,而氢气对TME的综合治疗作用还有待阐明。
在TME成分中,CAFs产生多种肿瘤促进作用,并可能诱导治疗无反应和耐药性。成纤维细胞被肿瘤细胞募集和激活。反过来,它们产生各种细胞外基质(ECM)蛋白,以建立阻碍药物递送和T细胞浸润的物理屏障。此外,CAFs还分泌大量的生长因子、细胞因子和趋化因子,如转化生长因子-β(TGF-β)、白细胞介素-6(IL-6)和CC-趋化因子配体2(CCL2),以降低T细胞反应并募集免疫抑制细胞(如Tregs、髓源性抑制细胞等),协助肿瘤免疫逃避。因此,CAFs可能是抗肿瘤治疗的一个有希望的靶点,调节CAFs可能是增强全身抗肿瘤免疫力的潜在策略。
研究发现
02
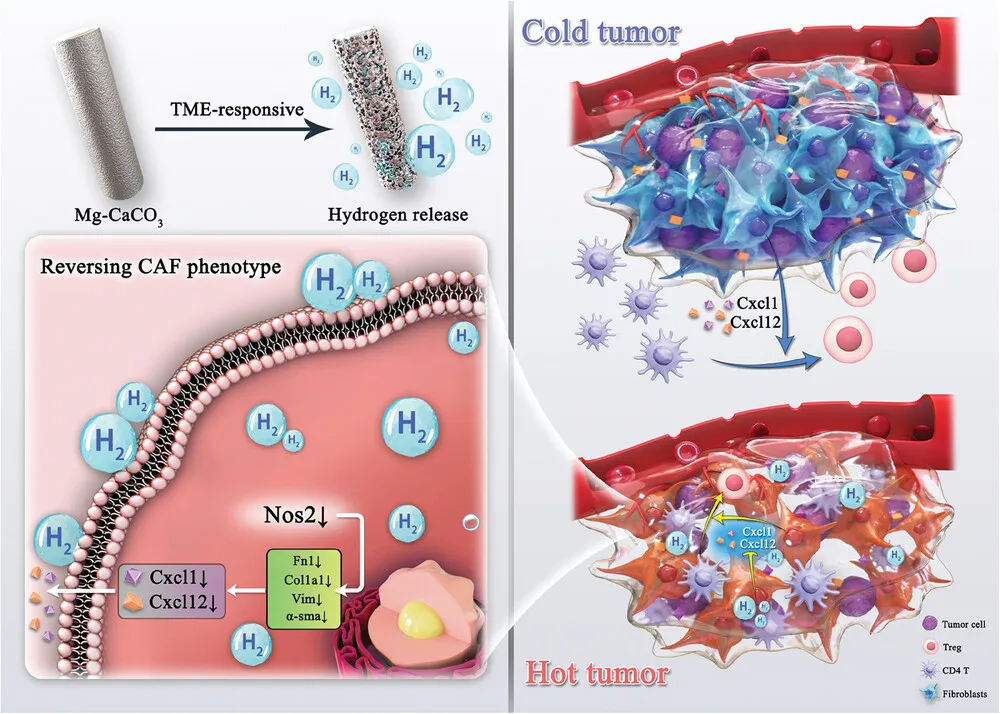
该研究观察到氢处理可以减轻CAFs的细胞内活性氧,并重塑CAFs的肿瘤促进和免疫抑制表型。因此,一种基于CaCO3的可控且TME响应的氢疗法纳米颗粒包覆镁体系(Mg-CaCO3)被开发。Mg-CaCO3的氢气疗法不仅能直接杀伤肿瘤细胞,还能抑制CAFs中的促肿瘤和免疫抑制因子,从而增强CD4 +T细胞的免疫活性。原位植入时,Mg-CaCO3能显著抑制肿瘤生长,将“冷”原发肿瘤转化为“热”,刺激系统抗肿瘤免疫,经“冷瘤”(4T1细胞)和“热瘤”(MC38细胞)的双侧肿瘤移植模型证实。这种氢疗法系统逆转了CAFs的免疫抑制表型,从而通过重塑肿瘤基质微环境提供了系统的抗肿瘤免疫刺激策略。
研究结论
03
综上所述,这种氢疗法系统逆转了CAFs的免疫抑制表型,从而通过重塑肿瘤基质微环境提供了系统的抗肿瘤免疫刺激策略。(转化医学网360zhyx.com)
参考资料:
https://onlinelibrary.wiley.com/doi/10.1002/advs.202401269
注:本文旨在介绍医学研究进展,不能作为治疗方案参考。如需获得健康指导,请至正规医院就诊。
 腾讯登录
腾讯登录









还没有人评论,赶快抢个沙发