触发铁死亡!重庆医科大学:发现治疗耐药肝癌患者的潜在靶点
| 导读 | 索拉非尼是晚期肝细胞癌(HCC)的标准一线治疗方案,但其疗效往往受到限制。 |
5月14日,重庆医科大学研究人员在期刊《Journal of Experimental & Clinical Cancer Research》上发表了研究论文,题为“PLAG1 interacts with GPX4 to conquer vulnerability to sorafenib induced ferroptosis through a PVT1/miR-195-5p axis-dependent manner in hepatocellular carcinoma”,新研究表明,索拉非尼可触发铁死亡,这是一种以脂质过氧化为特征的铁依赖性调节性细胞死亡(RCD)机制。本研究阐明了PLAG1在铁死亡中的作用,以及其作为索拉非尼治疗耐药的HCC患者的潜在治疗靶点的潜力。

https://jeccr.biomedcentral.com/articles/10.1186/s13046-024-03061-4
研究背景
01
HCC是全球癌症相关死亡的第二大常见原因,主要原因是诊断较晚,并且与饮酒等生活方式因素以及代谢综合征和病毒感染等疾病相关。索拉非尼是美国FDA批准的一种药物,其治疗HCC的一个主要问题是有效率低,仅在30%的HCC患者中显示出良好应答。此外,索拉非尼耐药往往在1年内发生。了解索拉非尼耐药背后的分子机制和识别新的靶点对于推进癌症治疗和提高患者生存率至关重要。
索拉非尼是一种口服多激酶抑制剂,已被证明对多种肿瘤有益,尤其是肝癌。其疗效源于其能够抑制多种激酶,从而导致肿瘤细胞生长停止、血管生成受限和诱导凋亡。然而,获得性或固有的细胞凋亡抵抗限制了索拉非尼诱导的细胞死亡的有效性。尤其是,索拉非尼还在肝癌细胞中触发了铁死亡,这是一种新发现的RCD形式。这种作用不是基于其多激酶抑制功能,而是增强药物的抗癌作用。与规律的凋亡和坏死不同,铁死亡是由细胞收缩和线粒体膜密度增加引起,从而导致铁依赖性脂质过氧化作用在细胞内累积。因此,通过索拉非尼促进铁死亡是增强肝癌治疗的潜在新方向。
研究进展
02
本研究旨在明确PLAG1在铁死亡抑制中的作用。为此,在MHCC97H和MHCC97L细胞中分别构建PLAG1敲低和过表达的肝癌细胞,然后用索拉非尼处理。蛋白质印迹和qRT-PCR分析证实索拉非尼在不改变PLAG1敲低和过表达效率的情况下降低了PLAG1蛋白和mRNA水平。铁死亡的一个关键特征是LPOs累积,通常由GSH耗竭触发。研究人员评估了MHCC97H和MHCC97L细胞的活力和GSH水平,以确定PLAG1是否可能是索拉非尼诱导的铁死亡的潜在靶点。有意思的是,与PLAG1上调相比,PLAG1敲低显著增强了索拉非尼对细胞活力的抑制和GSH的消耗。采用特异性探针检测铁死亡指标LPOs、脂质ROS和细胞内铁水平。结果表明,索拉非尼增强MHCC97H细胞的铁死亡,表现为细胞内铁、Liperfluo和脂质ROS水平升高。然而,它抑制了MHCC97L细胞的铁死亡,降低了这些标志物的水平。
从根本上说,铁死亡发生于氧化损伤和抗氧化防御之间失去平衡,导致猖獗的脂质过氧化和损害线粒体膜完整性。这种不稳定会升级为线粒体嵴破裂,引发铁死亡。透射电镜显示PLAG1抑制增加索拉非尼处理后线粒体膜密度,减小线粒体体积,诱导嵴膜崩解。综上所述,这些结果表明,PLAG1或是索拉非尼存在时促进铁死亡的一个有吸引力的战略靶点。
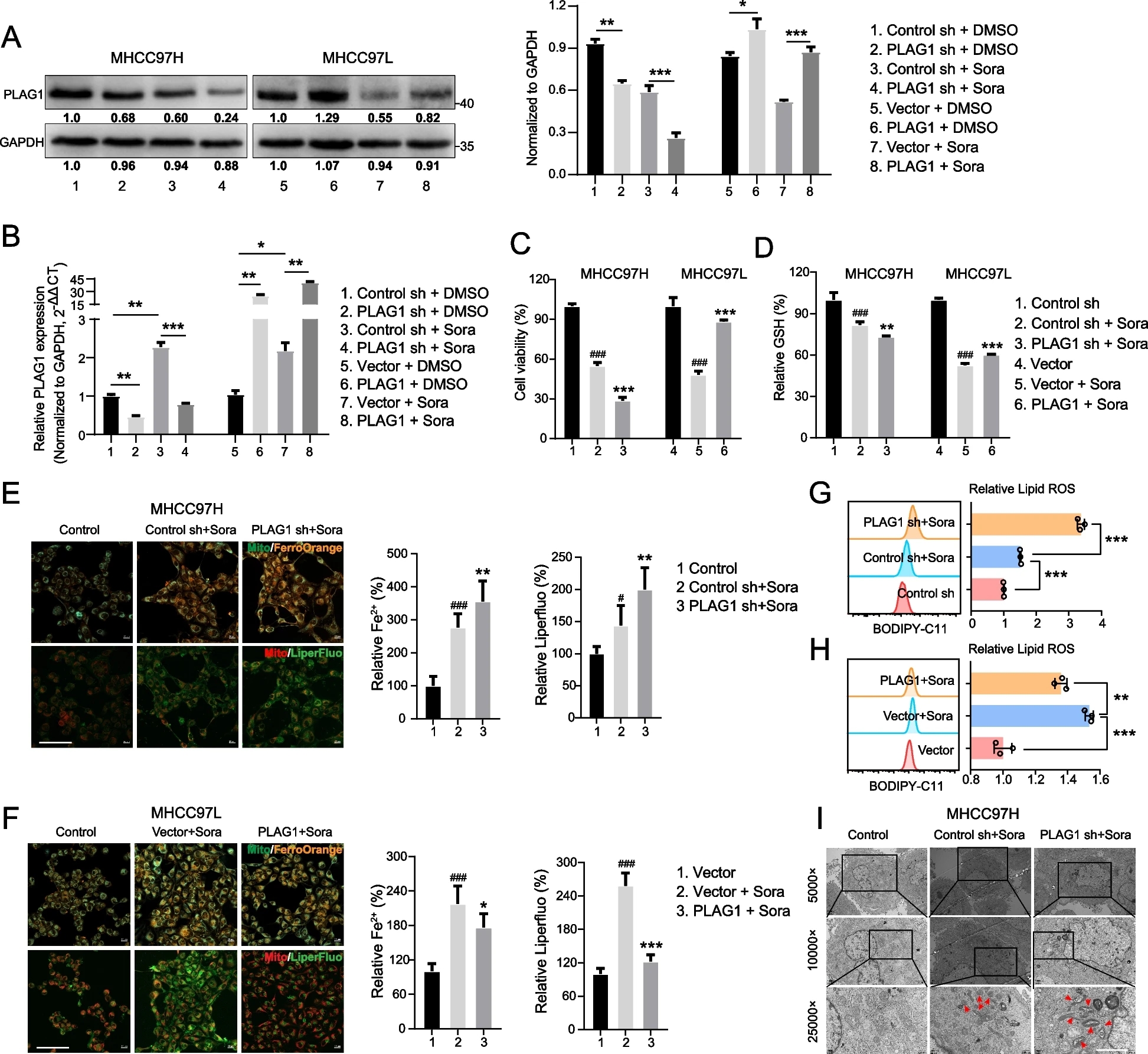
PLAG1可抑制索拉非尼诱导的铁死亡
研究结论
03
综上所述,本研究明确了PLAG1在索拉非尼诱导的铁死亡中的作用。研究人员发现PLAG1的下调通过调控PVT1/miR-195-5p轴增强铁死亡。此外,在体内和体外模型中,转录因子PLAG1在上游因子的刺激下与靶点GPX4相互作用并促进其转录,从而影响索拉非尼诱导的细胞死亡。这些发现强调了PLAG1与GPX4相互作用,通过PVT1/miR-195-5p轴依赖的方式克服索拉非尼诱导的铁死亡的脆弱性,并加强了PLAG1作为索拉非尼治疗HCC的治疗靶点的潜力。(转化医学网360zhyx.com)
参考资料:
https://jeccr.biomedcentral.com/articles/10.1186/s13046-024-03061-4
注:本文旨在介绍医学研究进展,不能作为治疗方案参考。如需获得健康指导,请至正规医院就诊。
 腾讯登录
腾讯登录









还没有人评论,赶快抢个沙发