水凝胶:医学革命的新希望!中山大学肖泽聪团队揭示先进治疗中的突破性潜力!
| 导读 | 在细胞治疗的背景下,团队讨论了水凝胶克服主流细胞治疗范式,面临的现有挑战,详细讨论了水凝胶在提高细胞治疗疗效方面的优势,并列出了它们在不同疾病场景中应用的具体例子。 |
2024年7月1日,中山大学附属第三医院纳米医学中心肖泽聪团队在期刊《Signal Transduction and Targeted Therapy》上发表了题为“Harnessing the potential of hydrogels for advanced therapeutic applications: current achievements and future directions”的研究论文。团队概述了水凝胶临床应用的最新进展和挑战,以及未来的研究方向,特别是在与先进生物制造技术的整合方面。

https://www.nature.com/articles/s41392-024-01852-x
研究背景
01
水凝胶是高度水合的三维(3D)聚合物基质,由于其出色的生物相容性、化学可改性和物理可调性,以及相对简单的加工程序,在医学和生物医学领域具有广阔的前景。水凝胶已被证明在支持细胞活力和功能方面具有潜力,并促进有针对性的交付,及治疗剂的控释。因此,将水凝胶组合到细胞治疗剂中,不仅可以保证其在体内的治疗效果和功效,还可以最大限度地减少系统不良反应,有望拓宽这些方式的治疗窗口。
尽管早期水凝胶由于其结构简单,而可能表现出有限的柔韧性,从而限制了它们在复杂治疗环境中的适用性,以及基于动态释放的治疗策略。但是,目前的合成和改性技术已经足够成熟,可以显著推进这种材料。例如,已经开发了多种响应性水凝胶,来对特定的生物和病理刺激(例如,PH 值、温度、活性氧(ROS),和其他外源性刺激),以满足特定疾病的复杂要求和不断升级的临床需求。通过调整它们的化学成分、交联策略和物理结构,新开发的水凝胶具有多种特性,能够直接调节细胞行为,引发特定的细胞表型,并实现控释和疾病特异性靶向。随着生物医学工程技术的快速发展,在细胞疗法、免疫疗法、基因疗法、再生医学的进步,以及向精准医学转变的推动下,水凝胶的应用有望进一步扩大。
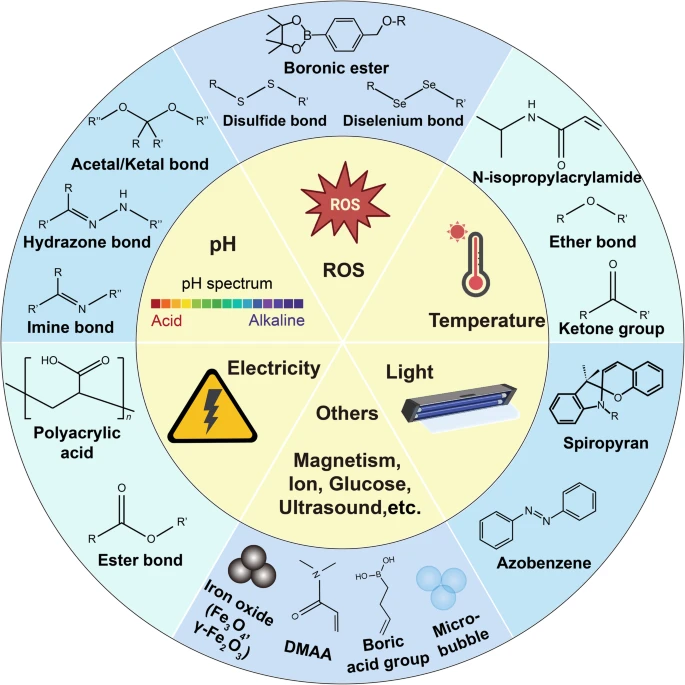
该原理图总结了目前用于高级疗法的水凝胶响应设计,包括 ROS 响应、pH 响应和热响应设计等,还列出了这些响应式设计中使用的代表性基团(例如,ROS 响应设计中使用的硼酸酯)和结构(例如,超声响应设计中使用的微泡)。
研究进展
02
探索水凝胶在克服细胞治疗挑战中的作用
迄今为止,FDA批准的大多数细胞治疗产品,都来自自体细胞来源。然而,同种异体细胞,或者更准确地说,“现成的”产品,由于它们在大规模制造、来源可用性和成本效益方面的优势,代表了该领域的未来。使用同种异体细胞的一个关键挑战,是克服免疫排斥反应。然而,服用免疫抑制剂的传统方法,可能会使患者面临严重感染的高风险,而新的遗传策略,如工程HLA敲除细胞,可能会导致更多隐藏和无法控制的问题。水凝胶为减轻同种异体细胞的免疫排斥,提供了一种相对直接和安全的替代方案,并可作为局部疾病的治疗选择。将移植细胞封装在生物相容性水凝胶基质中,可以在同种异体细胞和宿主之间形成免疫隔离物理屏障,有效地保护移植细胞免受细胞间接触介导的免疫反应,包括识别、裂解和吞噬作用。同时,固有的亲水性和多孔结构允许氧气、营养物质、细胞废物和治疗因子的双向交换,从而延长细胞存活,并确保体内治疗效果。这种可行性已在干细胞来源胰岛的水凝胶涂层的使用中得到证明。这种凝胶涂层成功地阻止了宿主对同种异体胰岛植入的免疫反应,同时允许葡萄糖、氧气和胰岛素从移植细胞分泌,在MHC不匹配模型中,显示出逆转糖尿病的巨大潜力。同样,将MSC封装在I型胶原水凝胶中,已被证明可以降低其免疫原性并维持其活力,从而显著减少小胶质细胞活化和星形胶质细胞募集。这种方法有效地解决了移植后中枢神经系统(CNS)细胞存活率低的常见问题。因此,采用生物相容性强、耐受性良好的水凝胶,特别是那些来自天然细胞外基质成分的水凝胶,可能是通过减少免疫排斥,来支持细胞存活和成功植入的可行方法。
此外,最大限度地减少患者的等待时间,是细胞治疗未来的另一个关键目标。除了利用预先制备的同种异体或通用细胞源外,研究人员还在探索用于快速体外扩增或体内基因修饰的水凝胶平台,从而简化制造过程。例如,采用三性离子水凝胶培养,使造血干细胞和祖细胞的频率增加了73倍,同时保留了它们的长期再填充能力。这种快速膨胀和自我更新能力的维持,可归因于凝胶的3D结构、超亲水性、防污和两性离子特性。这些特性可以使该培养系统更接近地模拟体内生态位,并有效地减少非特异性蛋白质的吸收和相互作用,从而避免意外分化。更引人注目的是,科学界已经出现了几种体内重编程制造范式,以直接在靶位点内实现基因修饰,引起了相当大的关注。例如,Chen及其同事开发了一种基于脑ECM模拟肽的可注射水凝胶,旨在将载有CAR质粒的纳米转运蛋白,转运到多形性胶质母细胞瘤(GBM)的切除腔中。这种富含CAR基因的水凝胶,成功地对巨噬细胞进行了原位重编程,产生了CD133特异性CAR巨噬细胞,增强了对神经胶质瘤干细胞的吞噬活性。当与使用该水凝胶储库的局部递送抗CD47抗体结合使用时,该方法有效地防止了GBM的术后复发,并在小鼠模型中诱导了长期抗肿瘤免疫。同样,基于海藻酸盐的冷冻凝胶支架,已被证明通过共同加载人体外周血单核细胞和CD-19编码的逆转录病毒颗粒,来生产体内CAR-T细胞的能力。这种支架将T细胞活化、扩增和转导,简化为单一的原位工艺,将制造时间从传统的几周,显著缩短到一天。水凝胶介导技术的这些进步,极大地促进了更快的制造程序,并预示着下一代细胞疗法的光明前景。
最后,就安全性问题而言,水凝胶仍然是一种可行的解决方案。因为它们具有灵活性和多功能性,可以控制转移细胞的药代动力学和生物分布。从根本上说,基于水凝胶的基质,可以建立一个局部的储存库,用于转移细胞的相对延长的释放。首先,这种细胞负载库,可以通过调整水凝胶的降解模式、动态变形和溶胀特性,来实现可控的转移细胞的流出速率,从而降低CRS的风险,这通常是由于效应免疫细胞在给药后,快速涌入体内造成的。在这种情况下,由于体内转移细胞的更持久存在,ACT治疗的有效性也将延长。另一方面,这种局部平台可以通过直接将细胞递送到焦点部位,或通过招募系统输注的细胞,来最大限度地减少转移细胞对非靶组织的暴露,从而减少甚至避免OTOT毒性效应。
此外,基于水凝胶的方法,提供了一种战略方法,可以规避与全身暴露于支持性细胞因子相关的副作用,这些细胞因子通常需要与过继转移细胞共同给药。这些细胞因子或支持剂(例如生长因子、抗体或共刺激分子)可以通过肝素功能化或无铜点击反应等化学修饰,安全地固定在水凝胶的骨架中,或者通过物理相互作用在凝胶中保持可溶性形式,从而在靶向位点实现受控释放。例如,已经开发了一种由疏水修饰的纤维素聚合物网组成的水凝胶,用于共同递送CAR-T细胞和IL-15,这是一种有效的T细胞激活剂。细胞因子和凝胶成分之间的疏水相互作用,大大减缓了IL-15从凝胶中的快速扩散,为CAR-T治疗提供了一种更安全、更持久有效的模式。更先进的策略,可以通过将携带IL-15的纳米凝胶背包,连接到转移的T细胞表面,以增强其抗肿瘤活性的设计。这种创新方法,将IL-15的刺激作用,限制在转移的细胞上,而不是引起全身效应,从而显著提高了ACT治疗的安全性。这些基于水凝胶的细胞治疗的战略方法,提高了治疗应用的安全性和有效性,强调了它们在应对当前挑战和塑造细胞治疗的未来潜力。
水凝胶介导的细胞治疗应用
近年来,水凝胶介导的干细胞递送,已成为伤口愈合、促进上皮化、血管生成和调节炎症的重要方法,为组织损伤治疗提供了新的策略。干细胞由于其多向分化和自我复制,对组织修复有效。然而,直接注射可能会受到微环境中炎症反应的影响,从而危及干细胞活力和修复成功。能够封装干细胞并保持其活力的水凝胶,已被开发成各种配方,并与不同的干细胞一起使用,以研究它们对组织修复的影响,包括心脏、肾脏、软骨和骨骼。
在皮肤修复应用中,立即治疗广泛的皮肤缺损,对于预防感染和过度炎症等并发症至关重要,尤其是在严重烧伤的情况下。生物材料的最新进展,已经推动了水凝胶的应用。理想水凝胶的设计(具有高透氧性、抗菌性能、细胞粘附等),在维持移植细胞功能和作为有效的伤口敷料方面显示出希望。例如,细菌纤维素是一种具有高吸水性、纯度和孔隙率的天然聚合物,当与细胞递送相结合时,显示出伤口愈合的潜力。两亲性材料,如磺基甜菜碱衍生物,具有亲水性和抗蛋白非特异性粘附特性,有助于预防伤口感染和抵抗异物反应。一种磺基甜菜碱衍生的葡聚糖(DSC)水凝胶,表现出优异的抗污染性,包括抗细菌和非特异性蛋白质粘附。将DSC与脂肪来源的干细胞(ADSC)注射到烧伤小鼠体内可减少细菌粘附、免疫识别和炎症,为ADSC增殖提供有利环境。
注射水凝胶对血液供应不良的深部或慢性伤口特别有益。例如,糖尿病伤口或全层皮肤损伤。传统的敷料或移植细胞,通常无法到达深层伤口,使长期和难治性皮肤伤口愈合复杂化。可注射的水凝胶,可以直接进入这些层,创造一个有利的微环境,来保护递送的细胞,从而保持其活力和功能。除干细胞外,其他组织细胞与水凝胶结合,如Trem2巨噬细胞,在伤口愈合方面显示出临床潜力。移植的Trem2巨噬细胞调节炎症反应,减少伤口部位的慢性炎症和纤维化。此外,角质形成细胞和成纤维细胞的协同作用加速了再上皮化。
在心肌梗死 (MI) 中,成人心脏有限的再生能力,表现为催化心肌重塑的坏死组织的扩张。同时,纤维化瘢痕会破坏电通信,梗死心肌的血液供应不足会加剧心脏损伤,增加心力衰竭的风险。干细胞移植,越来越被认为是心肌梗死的可行治疗选择。 多项研究证实了,水凝胶与细胞结合,对心脏功能和纤维化的积极作用。在这种情况下,水凝胶提供机械支撑,以维持受损区域的结构完整性并调节细胞递送。它们可提高细胞保留和存活率,确保治疗细胞的有效定位和功能。一个主要的挑战是,由于心肌纤维化瘢痕形成,导致机械和电信号传输的损失,因为水凝胶缺乏与宿主心肌组织的机电耦合,并且难以监测植入,可能会影响治疗结果。引入导电生物材料,如四苯胺(TA)、氧化石墨烯、碳纳米管和金属颗粒,可以缓解这些问题。
免疫疗法已成为肿瘤治疗的重要方法,ACT细胞,特别是CAR-T和TCR-T细胞,在治疗多种肿瘤方面显示出疗效。重点,特别是对CAR-T和TCR-T细胞的重视,与它们的治疗潜力相一致。然而,由于各种因素,CAR-T细胞治疗实体瘤的有效性面临局限性。为了克服这个问题,有人建议使用生物材料,特别是水凝胶来改善治疗。研究表明,生物材料支架(如水凝胶)可显著激活肿瘤部位的CAR-T细胞,并实现局部细胞因子递送,从而最大限度地减少全身暴露并降低毒性。此外,需要细胞因子的高CAR-T细胞活化,通常由于高浓度细胞因子的扩增而导致全身效应。研究表明,修饰水凝胶结构可以影响肿瘤部位T细胞的行为,通过控制T细胞活性,更精确地靶向实体瘤的可能性。鉴于免疫抑制性TME带来的挑战,未来的研究可能涉及,将免疫刺激剂和检查点抑制剂掺入水凝胶载体中,以进行CAR-T递送。这种方法可以增强内源性免疫细胞的募集,放大抗肿瘤反应。这些策略也适用于其他递送至局部肿瘤区域的过继细胞疗法(TCR-T、NK、DC 等)。
为了解决肿瘤切除后的复发问题,开发针对特定肿瘤特征(如TME)量身定制的响应性可降解水凝胶,对于监测复发性肿瘤细胞至关重要。研究表明,将NK细胞与水凝胶结合,可以有效预防HCC复发。此外,水凝胶与细胞结合,显示出远端肿瘤治疗的潜力。格罗斯科普夫的研究,在聚合物纳米颗粒水凝胶中使用CAR-T细胞和IL-1,在未经治疗的肿瘤小鼠中显示出快速治愈,突出了这种方法通过直接注射或导管输送治疗隐匿性转移或肿瘤的疗效。尽管与瘤周注射相比,其治疗时间更长。
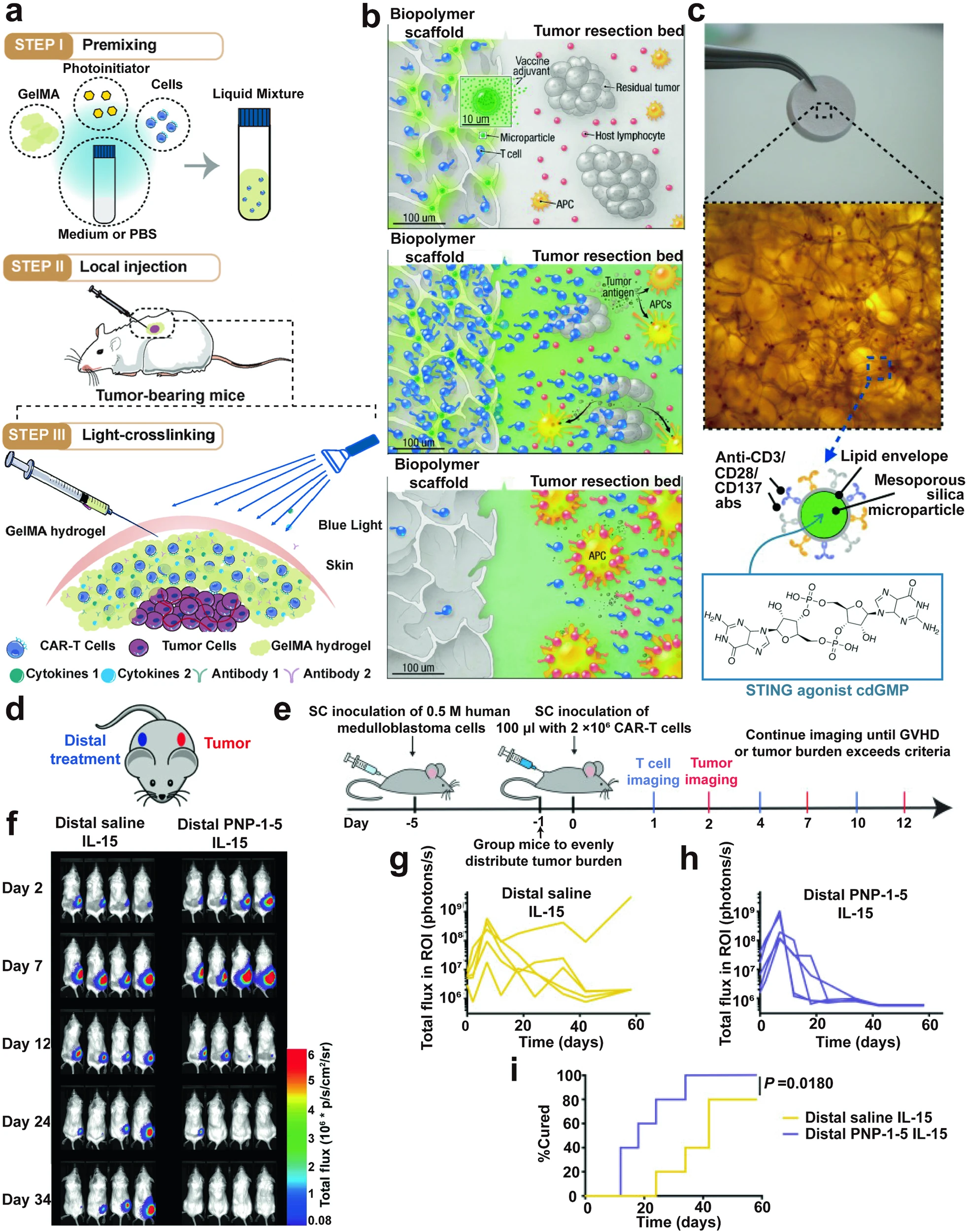
注射给药系统的安装过程示意图。
研究结论
03
水凝胶在基于细胞疗法中的广泛应用,凸显了它们在医学领域的巨大潜力,特别是在组织工程和癌症治疗等关键领域。
水凝胶应用的未来研究,将优先考虑:(1)水凝胶材料的安全性和稳定性。此外,研究人员应更加关注通过优化水凝胶的物理特性(包括弹性、孔隙结构和机械鲁棒性),来提高细胞和非细胞治疗疗效的策略。这种优化可以降低不良反应的风险,同时保持材料的生物相容性,从而提供更安全、更有效的治疗方法。水凝胶物理环境的精确调整,不仅有助于模拟有利于细胞生长的自然微环境,增强细胞粘附、增殖和分化,而且还可以细致控制药物释放机制,显著提高治疗特异性和有效性。
(2)开发用于细胞或非细胞治疗的多功能和多反应水凝胶平台,是另一个重要的研究途径。这些平台可响应温度、PH、光和电磁场等各种外部刺激,从而在临床环境中,实现更精确和有针对性的治疗药物递送。这些平台的多响应性,不仅促进了疾病部位的特定环境条件依赖性药物释放,而且还动态调整其物理特性,以支持组织发育和成熟,为个性化治疗提供了实质性支持。这些特性凸显了多功能和多响应水凝胶平台,在癌症治疗、组织再生和炎症控制等各个领域的临床应用的巨大潜力。
(3)通过整合材料科学、细胞生物学、医学工程和临床医学的知识和技术,增强跨学科合作的优势,将促进更复杂、更有效的治疗策略的创建。例如,应用3D / 4D打印技术,来设计和制造支持细胞生长和组织发育的患者特定水凝胶支架。此外,3D/4D打印技术能够精确操纵水凝胶中的药物或细胞,促进局部或靶向治疗,以优化治疗效果,同时最大限度地减少对邻近健康组织的影响。结合微流控技术,可以在微观尺度上模拟ECM,精确控制药物释放、细胞相互作用和细胞对环境变化的反应,从而为疾病建模、药物测试和机理研究,提供有价值的工具。
总之,未来的研究,应继续探索和完善基于水凝胶技术的安全、适应性和可控的治疗平台,以扩大其在基于细胞治疗中的应用。
 腾讯登录
腾讯登录









还没有人评论,赶快抢个沙发