【Nature子刊】深圳大学吴昊团队发文:揭示肺癌免疫治疗新思路
| 导读 | 免疫逃逸是恶性肿瘤尤其是非小细胞肺癌(NSCLC)的重要特征之一。越来越多的研究表明n6 -甲基腺苷(m6A)在NSCLC免疫逃逸中的作用。 |
7月11日,深圳大学吴昊研究团队在期刊《Cell Death Discovery》上发表了研究论文,题为“YTH domain family protein 3 accelerates non-small cell lung cancer immune evasion through targeting CD8+ T lymphocytes”,本研究旨在探讨m6A阅读器YTH结构域家族蛋白3 (YTHDF3)在NSCLC免疫逃逸中的作用及其机制。YTHDF3在NSCLC组织中高表达,可作为NSCLC患者总生存期的独立预后因素。在功能上,上调YTHDF3的表达可削弱CD8+ T细胞的抗肿瘤活性,加重NSCLC的免疫逃逸,而YTHDF3的沉默可恢复CD8+ T细胞的抗肿瘤活性,抑制NSCLC的免疫逃逸。此外,上调YTHDF3可降低NSCLC细胞的凋亡。机制上,PD-L1是YTHDF3的下游靶点,YTHDF3可以上调PD-L1 mRNA的转录稳定性。YTHDF3靶向PD-L1部分通过逃逸效应细胞杀伤CD8+ T细胞介导的杀伤和抗肿瘤免疫促进NSCLC免疫逃逸。综上所述,本研究揭示了m6A修饰对CD8+ T细胞介导的NSCLC抗肿瘤免疫的影响,为肺癌的肿瘤免疫治疗提供了新的思路。

https://www.nature.com/articles/s41420-024-02084-2#Sec10
背景知识
01
非小细胞肺癌(Non-small-cell lung cancer, NSCLC)占肺癌的很大比例(80-85%),是最常见的恶性肿瘤,也是全球肿瘤死亡的主要原因。NSCLC的5年生存率维持在20%左右。在临床上,肿瘤免疫治疗可恢复或增强CD8+ T细胞或其他免疫细胞的效应功能。因此,更好地理解NSCLC的免疫治疗具有重要意义。
免疫逃逸是恶性肿瘤的重要标志,是指肿瘤细胞逃避免疫细胞识别和杀伤的现象。NSCLC浸润期的免疫逃避过程不断演变,并且与肿瘤间/肿瘤内的异质性相关,这有助于检查点阻断(ICB)的免疫治疗。肿瘤免疫微环境(TME)与肿瘤免疫治疗疗效密切相关,其特征可显著影响肿瘤的进展和转移。TME对NSCLC的发生发展至关重要,NSCLC细胞与免疫细胞(T细胞、B细胞)相互作用,促进免疫逃逸。例如,在NSCLC中,ILT4过表达通过损害T细胞反应和招募m2样TAMs来抑制肿瘤免疫,防止免疫抑制,增强PD-L1抑制剂在EGFR野生型NSCLC中的疗效。
程序性细胞死亡蛋白配体-1 (PD-L1)是PD-1配体中的一种,已被证明是有价值的肿瘤预后生物标志物。在许多癌症中,PD-L1主要表达于癌细胞、抗原提呈细胞(APCs)或肿瘤浸润细胞。在NSCLC中,PD-L1的功能已得到广泛报道。例如,在NSCLC中,PD-L1的表达受致癌驱动因素的调节,如表皮生长因子受体(EGFR)或间变性淋巴瘤激酶(ALK)。此外,PD-L1表达与晚期/转移性NSCLC患者较短的生存期相关。因此,PD-L1在肿瘤免疫逃逸中发挥重要作用。
沉默YTHDF3可恢复CD8+ T细胞抗肿瘤活性,抑制NSCLC免疫逃逸
02
为了验证YTHDF3在NSCLC免疫逃逸中的作用,研究人员进行了以下一系列实验。首先,在NSCLC细胞(A549细胞)中进行YTHDF3沉默。在NSCLC细胞中,凋亡分析显示YTHDF3沉默增加了shRNA转染的A549细胞的凋亡率。构建共培养体系,检测CD8+ T细胞对NSCLC细胞的抗肿瘤活性。将活化的CD8+ T细胞与NSCLC细胞共孵育48 h后,检测CD8+ T细胞分泌的细胞因子,包括IFN-γ、TNF-α、颗粒酶B和穿孔素。与YTHDF3沉默的A549细胞共培养后,CD8+ T细胞分泌的IFN-γ、TNF-α、颗粒酶- B和穿孔素明显增加。CD8+ T细胞与活化的CD8+ T细胞共孵育后,LDH释放实验结果显示,与YTHDF3沉默转染的A549细胞共培养后,CD8+ T细胞具有更高的细胞毒活性。YTHDF3沉默引起NSCLC细胞表面PD-L1表达显著降低。总之,这些发现表明,YTHDF3沉默恢复了CD8+ T细胞的抗肿瘤活性,从而抑制NSCLC的免疫逃逸。
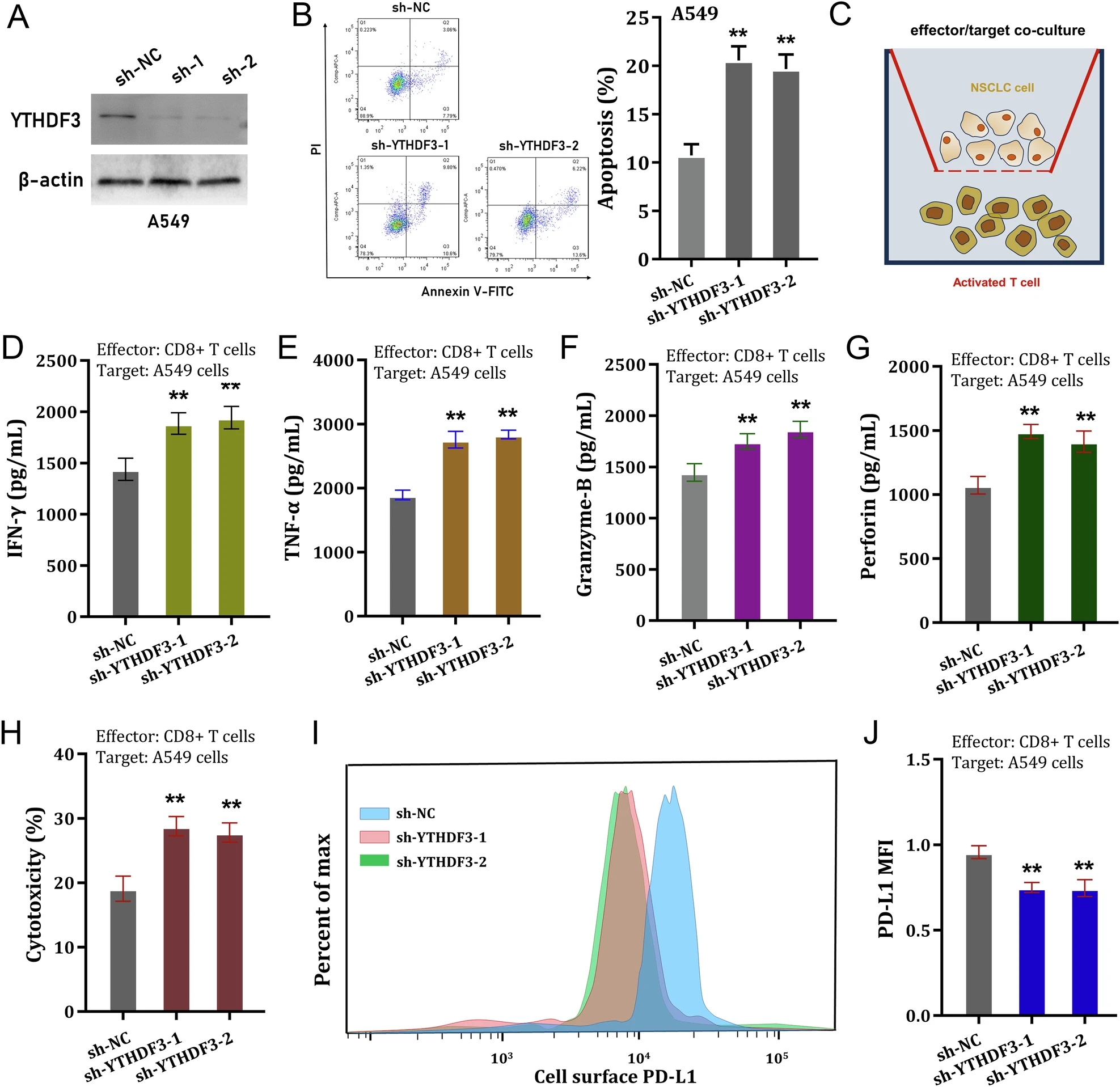
沉默YTHDF3可恢复CD8+ T细胞抗肿瘤活性,抑制NSCLC免疫逃逸
YTHDF3的上调损害了CD8+ T细胞的抗肿瘤活性,从而恶化了免疫逃逸
03
由于YTHDF3沉默恢复了CD8+ T细胞的抗肿瘤活性,接下来的实验检测了YTHDF3过表达对NSCLC细胞的作用。在H1299细胞中构建YTHDF3过表达转染。细胞凋亡分析显示YTHDF3过表达降低了YTHDF3过表达转染的H1299细胞的凋亡率。在CD8+ T细胞与NSCLC细胞共培养体系中,检测CD8+ T细胞分泌的细胞因子,包括IFN-γ、TNF-α、颗粒酶B和穿孔素。结果表明,与YTHDF3过表达的H1299细胞共培养后,CD8+ T细胞分泌的IFN-γ、TNF-α、颗粒酶B和穿孔素显著降低。CD8+ T细胞与活化的CD8+ T细胞共培养后,LDH释放实验结果显示,与YTHDF3过表达转染的H1299细胞共培养后,CD8+ T细胞的细胞毒活性降低。此外,YTHDF3过表达导致NSCLC细胞表面PD-L1的表达显著升高。总的来说,这些发现表明,YTHDF3上调损害了CD8+ T细胞的抗肿瘤活性,恶化了免疫逃逸。
研究小结
04
综上所述,YTHDF3可能通过抑制细胞毒性CD8+ T细胞介导的杀伤和抗肿瘤免疫而加速NSCLC的免疫逃逸。本研究为NSCLC的表观遗传学m6A修饰和CD8+ T细胞介导的抗肿瘤免疫提供了重要的见解,为NSCLC的免疫治疗提供了新的思路。(转化医学网360zhyx.com)
参考资料:
https://www.nature.com/articles/s41420-024-02084-2#Sec10
【关于投稿】
转化医学网(360zhyx.com)是转化医学核心门户,旨在推动基础研究、临床诊疗和产业的发展,核心内容涵盖组学、检验、免疫、肿瘤、心血管、糖尿病等。如您有最新的研究内容发表,欢迎联系我们进行免费报道(公众号菜单栏-在线客服联系),我们的理念:内容创造价值,转化铸就未来!
转化医学网(360zhyx.com)发布的文章旨在介绍前沿医学研究进展,不能作为治疗方案使用;如需获得健康指导,请至正规医院就诊。
 腾讯登录
腾讯登录









还没有人评论,赶快抢个沙发