“黄连素”抗肝癌!浙江大学王青青团队发文:发现抑制肝癌进展新策略
| 导读 | 越来越多的证据表明,黄连素(BBR)在肝细胞癌(HCC)中具有抗癌作用。然而,BBR调控肝癌免疫微环境的机制尚未完全阐明。 |
8月13日,浙江大学王青青研究团队在期刊《Advanced Science》上发表了研究论文,题为“Berberine Protects against Hepatocellular Carcinoma Progression by Regulating Intrahepatic T Cell Heterogeneity”,本研究中,研究人员建立了原位肝癌小鼠模型,并使用不同剂量的BBR进行治疗。BBR可有效降低肝癌小鼠的肿瘤负荷。流式细胞术检测显示BBR治疗后肿瘤免疫格局的变化,揭示了T淋巴细胞效应功能的增强。其中,BBR降低了TCRbhiPD-1hiCD69+CD27+效应性CD8+ T淋巴细胞的比例,升高了Ly6ChiTCRb+CD69+CD27+CD62L+中央记忆性CD8+ T淋巴细胞的比例。单细胞RNA测序进一步阐明了BBR对肝脏免疫细胞转录谱的影响,并证实了肝癌免疫微环境中T淋巴细胞的表型异质性。此外,BBR可能通过调节细胞因子介导的免疫细胞之间的受体-配体相互作用来调节肝癌中的抗肿瘤免疫。综上所述,这些发现提高了对BBR在预防HCC方面的作用的理解,强调了BBR在调节肝内T细胞异质性方面的作用。BBR有望成为一种抑制肝癌进展的治疗策略。

https://onlinelibrary.wiley.com/doi/10.1002/advs.202405182
背景知识
01
肝癌是癌症相关死亡的第三大原因,其中肝细胞癌(HCC)是最常见的原发性肝癌类型。在过去的十年中,包括免疫检查点抑制剂(ICIs)、酪氨酸激酶抑制剂和单克隆抗体在内的全身治疗已经改变了HCC的传统治疗模式。据估计,单药ICIs为15-20%的应答者提供了实质性的临床益处,但面临生物标志物无法识别这一人群的挑战。因此,有必要探索新的治疗策略来改善HCC的治疗前景。
肝脏免疫微环境在肝癌的发生过程中起着至关重要的作用。例如,观察到浸润肿瘤的T细胞和B细胞相互作用,导致局部免疫激活和对肝癌进展的控制。一项使用单细胞RNA测序(scRNA-seq)的研究揭示,在肝癌微环境中,耗竭的CD8+T细胞和浸润的Treg细胞可能发生克隆扩增。与在原发性肝癌中观察到的典型的耗竭状态不同,早期复发肝癌中的CD8+T细胞表现出类似于固有免疫的降低的细胞毒性和克隆扩增,这可能解释了与肝癌相关的受损抗肿瘤免疫功能和不良预后。因此,调节肿瘤免疫微环境(TIME)可能有助于开发有效的肝癌治疗方法。
黄连素(BBR)是一种从黄连、黄柏等植物的根、树皮和根茎中提取的异喹啉生物碱,具有多种药理作用。之前的研究表明,BBR通过减少糖异生和脂质合成来缓解非酒精性脂肪性肝病。此外,BBR还被报道通过激活PPARδ触发细胞凋亡并促进肠道微生物产生的丁酸来抑制肝癌。近年来,研究人员越来越关注BBR的免疫调节特性。研究人员发现,BBR通过降低PD-L1表达和增强肿瘤浸润T细胞的免疫功能来抑制非小细胞肺癌。另一项研究表明,BBR促进免疫抑制性M2巨噬细胞向肿瘤杀伤性M1巨噬细胞转化,恢复T细胞的抗肿瘤细胞毒性。然而,BBR调节肝癌免疫反应的确切机制尚未被发现。
BBR治疗减轻肝癌小鼠的肿瘤负荷
02
为了研究BBR治疗HCC的潜力,研究人员建立了原位HCC小鼠模型。在适应性喂养一周后,将Hepa 1-6细胞注射到小鼠左叶肝脏中,然后给予小鼠腹腔内BBR注射。根据BBR剂量,将小鼠分为三组:HC组(对照组)、LB组(低剂量BBR,10 mg/kg)和HB组(高剂量BBR,30 mg/kg)。每两天给予BBR一次,共14天。在处死小鼠后,收集小鼠肝脏并切除肿瘤组织进行进一步分析。结果显示,三组小鼠体重差异无统计学意义。然而,接受BBR治疗的小鼠肿瘤体积明显减小。特别是与LB组相比,高剂量BBR治疗显示出更显著的肿瘤体积和重量减少(p<0.05),表明BBR在减轻小鼠HCC负担方面呈剂量依赖性趋势。综上所述,BBR在小鼠模型中显示出减少肿瘤负荷的功效,提示其可能具有预防HCC进展的功能。
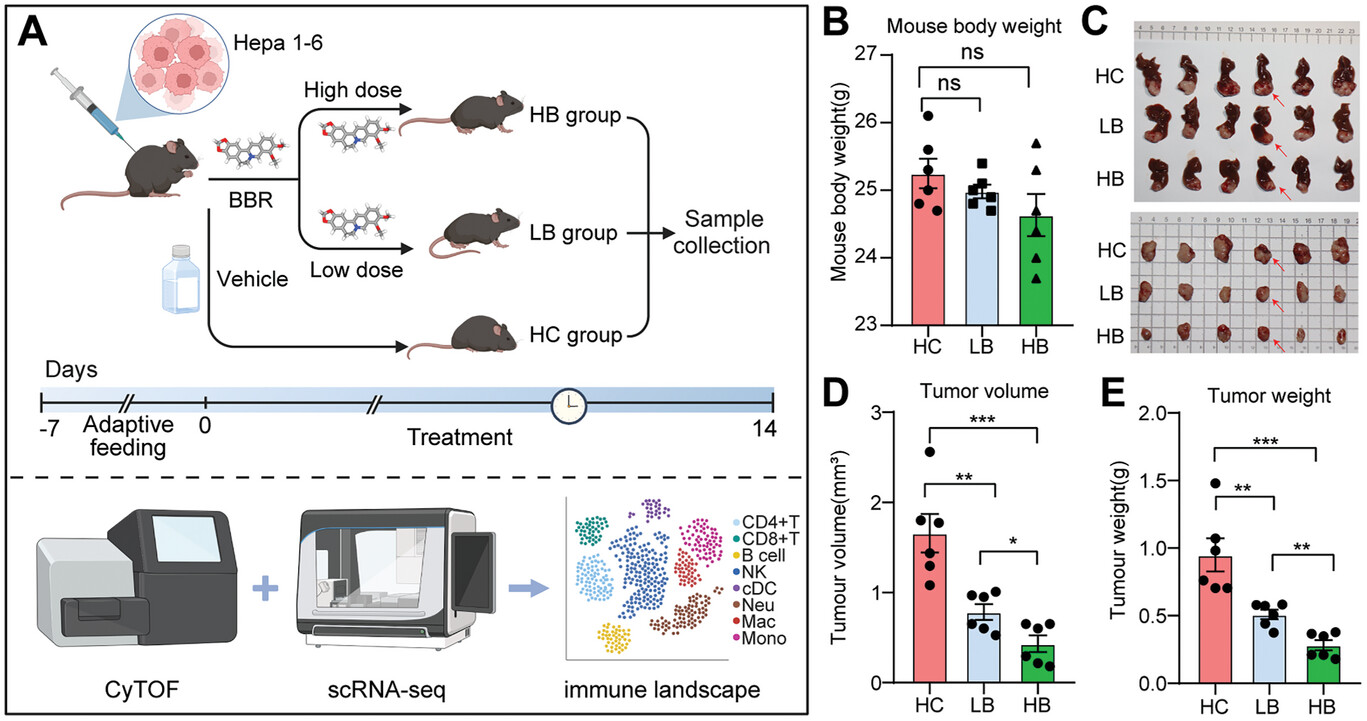
BBR治疗能减少HCC小鼠体内的肿瘤负荷
BBR增强肝癌免疫细胞间的相互作用与通讯
03
CellChat被用来确定各种免疫细胞类型之间的配体-受体相互作用和通信网络。与HC组相比,研究人员观察到高剂量BBR治疗后整体细胞间相互作用的增加。配体-受体分析揭示,高剂量BBR主要通过趋化因子配体-受体对(如CCL3-CCR5、CCL5-CCR5、CXCL16-CXCR6)以及SPP1-(ITGA+ITGB)配体/受体对(如SPP1-(ITGA4+ITGB1)、SPP1-(ITGAV+ITGB1))调节肝脏免疫细胞向CD4+T细胞的信号转导。此外,BBR主要通过包括CCL5-CCR1、CCL5-CCR5、巨噬细胞迁移抑制因子(MIF)-(CD74+CD44)、LGALS9-CD44、LGALS9-CD45、LGALS9-HAVCR2和SPP1-(ITGA+ITGB)在内的配体/受体对介导CD4+T细胞与免疫细胞如MoMF和库普弗细胞之间的细胞间通信。
此外,高剂量BBR通过CCL3-CCR5、CCL5-CCR5、CXCL6-CXCR6和SPP1-(ITGA4+ITGB1)等配体-受体对调节肝癌免疫细胞与CD8+T细胞之间的相互作用。BBR主要通过CCL5-CCR1、CCL5-CCR5和SPP1-(ITGA+ITGB)等配体-受体对促进CD8+T细胞与其他免疫细胞之间的通信。此外,高剂量BBR治疗还可在CD8+T细胞中诱导特定的信号,包括TGFβ、IL1和GDF。综上所述,高剂量BBR的抗肝癌作用可能是通过调节由细胞因子和趋化因子介导的免疫细胞之间的配体-受体相互作用,从而调节肝脏免疫微环境实现的。
研究小结
04
总之,本研究结果表明,BBR通过调节肝内T淋巴细胞的异质性来阻止HCC的发展,具体来说就是增加中央记忆CD8+T细胞的比例,同时减少效应CD8+T细胞的比例,从而逆转T细胞耗竭。此外,BBR还可通过调节T淋巴细胞分泌的细胞因子以及影响其分化状态来抑制HCC。本研究为BBR在HCC中的免疫调节机制提供了新的见解,表明其在HCC管理方面具有潜在的应用前景。(转化医学网360zhyx.com)
【参考资料】
https://onlinelibrary.wiley.com/doi/10.1002/advs.202405182
【关于投稿】
转化医学网(360zhyx.com)是转化医学核心门户,旨在推动基础研究、临床诊疗和产业的发展,核心内容涵盖组学、检验、免疫、肿瘤、心血管、糖尿病等。如您有最新的研究内容发表,欢迎联系我们进行免费报道(公众号菜单栏-在线客服联系),我们的理念:内容创造价值,转化铸就未来!
转化医学网(360zhyx.com)发布的文章旨在介绍前沿医学研究进展,不能作为治疗方案使用;如需获得健康指导,请至正规医院就诊。
 腾讯登录
腾讯登录









还没有人评论,赶快抢个沙发